Aminobenzaldeído
| Aminobenzaldeído | |||
| Nome | 2-Aminobenzaldeído | 3-Aminobenzaldeído | 4-Aminobenzaldeído |
| Outros nomes | o-Aminobenzaldeído orto-Aminobenzaldeído Antranilaldeído |
m-Aminobenzaldeído meta-Aminobenzaldeído |
p-Aminobenzaldeído para-Aminobenzaldeído |
| Fórmula estrutural |  |
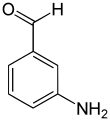 |

|
| Número CAS | 529-23-7 | 1709-44-0 | 556-18-3 |
| PubChem | 68255 | 74366 | 11158 |
| Fórmula molecular | C7H7NO | ||
| Massa molar | 121,14 g·mol−1 | ||
| Estado físico | Sólido | ||
| Ponto de fusão | 40 °C[1] | 72 °C[1] | |
| Ponto de ebulição | |||
| Identificação GHS |
– | ||
| Frases H e P | – | ||
| – | |||
| – | |||
Aminobenzaldeído são um grupo de compostos orgânicos que são formados por um anel benzeno com um grupo amino (–NH2), caracterizando uma amina, e um grupo aldeído (–CHO), como substituintes. Devido a seus diferentes arranjos, tem-se três isômeros com a fórmula C7H7NO. O 2-aminobenzaldeído raramente é tratado pelo seu nome popular "antranilaldeído".
Obtenção[editar | editar código-fonte]
O 2-aminobenzaldeido é preparado a partir de 2-nitrobenzaldeído, por redução com sulfato de ferro (II) e HCl.[2]
A preparação de 4-aminobenzaldeido é realizada a partir de 3-nitrobenzaldeído, por redução com cloreto de estanho II (estanoso) e ácido clorídrico concentrado.[3]
A preparação de 4-aminobenzaldeido é realizada a partir de 4-nitrotolueno por reação com sulfeto de sódio e enxofre (formando polissulfeto de sódio) em solução aquosa de hidróxido de sódio e etanol.[4][5]
Ver também[editar | editar código-fonte]
Referências
- ↑ a b CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ Lee Irvin Smith and J. W. Opie (1948). «o-Aminobenzaldehyde». Org. Synth. 28. 11 páginas. doi:10.15227/orgsyn.028.0011; Coll. Vol., 3
- ↑ R. B. Woodward; m-HYDROXYBENZALDEHYDE; Organic Syntheses, Coll. Vol. 3, p.453 (1955); Vol. 25, p.55 (1945).
- ↑ E. Campaigne, W. M. Budde, and G. F. Schaefer (1951). «p-Aminobenzaldehyde». Org. Synth. 6 páginas. doi:10.15227/orgsyn.031.0006; Coll. Vol., 4
- ↑ Herbert G. Beard and Herbert H. Hodgson; Preparation of p-aminobenzaldehyde, and the mechanism of the reactions of sodium polysulphides with p-nitrotoluene; J. Chem. Soc., 1944, 4-5; DOI: 10.1039/JR9440000004
