Brucina
| Brucina Alerta sobre risco à saúde | |
|---|---|
| |
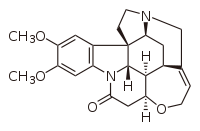
| Nome IUPAC | 2,3-Dimetoxiestricnidin-10-ona |
| Outros nomes | 2,3-Dimetoxiestricnina 10,11-Dimetoxiestricnina |
| Número CAS | |
| Solubilidade | Pouco solúvel em água (3,2 g·l-1 a 15 °C) |
| Ponto de fusão |
178 °C |
| SMILES |
|
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
A brucina é um alcaloide venenoso, muito semelhante à estricnina. É encontrado em inúmeras espécies vegetais, notadamente a Strychnos nux-vomica, ou noz vômica, procedente do sudeste asiático. Embora menos venenosa que a estricnina, seus efeitos são qualitativamente semelhantes. A dose letal para humanos adultos é estimada em 1 grama.[1] Também como a estricnina, é extremamente amarga. Seu sabor é detectável em soluções aquosas com a diluição de 1:220000.[2]
A brucina encontra uso terapêutico no controle da pressão sanguínea e em outras afecções cardíacas.
Propriedades físico-químicas[editar | editar código-fonte]
A brucina tem a mesma estrutura da estricnina, adicionada de dois grupos metóxi substituindo átomos de hidrogênio. Ambos os alcaloides apresentam assimetria óptica, sendo amplamente utilizados como agentes para a resolução quiral (separação de isômeros ópticos), propriedade já descrita em 1853 por Louis Pasteur, e amplamente utilizada nos trabalhos de Hermann Emil Fischer. Foi também utilizando a brucina que W. Marckwald realizou, em 1904, a primeira síntese assimétrica.[3][4] É também utilizada, em presença de ácido sulfúrico concentrado, para a detecção de nitratos, desenvolvendo coloração alaranjada.[5]
Referências culturais[editar | editar código-fonte]
É provável que a mais conhecida referência à brucina seja sua menção no romance O Conde de Monte Cristo, do escritor francês Alexandre Dumas, pai, em que discute o mitridatismo, ou seja a prática de ingerir quantidades crescentes de venenos para tornar-se imune a seus efeitos.
Referências
- ↑ Arlina Borges, "Brucine - 7.2.1.1 Adults" International Programme on Chemical Safety (IPCS), Canadian Centre for Occupational Health and Safety (CCOHS), Abril de 1990.
- ↑ Thieme Chemistry (Hrsg.): RÖMPP Online – Version 3.13. Georg Thieme Verlag KG, Stuttgart 2011
- ↑ Marckwald, W. (1904). «Ueber asymmetrische Synthese». Berichte der deutschen chemischen Gesellschaft. 37. 349 páginas. doi:10.1002/cber.19040370165
- ↑ Marckwald, W. (1904). «Ueber asymmetrische Synthese». Berichte der deutschen chemischen Gesellschaft. 37. 1368 páginas. doi:10.1002/cber.19040370226
- ↑ Jander, Blasius, Lehrbuch der analytischen und präparativen anorganischen Chemie, 12. Auflage, S. Hirzel Verlag, Stuttgart 1983, ISBN 3-7776-0379-1, S. 441.
Ligações Externas[editar | editar código-fonte]
| O Wikisource tem o texto da Encyclopædia Britannica (11.ª edição), artigo: Brucina (em inglês). |
- Brucine, INCHEM.org
