Dicromato de sódio
| Dicromato de sódio Alerta sobre risco à saúde | |
|---|---|
| |
| Outros nomes | Dicromato de sódio hidratado |
| Identificadores | |
| Número CAS | |
| Número RTECS | HX7750000 |
| Propriedades | |
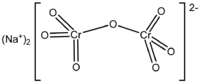
| Fórmula molecular | Na2Cr2O7·2H2O |
| Massa molar | 298.02 g/mol (dihidrato) |
| Densidade | 2.52 g/cm3 |
| Ponto de fusão |
356.7°C |
| Ponto de ebulição |
decompõe-se |
| Solubilidade em água | 2380 g/L at 0°C |
| Riscos associados | |
| Principais riscos associados |
carcinogênico |
| Frases R | R45, R46, R60, R61, R8, R21, R25, R26, R34, R42/43, R48/23, R35, |
| Frases S | S53, S45, S60, S61 |
| Compostos relacionados | |
| Compostos relacionados | K2Cr2O7 KMnO4 CrO3 Na2CrO4 |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Dicromato de sódio, comercialmente também chamado de bicromato de sódio, é o composto químico com a fórmula Na2Cr2O7. Normalmente o sal é usado em sua forma dihidratada Na2Cr2O7·2H2O. Sua química, aparência, e comportamento são muito similares ao de seu similar mais largamente encontrado dicromato de potássio. Esta substância é aproximadamente vinte vezes mais solúvel em água que o similar sal de potássio (49 g/L a 0 °C) e seu peso equivalente é também mais baixo, o que frequentemente é desejável.[1]
Aplicações[editar | editar código-fonte]
Tem aplicação como um conservante para madeira, em especial conjuntamente com o sulfato de cobre, no que é chamado de cromato de cobre ácido, que é uma mistura de sulfato de cobre, dicromato de sódio e trióxido de cromo, patenteada em 1927.[2]
Aplicações em química orgânica[editar | editar código-fonte]
Este composto oxida ligações C-H benzílicas e alicíclicas a derivados carbonila. Por exemplo, 2,4,6-trinitrotolueno é oxidado ao correspondente ácido carboxílico.[3]. Similarmente, 2,3-dimethylnaphthalene é oxidado por Na2Cr2O7 para 2,3-naphthalenedicarboxylic acid (m.p. 239–241 °C).[4]
Segurança[editar | editar código-fonte]
Tal qual muitos compostos de cromo hexavalente, dicromato de sódio é considerado perigoso, possivelmente carcinogênico.
Referências
- ↑ Freeman, F. "Sodium Dichromate" na Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. DOI: 10.1002/047084289.
- ↑ João Carlos Moreschi; PRODUTOS PRESERVANTES DE MADEIRA Arquivado em 24 de dezembro de 2006, no Wayback Machine.; UNIVERSIDADE FEDERAL DO PARANÁ - CURSO DE PÓS-GRADUAÇÃO EM ENGENHARIA FLORESTAL - www.madeira.ufpr.br
- ↑ Clarke, H. T.; Hartman, W. W. “2,4,6-Trinitrobenzoic Acid” Organic Syntheses, Collected Volume 1, p.543 (1941). http://www.orgsyn.org/orgsyn/pdfs/CV1P0543.pdf Arquivado em 30 de setembro de 2007, no Wayback Machine.
- ↑ Friedman, L. “2,3-Naphthalenedicarboxylic Acid” Organic Syntheses, Collected Volume 5, p.810 (1973). http://www.orgsyn.org/orgsyn/pdfs/CV5P0810.pdf Arquivado em 30 de setembro de 2007, no Wayback Machine..
