Sorbato de potássio
| Sorbato de potássio Alerta sobre risco à saúde[1][2] | |
|---|---|

| |
| |
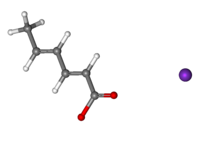
| Nome IUPAC | (2E,4E)-hex-2,4-dienoato de Potássio |
| Outros nomes | E202 Sorbistat-K Sorbistat potassium Sal potássico do ácido 2,4 hexadienóico |
| Identificadores | |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| KEGG | |
| ChEBI | |
| SMILES |
|
| InChI | 1/C6H8O2.K/c1-2-3-4-5-6(7)8;/h2-5H,1H3,(H,7,8);/q;+1/p-1/b3-2+,5-4+;
|
| Propriedades | |
| Fórmula molecular | C6H7KO2 |
| Massa molar | 150.22 g/mol |
| Aparência | Pô granulado branco |
| Densidade | 1.363 g/cm3 |
| Ponto de fusão |
270 °C (decomposição) |
| Solubilidade em água | 58.2% à 20 °C |
| Solubilidade | solúvel em etanol, propileno glicol pouco solúvel em acetona muito pouco solúvel em clorofórmio, óleo de milho, éter insolúvel em benzeno |
| Riscos associados | |
| NFPA 704 | |
| LD50 | 4920 mg/kg (rato, oral) |
| Compostos relacionados | |
| Outros catiões/cátions | Ácido sórbico |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O sorbato de potássio é um sal de potássio do ácido sórbico, conservante fungicida e bactericida, inibidor de crescimento de bolores e leveduras, amplamente utilizado na alimentação como conservante. O ácido sórbico se encontra em forma natural em alguns frutos, contudo geralmente, utiliza-se o sorbato de potássio na indústria alimentar, pois é mais solúvel em água que o ácido sórbico.
Ele impede rancidez e mofos em margarinas e maioneses. Muito utilizado também na produção de queijos de corte, frescos e fundidos. Quando empregado no segmento de bebidas, molhos, doces, panificação entre outras aplicações, evita a formação de mofos e bolores.
Por inibir a ação do fermento, não se deve utilizar este composto em produtos cuja elaboração inclui a fermentação.
Síntese[editar | editar código-fonte]
O sorbato de potássio é produzido industrialmente pela neutralização do ácido sórbico com hidróxido de potássio. O percursor ácido sórbico é produzido em um processo de duas etapas através da condensação de crotonaldeído e cetena.[3][4][5]
Usos[editar | editar código-fonte]
O sorbato de potássio é utilizado para inibir bolores e leveduras em muitos alimentos, como queijos, vinhos, iogurtes, carne-seca, frutas secas, refrigerantes, pães e bolos.[6] Além disso, suplementos dietéticos à base de plantas geralmente contêm sorbato de potássio, que atua na prevenção de mofo e micróbios e no aumento do prazo de validade. É utilizado em quantidades nas quais não são conhecidos efeitos adversos à saúde, durante curtos períodos de tempo.[7]
A rotulagem deste conservante nas declarações dos ingredientes diz "sorbato de potássio" ou "E202". Além disso, é usado em muitos produtos de higiene pessoal e cosméticos para inibir o desenvolvimento de microorganismos para estabilidade de armazenamento. Alguns fabricantes estão usando este conservante como substituto dos parabenos. A alimentação por sonda com sorbato de potássio reduz a carga gástrica de bactérias patogênicas.[8]
Também conhecido como “estabilizador de vinho”, o sorbato de potássio produz ácido sórbico quando adicionado ao vinho. Servindo dois propósitos, quando a fermentação ativa cessa e o vinho é trasfegado pela última vez após a clarificação, o sorbato de potássio torna qualquer levedura sobrevivente incapaz de se multiplicar. A levedura que vive naquele momento pode continuar a fermentar qualquer açúcar residual em CO2 e álcool, mas quando morrer, nenhuma nova levedura estará presente para causar fermentação futura. Quando um vinho é adoçado antes do engarrafamento, o sorbato de potássio é usado para evitar a refermentação quando usado em conjunto com o metabissulfito de potássio. É utilizado principalmente com vinhos doces, espumantes e algumas sidras duras, mas pode ser adicionado a vinhos de mesa, que apresentam dificuldade em manter a clareza após a colagem.
Alguns bolores (nomeadamente algumas estirpes de Trichoderma e Penicillium) e leveduras são capazes de desintoxicar sorbatos por descarboxilação, produzindo piperileno (1,3-pentadieno). O pentadieno se manifesta como um odor típico de querosene ou petróleo.[9]
Toxicologia[editar | editar código-fonte]
Na forma pura, o sorbato de potássio é irritante para a pele, os olhos e as vias respiratórias.[10][11] Concentrações de até 0,5% não são irritantes significativos para a pele.[12]
Como aditivo alimentar, o sorbato de potássio é usado como conservante em concentrações de 0,025 a 0,100%,[13] o que em uma porção de 100 g rende uma ingestão de 25 a 100 mg. Nos Estados Unidos, não é permitido mais de 0,1% em manteigas de frutas, geleias, conservas e produtos relacionados.[14] Até 0,4% foi estudado em picles de fermentação natural com baixo teor de sal e, quando combinado com cloreto de cálcio, 0,2% produziu "picles de boa qualidade".[15] O sorbato de potássio tem cerca de 74% da atividade antimicrobiana do ácido sórbico.[13] Quando calculado como ácido sórbico, 0,3% é permitido em “alimentos de queijo embalados a frio”.[16] O limite superior de pH para eficácia é 6,5.[13]
A ingestão diária máxima aceitável para consumo humano é de 25 mg/kg, ou 1.750 mg por dia para um adulto médio (70 kg).[17][18] Em algumas condições, particularmente em concentrações elevadas ou quando combinado com nitritos, o sorbato de potássio demonstrou atividade genotóxica in vitro.[18]
Três estudos realizados na década de 1970 não revelaram quaisquer efeitos cancerígenos em ratos.[19][20][21]
Indicações de Segurança[editar | editar código-fonte]
Apesar de classificado como irritante em alguns lugares, esse conservante é considerado seguro e suave por conta de seu longo histórico de segurança e perfil não-tóxico. O Sorbato de Potássio é não-irritante e não-sensibilizante. Reações alérgicas são muito raras e ele é bem tolerado quando administrado internamente.
Ver também[editar | editar código-fonte]
Referências
- ↑ Merck Index, 11th Edition, 7661.
- ↑ Potassium sorbate at Sigma-Aldrich
- ↑ Erich Lück, Martin Jager and Nico Raczek "Sorbic Acid" in Ullmann's Encyclopedia of Industrial Chemistry, 2011, Wiley-VCH, Weinheim. doi:10.1002/14356007.a24_507.pub2
- ↑ patent process for commercial potassium sorbate Arquivado em 2012-01-31 no Wayback Machine
- ↑ «Agricultural Marketing Service». www.ams.usda.gov. Consultado em 21 de setembro de 2012. Arquivado do original em 11 de junho de 2014
- ↑ Erich Lück, Martin Jager and Nico Raczek "Sorbic Acid" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2000.doi:10.1002/14356007.a24_507
- ↑ «036. Sorbate, potassium (FAO Nutrition Meetings Report Series 40abc)». Inchem.org. Consultado em 22 de fevereiro de 2013
- ↑ Tulamait, Aiman; Laghi, Franco; Mikrut, Kathleen; et al. (2005). «Potassium sorbate reduces gastric colonization in patients receiving mechanical ventilization». J. Crit. Care. 20 (3): 281–287. PMID 16253799. doi:10.1016/j.jcrc.2005.03.002
- ↑ The Soft Drinks Companion – A technical handbook for the beverage industry, Chapter 10.
- ↑ «Potassium Sorbate» (PDF). Chem One, Ltd. 14 de junho de 2010. Consultado em 4 de maio de 2015[ligação inativa]
- ↑ «Sorbic Acid - National Library of Medicine HSDB Database». National Institute of Health
- ↑ Elder, R. E. (1988). «Final report on the safety assessment of sorbic acid and potassium sorbate.» (PDF). J Am Coll Toxicol. 7 (6): 837–880. doi:10.3109/10915818809078711. Consultado em 26 de maio de 2018. Arquivado do original (PDF) em 27 de maio de 2018
- ↑ a b c «Potassium sorbate - Agricultural Marketing Service - USDA» (PDF). U.S. government. Consultado em 26 de maio de 2018.
Potassium sorbate is effective against yeasts, molds, and select bacteria, and is widely used at 0.025 to 0.10 % levels in cheeses, dips, yogurt, sour cream, bread, cakes, pies and fillings, baking mixes, doughs, icings, fudges, toppings, beverages, margarine, salads, fermented and acidified vegetables, olives, fruit products, dressings, smoked and salted fish, confections and mayonnaise.
- ↑ «21 CFR 150 - Fruit butters, jellies, preserves, and related products» (PDF). Government Printing Office. 1 de abril de 2011. Consultado em 25 de maio de 2018
- ↑ Guillou, A.A.; Floros, J.D.; Cousin, M.A. (1992). «Calcium Chloride and Potassium Sorbate Reduce Sodium Chloride used during Natural Cucumber Fermentation and Storage». Journal of Food Science. 57 (6): 1364–1368. ISSN 0022-1147. doi:10.1111/j.1365-2621.1992.tb06859.x
- ↑ «21 CFR 133 - Cheeses and related cheese products» (PDF). Government Printing Office. 1 de abril de 2011. Consultado em 25 de maio de 2018
- ↑ «036. Sorbate, potassium (FAO Nutrition Meetings Report Series 40abc)». Inchem.org. Consultado em 22 de fevereiro de 2013
- ↑ a b Carocho, Márcio; Barreiro, Maria Filomena; Morales, Patricia; Ferreira, Isabel C. F. R. (2014). «Adding Molecules to Food, Pros and Cons: A Review on Synthetic and Natural Food Additives». Comprehensive Reviews in Food Science and Food Safety. 13 (4): 377–399. PMID 33412697. doi:10.1111/1541-4337.12065. hdl:10198/12042

- ↑ Hendy, R. J.; Hardy, J.; Gaunt, I. F.; Kiss, I. S.; Butterworth, K. R. (1976). «Long-term toxicity studies of sorbic acid in mice». Food and Cosmetics Toxicology. 14 (5): 381–386. PMID 1010505. doi:10.1016/S0015-6264(76)80173-3
- ↑ Gaunt, I. F.; Butterworth, K. R.; Hardy, J.; Gangolli, S. D. (1975). «Long-term toxicity of sorbic acid in the rat». Food and Cosmetics Toxicology. 13 (1): 31–45. PMID 1123201. doi:10.1016/0015-6264(75)90080-2
- ↑ Mason, P. L.; Gaunt, I. F.; Hardy, J.; Kiss, I. S.; Butterworth, K. R.; Gangolli, S. D. (1976). «Long-term toxicity of parasorbic acid in rats». Food and Cosmetics Toxicology. 14 (5): 387–394. PMID 1010506. doi:10.1016/S0015-6264(76)80174-5
Ligações externas[editar | editar código-fonte]
- (em português)Características do Sorbato de Potássio

