Tetracloreto de titânio
Tetracloreto de titânio ou cloreto de titânio (IV) é o composto inorgânico com a fórmula TiCl4. É um importante intermediário na produção do metal titânio e do pigmento dióxido de titânio.
TiCl4 é um exemplo incomum de um haleto metálico que é altamente volátil. Em contato com a humidade do ar, ele forma "cortinas de fumaça" muito densas de Dióxido de titânio (TiO2) e Ácido clorídrico (HCℓ).[1]-->
Aplicações[editar | editar código-fonte]
Produção do metal Titânio[editar | editar código-fonte]
A produção mundial de Titânio é da ordem de 4 Milhões de toneladas / ano, e é feito de TiCl4, usando o Processo Kroll.
- 2 Mg + TiCl4 → 2 MgCl2 + Ti
Produção de dióxido de titânio[editar | editar código-fonte]
Cerca de 90% da produção de TiCl4, é usado para fazer o pigmento Dióxido de titânio, envolvendo o processo de hidrólise.[2]
- TiCl4 + 2 H2O → TiO2 + 4 HCl
Cortinas de fumaça[editar | editar código-fonte]
O Tetracloreto de titânio, também tem sido usado para produzir "cortinas de fumaça" para uso militar, pois gera uma fumaça branca com baixa tendência à dissipação.[3]
Reações químicas[editar | editar código-fonte]
O Tetracloreto de titânio, é um reagente versátil que forma vários outros compostos, incluindo os ilustrados abaixo.
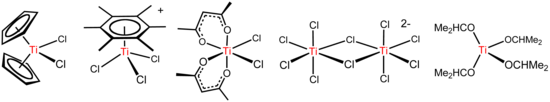
Ver também[editar | editar código-fonte]
Referências[editar | editar código-fonte]
- ↑ [1] American Chemistry
- ↑ Hans G. Völz et al. “Pigments, Inorganic” in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2006. doi:10.1002/14356007.a20_243.pub2
- ↑ The Royal Navy at War (DVD). London: Imperial War Museum. 2005



