Tioéster
Os tioésteres são compostos orgânicos semelhantes aos ésteres onde um dos átomos de oxigênio é substituído por um átomo de enxofre. Há dois tipos de tioésteres, os tiolésteres e os tionoésteres. Os tiolésteres, que contém o grupo funcional C-S-CO-C, são de longe, os mais importantes e por isto é sempre a eles que se refere quando se fala apenas em tioésteres. São produto da esterificação de um ácido carboxílico com um tiol. Os tioésteres são parte importante da química dos organismos vivos, com especial destaque para a acetil-CoA.

Síntese[editar | editar código-fonte]
De modo análogo ao das rotas sintéticas de preparação de ésteres, os tioésteres resultam da reação de tióis e ácidos carboxílicos na presença de agentes desidratantes: [1]
- RSH + R'CO2H → RSC(O)R' + H2O
Um agente desidratante muito utilizado para este propósito é a N,N'-Diciclohexilcarbodiimida (DCC). Os anidridos e algumas lactonas também reagem com tióis em presença de bases.
Podem também ser produzidos pela carbonilação de alquinos e alquenos na presença de tióis.[2]
Reações[editar | editar código-fonte]
O centro carbonílico dos tioésteres é reativo frente aos agentes nucleófilos. Esta reatividade assemelha-se com a dos cloretos de ácidos, embora seja um pouco mais branda. Desta forma os tioésteres reagem com as aminas formando amidas:
- R"NH2 + RSC(O)R' → R"2NC(O)R' + RSH
Os grupamentos C-H adjacentes à carbonila nos tioésteres têm caráter levemente acídico e participam de condensações aldólicas. Esta reação é fundamental na biossíntese dos ácidos graxos pois graças a ela ocorre, dois a dois, o aumento do número de átomos de carbono nas cadeias.
Bioquímica[editar | editar código-fonte]
Tioésteres são intermediários comuns em muitas reações biossintéticas, incluindo a formação e degradação dos ácidos graxos e do mevalonato, precursor dos esteróides. A biossíntese da lignina procede a partir do derivado tioéster do ácido caféico.[3] São exemplos de tioésteres a malonil-CoA, a acetoacetil-CoA, a propionil-CoA e a cinamoil-CoA. A acetogênese procede por intermédio da formação da acetil-CoA. A biossíntese dos tioésteres procede de modo análogo aos processos de síntese descritos anteriormente, mas utiliza-se do ATP como agente desidratante.
Tioésteres e a origem da vida[editar | editar código-fonte]
A importância central dos tioésteres nos mecanismos de produção e utilização de recursos energéticos nos organismos vivos levou Christian de Duve a postular o Mundo do Tioéster, como uma etapa necessária na evolução primitiva dos processos vitais.
Compostos isômeros: os tionoésteres[editar | editar código-fonte]
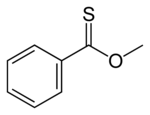
Os tionoésteres são isômeros dos tioésteres. Num tionoéster, o enxofre substitui o oxigênio da carbonila do éster. O tionobenzoato de metila tem como fórmula C6H5C(S)OCH3. Estes compostos são tipicamente preparados pela reação de um cloreto de tioacila com um álcool, mas tambem podem ser resultar da ação do reagente de Lawesson com ésteres. [4]

Referências[editar | editar código-fonte]
- ↑ http://www.organic-chemistry.org/synthesis/C1S/thioesters.shtm
- ↑ Werner Bertleff, Michael Roeper, Xavier Sava “Carbonylation” Ullmann's Encyclopedia of Industrial Chemistry 2007, Wiley-VCH. {DOI| 10.1002/14356007.a05_217.pub2}
- ↑ Nelson, D. L.; Cox, M. M. "Lehninger, Principles of Biochemistry" 3rd Ed. Worth Publishing: New York, 2000. ISBN 1-57259-153-6.
- ↑ R. J. Cremlyn “An Introduction to Organosulfur Chemistry” John Wiley and Sons: Chichester (1996). ISBN 0 471 95512 4.
