Vírus da imunodeficiência humana
| Vírus da imunodeficiência humana | |||||||
|---|---|---|---|---|---|---|---|
| Classificação científica | |||||||
| |||||||
| Espécies | |||||||
| |||||||
O Vírus da Imunodeficiência Humana (VIH ou HIV, do inglês Human Immunodeficiency Virus) é um lentivírus que está na origem da Síndrome da Imunodeficiência Adquirida,[1][2] uma condição em seres humanos na qual a deterioração progressiva do sistema imunitário propicia o desenvolvimento de infeções oportunistas e cancros potencialmente mortais. A infeção com o VIH tem origem na transferência de sangue, sémen, lubrificação vaginal, fluido pré-ejaculatório ou leite materno. Na saliva a transmissão é mínima em termos estatísticos.[3] O VIH está presente nestes fluidos corporais, tanto na forma de partículas livres como em células imunitárias infectadas. As principais vias de transmissão são as relações sexuais desprotegidas, a partilha de seringas contaminadas, e a transmissão entre mãe e filho durante a gravidez ou amamentação. Em países desenvolvidos, a monitorização do sangue em transfusões praticamente eliminou o risco de transmissão por esta via.
A infeção por VIH em seres humanos é atualmente uma pandemia. Cerca de 0,6% da população mundial está infetada com o VIH.[4] Entre 1981 e 2006, a SIDA foi responsável pela morte de mais de 25 milhões de pessoas. Um terço destas mortes ocorreu na África subsariana, atrasando o crescimento económico e aumentando a pobreza.[5] Até 2013, estimou-se que 78 milhões de pessoas foram contaminadas,[6] 39 milhões das quais morreram.[7]
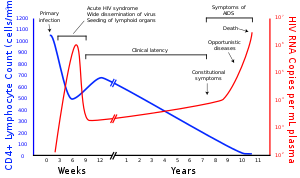
O VIH infecta células vitais no sistema imunitário, como os linfócitos T auxiliares CD4+, macrófagos e células dendríticas.[8] A infeção por VIH provoca a diminuição do número linfócitos T CD4+ através de diversos mecanismos, entre os quais a apoptose de células espectadoras,[9] a morte viral direta de células infectadas, e morte de linfócitos T CD4+ através de linfócitos T citotóxicos CD8 que reconhecem as células infectadas.[10] Quando o número de linfócitos T CD4+ desce abaixo do limiar aceitável, o corpo perde a imunidade mediada por células e torna-se progressivamente mais suscetível a infeções oportunistas.
A maior parte das pessoas infetadas com VIH, quando estão sem tratamento, desenvolve SIDA. A elevada mortalidade desta doença deve-se ao colapso progressivo do sistema imunitário, ao qual está associado o aparecimento de infeções oportunistas ou tumores malignos.[11] Sem tratamento, cerca de nove em cada dez pessoas infetadas com VIH desenvolve SIDA após de 10-15 anos, embora algumas pessoas desenvolvam muito mais cedo.[12] O tratamento com antirretrovirais aumenta a esperança de vida de portadores do VIH, mesmo que a infeção tenha já evoluído para um diagnóstico de SIDA. Com a entrada de novos antiretrovirais a expectativa passou para algo em torno de 20-50 anos (provavelmente, esta expectativa pode ser ainda maior, posto que atualmente há novos medicamentos e terapias mais toleráveis ao organismo dos portadores). Para pessoas com HIV em tratamento antiretroviral de longo prazo e com alta contagem de células CD4, estima-se que a expectativa de vida seja próxima à da população em geral, independentemente de quando iniciaram o tratamento.[13]
Avanços na medicina permite relacionamentos entre casais sorodiferentes, em que uma pessoa vive com HIV e a outra não sem que haja a transmissão do vírus. Pessoas vivendo com HIV em tratamento e com carga viral indetectável a pelo menos seis meses não transmitem o vírus por via sexual. O termo Indetectável = Intransmissível (I = I) é adotado por cientistas e instituições de referência sobre o HIV em abrangência mundial.[14][15]
Virologia[editar | editar código-fonte]
Classificação[editar | editar código-fonte]
| Espécie | Virulência | Infectividade | Prevalência | Origem deduzida |
|---|---|---|---|---|
| VIH-1 | Elevada | Elevada | Global | Chimpanzé-comum |
| VIH-2 | Muito baixa | Baixa | África Ocidental | Cercocebus atys |
O VIH é um membro do género Lentivirus,[16] e parte da família Retroviridae.[17] Os lentivírus têm diversas propriedades morfológicas e biológicas em comum. Muitas espécies são infectadas por lentivírus, que são caracteristicamente responsáveis por doenças de longa duração com período de incubação longo.[18] Os lentivírus são transmitidos como vírus ARN encapsulados, de sentido positivo e de cadeia única. Ao entrar na célula-alvo, o genoma ARN viral é convertido em ADN de cadeia dupla pela transcriptase reversa, que é transportada juntamente com o genoma viral na partícula do vírus. O ADN viral resultante é então importado para o núcleo celular e integrado no ADN celular pela integrase e cofactores. Uma vez integrado, o vírus pode tornar-se latente, permitindo-lhe a si e à célula hospedeira não serem detectados pelo sistema imunitário. Em alternativa, o vírus pode ser transcrito, produzindo novos genomas ARN e proteínas virais que são libertadas das células como novas partículas virais que iniciam novamente o ciclo de reprodução.[19]
Foram identificados dois tipos de VIH: o VIH-1 e o VIH-2. O VIH-1 é o vírus que foi inicialmente descoberto e denominado LAV e HTLV-III. É o mais virulento, mais infeccioso,[20] e o que provoca a maioria das infeções por VIH a nível mundial. A menor infecciosidade do VIH-2 em comparação com o VIH-1 indica que, a cada exposição, o risco de contágio é menor. Devido à sua reduzida capacidade de contágio, o VIH-2 está maioritariamente restrito à África Ocidental.[21]
Estrutura e genoma[editar | editar código-fonte]

A estrutura do VIH é diferente da de outros retrovírus. É aproximadamente esférica e com um diâmetro de cerca de 120 nm, cerca de 60 vezes menor que um glóbulo vermelho, ainda que grande para um vírus.[22][23] É composto por duas cópias de ARN positivo de cadeia única de senso positivo com aproximadamente 9749 nucleotídeos[24] que codifica os nove genes do vírus, envolto por um capsídeo cónico composto de 2 milcópias da proteína viral p24.[25] O ARN de cadeia único está intimamente ligado às proteínas da nucleocapside, p7, e às enzimas necessárias ao desenvolvimento do virião como a Transcriptase reversa, a aspartate protease, ribonuclease e integrase. O capsídeo é envolto por uma matriz composta pela proteína viral p17, assegurando a integridade da partícula do virião.[25]
Este conjunto é por sua vez envolto pelo envelope viral, que é composto por duas camadas de moléculas gordas denominadas fosfolípidos, obtidas a partir da membrana de uma célula humana quando uma partícula viral recém-formada brota da célula. No envelope viral estão incorporadas proteínas da célula anfitriã e cerca de 70 cópias de uma proteína complexa do VIH que é proeminente na superfície da partícula viral.[25] Esta proteína, conhecida por Env, consiste num conjunto de três moléculas denominadas glicoproteína (gp) 120, e uma haste que consiste em três moléculas gp41 que ligam a estrutura ao envelope viral.[26] Este complexo glicoproteico permite ao vírus ligar-se e fundir-se com as células-alvo de modo a dar início ao ciclo de infeção.[26] Estas duas proteínas de superfície, sobretudo a gp120, têm vindo a ser identificadas como o alvo de futuros tratamentos ou vacinas contra o VIH.[27]
O genoma de ARN consiste em pelo menos sete marcos estruturais (LTR, TAR, RRE, PE, SLIP, CRS e INS) e nove genes ('gag, pol, and env, tat, rev, nef, vif, vpr, vpu, e por vezes um décimo tev, que consiste numa fusão de tat, env e rev), codificando 19 proteínas. Três destes genes, gag, pol e env, contêm a informação necessária para produzir as proteínas estruturais de novas partículas virais.[25] por exemplo, o env codifica uma proteína denominada gp160 que é quebrada por uma protease celular de modo a formar gp120 e gp41. Os restantes seis genes, 'tat, rev, nef, vif, vpr, e vpu (ou vpx no caso do VIH-2), são genes reguladores para proteínas que controlam a capacidade do VIH em infectar céulas, produzir novas cópias de si mesmo (replicar-se) ou provoca a doença.[25]
As duas proteínas Tat (p16 e p14) são trans-ativadores transcricionais do LTR, atuando ao ligar o elemento ARN do TAR. O TAR pode também ser processado em micro-ARNs que regulam os genes da apoptose ERCC1 e IER3.[28][29] A proteína Rev (p19) está envolvida no encerramento dos ARN do núcleo e do citoplasma, ao ligar-se ao elemento de ARN RRE. A proteína Vif (p23) previne a acção da APOBEC3G (uma proteína celular que devide os híbridos de ADN:ARN e/ou interfere com a proteína Pol). A proteína Vpr (p14) pára a divisão celular e G2/M. A proteína Nef (p27) infra-regula o CD4 (o maior recetor viral), assim como as moléculas MHC classe I e II.[30][31][32] A proteína Vpu (p16) influencia a libertação de novas partículas virais a partir de células infectadas.[25] As extremidades de cada cadeia de ARN do HIV contêm uma sequência de ARN denominada long terminal repeat (LTR). As regiões no LTR atuam como interruptores que controlam a produção de novos vírus e podem ser ativadas pelas proteínas quer do VIH quer da célula anfitriã. O elemento Psi está envolvido no envelope do genoma viral e é reconhecido pelas proteínas Gag e Rev. O elemento SLIP está envolvido no deslocamento do quadro de leitura Gag-Pol, necessário para a produção de Pol funcional.[25]
Tropismo[editar | editar código-fonte]

O termo tropismo viral refere-se ao tipo de células que determinado vírus infeta. O VIH pode infetar diversas células imunitárias, como os linfócitos T CD4+, macrófagos e microgliócitos. A entrada do VIH-1 nos macrófagos e nos linfócitos CD4+ é mediada através da interação das glicoproteínas do envelope do virião (gp120) com a molécula CD4 nas células-alvo, e ainda através de co-recetores de quimiocina.[26]
As cadeias do VIH-1 que afectam os macrófagos (M-trópicas) usam os co-recetores de quimiocina CCR5 para entrar, sendo assim capazes de se replicarem em macrófagos e linfócitos T CD4+.[33] Este co-recetor CCR5 é usado por praticamente todos os tipos primários de VIH-1, independentemente do seu subtipo genético. Assim, os macrófagos desempenham um papel essencial em vários aspetos fundamentais da infeção por VIH, aparentando ser as primeiras células a ser infetadas e talvez a fonte de produção de VIH a partir do momento em que o doente perde as células CD4. Em amígdalas e adenoides de doentes infetados com VIH, os macrófagos fundem-se em células de grandes dimensões e vários núcleos que produzem grandes quantidades de partículas virais. As cadeias T-trópicas replicam-se tanto em linfócitos T CD4+ como em macrófagos e usam para entrar o co-recetor de quimioquina CXCR4.[33][34][35] Pensa-se que as cadeias VIH-1 de tropismo duplo sejam cadeias de VIH-1 em transição, e portanto capazes de usar como co-recetores de entrada tanto o CCR5 como o CXCR4. A quimioquina-alfa SDF-1, um ligante do CXCR4, suprime a replicação dos tipos T-trópicos. Consegue-o através da infra-regulação da expressão do CXCR4 na superfície destas células. O VIH que usa apenas o co-recetor CCR5 é denominado R5; o que usa apenas o CXCR4 é denominado X4; e o que usa ambos é denominado X4R5. No entanto, o uso do co-recetor por si só não explica o tropismo viral, já que nem todos os vírus R5 são capazes de usar o CCR5 em macrófagos de modo a dar origem a uma infeção bem sucedida e o VIH pode também infetar um subtipo de células dendríticas mieloides, que provavelmente constituem uma reserva que mantém a infeção quando a contagem de células CD4+ desce para níveis extremamente baixos.[33][36] Algumas pessoas são resistentes a determinadas estirpes de VIH.Por exemplo, pessoas com a mutação CCR5-Δ32 são resistentes a infeções com o vírus R5, uma vez que a mutação impede o VIH de se ligar ao seu co-recetor, reduzindo a sua capacidade de infetar células-alvo.[37]
A relação sexual é o principal meio de transmissão do VIH. Tanto o VIH X4 como o R5 estão presentes no sémen que é transmitido entre o homem e o seu parceiro sexual. Os viriões podem assim infetar vários alvos celulares e disseminar-se por todo o organismo. No entanto, a existência de um processo de seleção faz com que através desta via seja predominante a transmissão do vírus R5.[38][39][40] A forma como o processo seletivo funciona está ainda a ser investigada, mas um dos modelos propõe que os espermatozoides possam seletivamente transportar VIH R5, uma vez que na superfície possuem CCR3 e CCR5, mas não CXCR4,[41] e que as células epiteliais genitais sequestram de forma preferencial vírus X4.[42] Em pessoas infetadas com o subtipo HIV-1, muitas vezes verifica-se a troca de co-recetor durante a fase avançada da doença, e as variantes T-trópicas aparentam poder infetar diferentes linfócitos T através do CXCR4.[43] Estas variantes replicam-se então de forma mais agressiva e com maior virulência, o que provoca a diminuição acentuada dos linfócitos T, o colapso do sistema imunitário e o aparecimento de infeções oportunistas, características da SIDA.[44] Assim, durante o curso da infeção, a adaptação viral para passar a usar o CXCR4 em vez do CCR5 pode representar um passo fundamental na progressão para a SIDA. Vários estudos em indivíduos infetados com o subtipo B concluíram que 40 a 50% dos pacientes com SIDA podem apresentar vírus T-trópicos e, presume-se, fenótipos X4.[45][46]
O VIH-2 é muito menos patogénico do que o VIH-1 e a sua ocorrência é mais restrita em termos globais. A adoção de "genes acessórios" pelo VIH-2 e o seu padrão promíscuo de utilização de coreceptores (incluindo a independência relativamente ao CD4) pode auxiliar o vírus na sua adaptação de forma a evitar fatores de restrição inatos presentes nas células anfitriãs. A capacidade do VIH-2 em se replicar nos seres humanos pode ter origem na capacidade de adaptação do vírus, de modo a ser capaz de usar processos celulares normais de forma a permitir a transmissão e a infeção produtiva. Uma das estratégias de sobrevivência de qualquer agente infecioso é não matar o seu hospedeiro, mas antes estabelecer uma relação de comensalismo entre organismos. Tendo conseguido obter baixa patogenicidade, ao longo do tempo irão sendo selecionadas as variantes mais eficazes na transmissão.[47]
Ciclo de replicação[editar | editar código-fonte]


Penetração celular[editar | editar código-fonte]
O VIH penetra nos macrófagos e nos linfócitos T CD4+ através da adsorção de glicoproteínas na sua superfície para recetores na célula-alvo, seguida pela fusão do envelope viral com a membrana celular e pela libertação do capsídeo do VIH na célula.[48][49]
A penetração na célula tem início com a interação do complexo envelope trímero (gp160) com o CD4 e um recetor de quimiocina na superfície da célula (geralmente o CCR5 ou CXCR4, embora sejam conhecidos outros).[48][49] A gp120 liga-se à integrina α4β7, ativando o LFA-1, a principal integrina envolvida no estabelecimento de sinapses virológicas, que facilita a disseminação eficiente do VIH-1 entre células.[50] A gp160 contém domínios de ligação tanto para o CD4 como para os recetores de quimioquina.[48][49]
O primeiro estágio na fusão envolve a união dos domínios de ligação CD4 da gp120 ao CD4. Uma vez ligada a gp120 com a proteína CD4, o complexo envelope atravessa uma alteração na estrutura, expondo os domínios de ligação de quimioquina da gp120 e permitindo-lhes interagir com o recetor-alvo de quimioquina.[48][49] Isto permite uma ligação mais estável, o que permite ao peptídeo de fusão N-terminal gp41 penetrar na membrana celular.[48][49] Em seguida, as sequências de repetição na gp41, HR1 e HR2 interagem entre si, provocando o colapso da porção extracelular da gp41 num hairpin. Esta estrutura circular aproxima o vírus da membrana celular, permitindo a fusão das suas membranas e consequente entrada do capsídeo viral.[48][49]
Depois do VIH se ligar à célula-alvo, injeta nela o seu ARN e as suas diversas enzimas, incluindo a transcriptase reversa, integrase, ribonuclease e protease.[48] O VIH pode infetar células dendríticas (CD) através do processo CD4-CCR5, embora possa também usar recetores de lectina tipo C.[51] As células dendríticas são uma das primeiras células que o vírus encontra durante a transmissão por via sexual. Atualmente, pensa-se que as CD desempenhem um papel importante na transmissão do VIH para os linfócitos, durante o momento em que o vírus é capturado na mucosa.[51] Acredita-se que a presença da proteína FEZ-1, que ocorre naturalmente em neurónios, impeça que o VIH infecte as células.[52]
Replicação e transcrição[editar | editar código-fonte]

Pouco depois do capsídeo viral penetrar na célula, uma enzima denominada transcriptase reversa liberta o genoma ARN de cadeia única das proteínas virais, e copia-o para uma molécula complementar de ADN.[53] O processo de transcrição reversa é extremamente predisposto a erros e as mutações daí resultantes podem provocar resistência aos anti-virais ou permitir ao vírus evadir o sistema imunitário. A transcriptase reversa tem também atividade de ribonuclease, que degrada o ARN viral durante a síntese de ADN complementar, assim como atividade de ADN polimerase ADN-dependente, capaz de criar ADN de sentido positivo a partir do ADN complementar de sentido negativo.[54] Juntos, o ADN complementar e o seu complemento forma um ADN viral de cadeia dupla que é assim transportado para o núcleo celular. A integração do ADN viral com o genoma das células anfitriãs é realizada por outra enzima viral, denominada integrase.[53]
O ADN viral, agora integrado na célula, pode permanecer dormente durante a fase latente da infeção.[53] De forma ao vírus poder ser produzido de forma ativa, têm que estar presentes determinados fatores de transcrição, o mais importante dos quais o NF-κB (factor nuclear kappa B), que é depois supra-regulado quando os linfócitos T são ativados.[55]
Durante a replicação viral, o AND proviral integrado é transcrito para ARNm, que é depois reorganizado através de splicing em partes mais pequenas. Estas partes são exportadas do núcleo para o citoplasma, onde são transcritas para as proteínas reguladoras Tat (que incentiva a produção de novos vírus) e Rev. À medida que as proteínas Rev recém-formadas se acumulam no núcleo, vão-se ligando ao ARNm viral e permitem ao ARN que ainda não sofreu splicing abandonar o núcleo, onde de outra forma são retidos até sofrerem splicing.[56]
Recombinação[editar | editar código-fonte]
Em cada partícula de VIH-1 estão encapsulados dois genomas ARN. Durante a infeção e replicação catalisadas pela transcriptase reversa, pode ocorrer recombinação entre estes dois genomas.[57][58] A recombinação ocorre quando os genomas ARN+ de cadeia única são transcritos reversamente para formar ADN. Durante a transcrição reversa o novo ADN pode alternar diversas vezes entre as duas cópias do ARN viral. Esta forma de recombinação é denominada cópia-escolha. Os processos de recombinação podem ocorrer ao longo de todo o genoma, e entre 2 e 20 eventos por genoma em cada ciclo de replicação. Estes eventos podem alterar rapidamente a informação genética que é transmitida dos genomas progenitores para os descendentes.[58]
A recombinação viral produz variação genética que é provável que contribua para a evolução da resistência à terapia antiviral.[59] A recombinação pode também contribuir, em princípio, para vencer as defesas imunitárias do hospedeiro. No entanto, para que as vantagens adaptativas da variação genética ocorram, os dois genomas virais contidos em cada uma das partículas de vírus devem ter origem em diferentes vírus progenitores e de constituição genética distinta. Não se sabe ainda com que frequência este fenómeno ocorre em condições naturais.[60]
Um estudo sugeriu que a alternância do modelo por parte da transcriptase reversa atua como processo de reparação das quebras no genoma ssARN.[61] Outro estudo sugeriu que a recombinação é uma adaptação tendo em vista a reparação de danos nos genomas ARN.[57] A variação na troca de fita pela transcriptase reversa poderia gerar uma cópia não danificada de ADN genómico a partir de duas cópias danificadas de genoma ssARN. Este ponto de vista dos benefícios da recombinação no VIH poderia explicar porque é que cada partícula de VIH contém dois genomas completos, em vez de apenas um. Além disso, no ponto de vista que sustenta que a recombinação no VIH é um processo de reparação está implícito que esse benefício possa ocorrer a cada ciclo de replicação, e que o benefício possa ser conseguido quer os genomas sejam ou não diferentes em termos genéticos.[61]
A infeção por VIH-1 provoca um processo inflamatório contínuo e a produção de espécies reativas de oxigénio.[62] Assim, o genoma do VIH pode ser vulnerável a danos de oxidação, incluindo quebras no ARN de fita única. No caso do VIH, e para todos os vírus de forma genérica, a infeção bem sucedida está dependente de superar as estratégias defensivas do hospedeiro, que normalmente incluem a produção de oxigénio reativo capaz de destruir genoma. Um estudo sugeriu que a recombinação por parte dos vírus é uma adaptação com o objetivo de reparar os danos no genoma, e que a variação na recombinação é um subproduto que pode trazer benefícios acrescidos.[63]
Montagem e lançamento[editar | editar código-fonte]
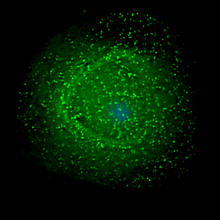
O último passo do ciclo viral, a montagem dos viriões do novo VIH-1, tem início na membrana de plasma da célula anfitriã. A poliproteína Env (gp160) atravessa o retículo endoplasmático e é transportada para o complexo de Golgi, onde é dividida pela furina, dando origem às duas glicoproteínas do envelope do VIH, gp41 e gp120.[64] Estas proteínas são transportadas para a membrana plasmática da célula anfitriã, na qual a gp41 fixa a gp120 à membrana da célula infetada. As poliproteínas Gag (p55) e Gag-Pol (p160) também interagem com a superfície interior da membrana plasmática, em conjunto com o ARN genómico do VIH, à medida que o virião em formação começa a despontar da célula anfitriã. Este novo virião encontra-se ainda imaturo, uma vez que as poliproteínas Gag precisam ainda de ser separadas em proteínas de matriz, capsídeo e nucleocapsídeo. Esta divisão é mediada pela protease viral e pode ser inibida por fármacos antirretrovirais da classe dos inibidores da protease. Finalmente, os vários componentes são montados de modo a produzir um virião de VIH amadurecido, que são os únicos capazes de infetar outras células.[65]
Latência e reservatórios de HIV[editar | editar código-fonte]
O vírus HIV se replica em linfócitos T CD4+ ativos, porque estes expressam fatores necessários para transcrição reversa, integração e expressão do DNA viral. Como exemplo de um fator que interfere na expressão do DNA viral está o fator de transcrição pró-inflamatório NF-κB, cuja expressão é induzida após ativação de linfócitos T CD4+; tal fator tem um papel importante no início da transcrição da sequência de DNA viral e expressão das proteínas virais primárias.[66]
Os dois primeiros processos não ocorrem nos linfócitos T CD4+ em repouso (que não foram ativados pela apresentação de um antígeno específico) infectados, caracterizando a latência pré-integração. Esse DNA viral extracromossomal (que não está integrado) permanece viável por semanas após a infecção, constituindo um reservatório por certo intervalo de tempo, uma vez que, se tais células forem ativadas subsequentemente à infecção, o DNA viral se integrará e poderá gerar novos vírus.[67]
Quando ocorre a ativação dos linfócitos T CD4+, que podem já estar infectados com o vírus ou serem infectados posteriormente à sua ativação, há estimulo para a proliferação celular e, assim, é possível que ocorra a integração do DNA viral e replicação do HIV; porém este estado é transitório e, após um tempo, os linfócitos voltam à fase de repouso como células de memória. Com isso, proteínas virais deixam de ser expressas e o vírus entra no estado de latência pós-integração: deixa de se replicar, mas seu DNA continua integrado, formando o reservatório de HIV. Caso essas células voltem a ser ativadas, ocorrerá a reativação da replicação do HIV e da sua infecção.[67]
Nos macrófagos, que também são células que não estão em divisão e são o segundo alvo principal do vírus, não ocorre o bloqueio da síntese e integração do provírus, sendo assim, estes não abrigam o HIV em latência pré-integração, mas podem abrigá-lo em latência pós-integração, na qual mesmo com o provírus não há formação de novas partículas virais.[67]
Variabilidade genética[editar | editar código-fonte]

O VIH difere de grande parte dos vírus na medida em que possui uma imensa variabilidade genética. Esta diversidade é resultado do seu rápido ciclo de replicação, capaz de gerar 1010 viriões por dia; de uma elevada taxa de mutação, de cerca de 3 x 10−5 por nucleobase por ciclo de replicação; e das propriedades recombinativas da transcriptase reversa.[68][69][70]
Este esquema complexo leva a que sejam produzidas diversas variantes de VIH por dia num paciente infetado com VIH.[68] Esta variabilidade é agravada quando uma célula é simultaneamente infetada por duas ou mais estirpes de VIH. Quando ocorre infeção em simultâneo, o genoma dos viriões progenitores pode ser constituído por fitas de ARN de duas estirpes diferentes. Este virião híbrido infeta depois uma nova célula, onde se replicará. Enquanto isto acontece, a transcriptase reversa, ao alternar entre dois padrões diferentes de ARN, vai gerar uma nova sequência de ADN retroviral que é uma recombinação entre os dois genomas progenitores.[68] Esta recombinação é mais óbvia quando ocorrer entre subtipos.[68]
O vírus da imunodeficiência símia (VIS) evoluiu para diversas estirpes, classificadas em função da espécie do hospedeiro natural. Pensa-se que as estirpes de VIS dos géneros Chlorocebus (VISagm) e Cercocebus atys (VISsmm) tenham tido uma longa história evolutiva em paralelo com os seus hospedeiros. Estes hospedeiros adaptaram-se à presença do vírus,[71] que está presente em grande quantidade no seu sangue mas espoleta apenas uma resposta imune moderada,[72] não provoca o aparecimento da SIDA símia,[73] e nem sofre as amplas mutações e recombinações típicas da infeção do VIH em seres humanos.[74]
Em contraste, quando estas estirpes infetam espécies que não estão adaptadas ao VIS, os animais desenvolvem SIDA e o vírus gera diversidade genética semelhante à que é observada na infeção humana com o VIH..[75] O SIV em chimpanzés (VIScpz), o parente genético mais próximo do VIH-1, está associado a maior mortalidade e sintomas semelhantes à SIDA no seu hospedeiro natural.[76] O VIScpz aparenta ter sido transmitido aos chimpanzés e à população humana há relativamente pouco tempo, pelo que os seus hospedeiros não estão ainda adaptados ao vírus.[71] Este vírus também perdeu a função do gene Nef que está presente na maior parte dos VIS; sem esta função, é mais provável que ocorra a diminuição dos linfócitos T, levando à imunodeficiência.[76]
Foram identificados três grupos de VIH-1 com base nas diferenças entre a região do envelope (env): M, N e O.[77] O grupo M é o mais prevalente e é subdividido em oito subtipos (ou clados) com base no genoma completo, que são distintos em termos geográficos.[78] Os mais prevalentes são os subtipos B (encontrados principalmente na Europa e América do Norte), A e D (encontrados principalmente em África), e C (encontrado principalmente em África e na Ásia). Estes subtipos formam ramos na árvore filogénica que representam a linhagem do grupo M do VIH-1. A co-infeção com diferentes subtipos suscita formas recombinantes circulantes (FRC ou, em inglês, CRF). Em 2000, o último ano em que foi feita uma análise da prevalência à escala global dos subtipos, 47,2% das infeções eram do subtipo C, 26,7% eram do subtipo A/CRF02_AG, 12,3% eram do subtipo B, 5,3% do subtipo D, 3,2% eram CRF_AE, e os restantes 5,3% eram constituídos por outros subtipos e formas recombinantes.[79] Grande parte da investigação relativa ao VIH-1 está focada no subtipo B e poucos laboratórios se focam nos restantes subtipos.[80] Tem sido colocada a hipótese de um outro grupo "P", com base num vírus isolado em 2009. A estirpe aparenta ser derivada do VIS do gorila (VISgor), isolada pela primeira vez em 2006.[81]
Diagnóstico[editar | editar código-fonte]
Muitos seropositivos desconhecem que estão infetados com o vírus. Por exemplo, em 2001, menos de 1% da população urbana sexualmente ativa em África tinha sido testada, sendo esta percentagem ainda menor entre a população rural. No mesmo ano, só 0,5% das mulheres grávidas que tiveram uma consulta em áreas urbanas foram aconselhadas, examinadas ou receberam os resultados dos testes e, igualmente, esta percentagem é inferior em áreas rurais.[82] Uma vez que os dadores de sangue podem não estar conscientes da sua infeção, o sangue doado é sistematicamente examinado em relação à presença de VIH.[83]
O teste de VIH-1 é inicialmente feito através de um exame ELISA, que deteta a presença de anticorpos do VIH-1. Indivíduos com resultado não reativo ao primeiro exame são considerados seronegativos, até que se verifique nova exposição a um parceiro infetado. Indivíduos com resultado positivo são novamente testados.[84] Se o resultado de ambos os testes é reativo, o indivíduo é classificado como duplamente reativo e submetido e exames de confirmação com testes complementares mais específicos (por exemplo, western blot ou, menos comum, imunofluorescência. Apenas os indivíduos que são duplamente reativos pelo ELISA e positivos por imunofluorescência ou reativos pelo western blot é que são considerados seropositivos e indicadores da presença de uma infeção com o VIH. Alguns indivíduos que são duplamente reativos ao ELISA, ocasionalmente têm resultados indeterminados com western blot, o que pode significar tanto uma resposta incompleta dos anticorpos ao VIH numa pessoa infetada, como reações não específicas numa pessoa não infetada.[85] Embora a imunofluorescência possa ser usada para confirmar a infeção nestes casos ambíguos, este ensaio não é amplamente usado. Regra geral, deve ser colhida uma segunda amostra mais de um mês depois da primeira, e novamente testadas as pessoas com resultados indeterminados de western blot. Embora seja muito menos comum, o exame com ácido nucleico pode auxiliar o diagnóstico em determinadas situações.[84]
Os exames de VIH modernos são extremamente precisos. Um único exame apresenta resultados corretos em mais de 99% dos casos.[86] Estima-se que a probabilidade da ocorrência de um resultado falso positivo no exame protocolar seja de apenas 1 em 250 000, numa população de baixo risco.[86] É recomendado que, após uma exposição ao VIH, os exames sejam feitos de imediato, a seis semanas, a três meses e a seis meses.[87]
Em 2017, dois pesquisadores da Stanford criaram uma centrífuga de papel que pode revolucionar como infecções como malária e HIV são detectadas nos países em desenvolvimento.[88]
Transmissão[editar | editar código-fonte]
| Forma de exposição | Chance de infecção | |||
|---|---|---|---|---|
| Transfusão de sangue | 90%[89] | |||
| Nascimento (para a criança) | 25%[90] | |||
| Partilha de seringas em drogas intravenosas |
0,67%[89] | |||
| Perfuração percutânea com agulha | 0,30%[91] | |||
| Sexo anal receptivo desprotegido | 0,04–3,0%[92] | |||
| Sexo anal insertivo desprotegido | 0,03%[93] | |||
| Sexo vaginal receptivo desprotegido | 0,05–0,30%[92][94] | |||
| Sexo vaginal insertivo desprotegido | 0,01–0,38%[92][94] | |||
| Sexo oral masculino receptivo desprotegido | 0–0,04%[92] | |||
| Sexo oral masculino insertivo desprotegido | 0–0,005%[95] | |||
| Observação: "desprotegido" significa que não é usado preservativo. | ||||
Estão identificadas três principais vias de transmissão do VIH: através de relações sexuais desprotegidas; por contacto sanguíneo, sobretudo através de feridas expostas, partilha de seringas ou transfusão de sangue que não tenha sido rastreado; e de mãe para filho durante a gravidez, parto ou amamentação. A infeção por VIH não proporciona imunidade adquirida, pelo que é possível ser infetado diversas vezes com estirpes diferentes do vírus.
Sexual[editar | editar código-fonte]
A maioria das infeções por VIH é adquirida através de relações sexuais desprotegidas. A transmissão por via sexual pode ocorrer quando as secreções sexuais infetadas de um dos parceiros entram em contacto com as membranas muscosas genitais, orais ou anais do outro. Em países desenvolvidos, o risco de transmissão da mulher para o homem é de 0,04% por ato, enquanto o risco da transmissão do homem para a mulher é de 0,08% por ato. Por várias razões, este risco é entre 4 a 10 vezes superior em países em desenvolvimento.[96]
A utilização correta e consistente de preservativos de látex reduz o risco de transmissão do VIH por via sexual em cerca de 85%..[97] No entanto, a utilização de espermicida é capaz de aumentar a probabilidade de contágio.[98][99][100]
Uma meta-análise de 27 estudos observacionais realizados até 1999 na África subsariana indicou que a circuncisão masculina reduz o risco de infeção por VIH.[101] No entanto, uma revisão posterior indicou que a correlação entre a circuncisão e o VIH nestes estudos observacionais pode ter sido devido a factores de confusão.[102] Além disso, foram levantadas preocupações relativas ao potencial de disseminação do VIH que as lâminas não esterilizadas constituem durante a circuncisão em rituais.[103] Foram posteriormente realizados outros ensaios, em África do Sul[104] no Quénia,[105] e no Uganda[106] nos quais homens não circuncidados eram aleatoriamente escolhidos para ser circuncidados em condições estéreis, e os resultados comparados contra um grupo não circuncidado, e que mostraram reduções na transmissão do VIH entre heterossexuais de 60%, 53% e 51%, respetivamente. Posteriormente, um painel de especialistas convocado pela OMS e pelo Secretariado da UNAIDS recomendou que a circuncisão masculina fosse reconhecida enquanto intervenção complementar na reduzir o risco de uma infeção de VIH adquirida por contacto sexual heterossexual.[107]
Sangue[editar | editar código-fonte]
Regra geral, há o risco de transmissão de VIH quando sangue infetado entra em contacto com qualquer ferida exposta. Esta via de transmissão é responsável por grande parte dos casos em pessoas que injetam drogas, hemofílicos e receptores de transfusões de sangue ou produtos derivados do sangue (embora nos países desenvolvidos as transfusões sejam despistadas para a presença de VIH). É também um motivo de preocupação em pessoas que recebam cuidados de saúde em regiões onde não sejam comuns as boas práticas de higiene no manuseio de equipamento de injeção, como a reutilização de agulhas em países sub-desenvolvidos. Indivíduos que realizem ou recebam tatuagem, piercings ou escarificações são também grupos de risco. Tem sido observado VIH em baixas concentrações em saliva, lágrimas e urina de indivíduos portadores; no entanto, não há qualquer caso registado de infeção através destas secreções e o risco potencial de transmissão é desprezível.[3] A transmissão de VIH através do mosquito não é possível.[108]
De mãe para filho[editar | editar código-fonte]
A transmissão do vírus de mãe para filho pode ocorrer durante a gravidez, no momento do parto ou através de amamentação. Na ausência de tratamento, a taxa de transmissão é de cerca de 25%. No entanto, caso estejam disponíveis tratamentos de combinação de antirretrovirais e a possibilidade de realizar uma cesariana, este risco pode ser reduzido para 1%.[90] A partilha da tarefa de amamentação entre mães deve ser evitada, já que é uma das causas de transmissão.[109]
Infeção múltipla e imunidade[editar | editar código-fonte]
Ao contrário de outros vírus, a infeção com VIH não proporciona imunidade contra novas infeções, sobretudo no caso de vírus geneticamente distantes. Têm sido relatados vários casos de infeções múltiplas inter- e intra-clado.[110] As múltiplas infeções têm sido ainda associadas a uma progressão mais rápida da doença.[111] As infeções múltiplas são divididas em duas categorias, dependendo do momento da aquisição da segunda estirpe. A "coinfeção" denomina duas estirpes que aparentam ter sido adquiridas em simultâneo, ou muito perto para se poder distinguir. A "reinfeção" ou "superinfeção" denomina a infeção com uma segunda estirpe num intervalo de tempo mensurável após a primeira. No caso do VIH, têm sido relatadas à escala global ambas as formas de infeção múltipla, tanto em infeções crónicas como agudas.[112][113][114][115]
Prevenção e tratamento[editar | editar código-fonte]

Não existe atualmente qualquer vacina ou cura para o VIH/SIDA. O único método de prevenção recomendado é evitar a exposição ao vírus. No entanto, acredita-se que um tratamento antirretrovírico denominado profilaxia pós-exposição (PPE) reduza o risco de infeção caso seja iniciado imediatamente após a exposição.[116] O tratamento atual para a infeção com VIH consiste numa terapêutica antirretrovírica de alta eficácia (em inglês, HAART), introduzida em 1996.[117][118] As opções terapêuticas atuais são compostas por três fármacos, pertencentes a pelo menos duas classes de agentes antirretrovirais. Regra geral, estas classes são dois nucleósidos inibidores da transcriptase reversa (NITR), associados a um não nucleósido inibidor da transcriptase reversa (NNITR) inibidor da protease (IP).[119] Uma vez que a progressão em crianças é mais rápida e menos previsível do que em adultos, são recomendados tratamentos mais agressivos.[120] Em países desenvolvidos nos quais esteja disponível a terapêutica HAART, o médico faz a avaliação completa do paciente, medindo a carga viral, a velocidade de declínio do CD4 e a capacidade de resposta do paciente, usando estes dados para decidir quando recomendar o início do tratamento.[121]
A terapêutica HAART permite a estabilização dos sintomas e da viremia, mas não cura o paciente nem alivia os sintomas. Uma vez interrompido o tratamento, os VIH-1 regressa aos níveis elevados anteriores.[122][123] Além disso, seria necessário um prazo superior a toda uma vida para eliminar a infeção recorrendo apenas à terapêutica HAART.[124] Apesar disso, muitos indivíduos infetados apresentam uma melhoria significativa em termos de saúde e qualidade de vida, o que tem proporcionado uma redução significativa da morbosidade e mortalidade associadas ao VIH em países desenvolvidos.[117][125][126] A esperança média de vida de um indivíduo infetado por HIV é de 32 anos a partir da data de infeção, caso o tratamento seja iniciado quando a contagem de CD4 for 350/µL.[127] Na ausência de terapêutica HAART, o tempo mediano para que uma infeção por VIH faça a progressão para SIDA é de cerca de nova a dez anos, enquanto que a estimativa mediana de sobrevivência depois de instalada a SIDA é de apenas 9,2 meses.[128] No entanto, a terapêutica HAART por vezes não atinge resultados satisfatórios, sendo em algumas circunstâncias ineficaz em mais de metade dos casos. Isto deve-se a várias razões, entra as quais intolerância ou efeitos secundários da medicação, terapêuticas antirretrovirais anteriores ineficazes, ou infeção com uma estirpe resistente de VIH. No entanto, a não adesão ou desistência por parte do paciente ao longo de uma terapia antirretroviral são a principal causa de insucesso da terapia HAART.[129] São várias as razões para a não adesão ou desistência da terapêutica HAART. A não adesão é motivada sobretudo pelo acesso deficiente a cuidados de saúde, apoios sociais inadequados, a presença de doenças psiquiátricas ou a toxicodependência. A desistência é motivada pela complexidade dos regimes HAART, em particular do número de comprimidos, da frequência das doses, da restrição alimentar ou ainda por outros motivos a par de efeitos secundários.[130][131][132] Os efeitos secundários incluem lipodistrofia, dislipidemia, resistência à insulina, aumento de riscos cardiovasculares e doenças congénitas.[133][134]

O momento preciso para iniciar o tratamento é ainda objeto de debate. É indiscutível que o tratamento deva ser iniciado antes da contagem de CD4 do paciente ser inferior a 200. A maior parte das recomendações nacionais indica que o tratamento deva ser iniciado mal a contagem seja inferior a 350, embora evidências de alguns estudos apontem para que seja iniciado ainda antes de ultrapassar os 350.[135][136] Em países onde não estão disponíveis métodos para contagem de CD4, o tratamento deve ser iniciado em pacientes nos estágios III e IV, conforme definido pela OMS.[137] Os fármacos antirretrovirais são dispendiosos, pelo que a maioria da população infetada a nível mundial não tem acesso ao tratamento de VIH/SIDA.[138] A investigação para melhorar os tratamentos atuais contempla a diminuição dos efeitos secundários, a simplificação dos regimes para diminuir a desistência, e a determinação da melhor sequência de regimes de modo a gerir a resistência aos fármacos. No entanto, pensa-se que apenas a vacinação será capaz de travar a pandemia global, já que se trata da única solução de baixo custo e que não requer tratamentos diários, sendo assim capaz de ser financeiramente sustentável em países em desenvolvimento.[138] No entanto, após mais de vinte anos de investigação, o VIH-1 continua a ser um candidato difícil para uma vacina.[138] Apesar disso, pensa-se que uma região da sua superfície constitua um potencial alvo para a criação uma vacina.[139]
Pesquisadores, em 2019, eliminaram o vírus HIV de animais vivos pela primeira vez,[140] usando uma estratégia de dois passos de acertar o vírus tanto com o CRISPR quanto com uma forma potente dos remédios normais. As moléculas do fármaco foram quimicamente ajustadas para torná-las solúveis em gordura, mas encapsuladas em uma gaiola molecular solúvel em água.[141] Isso significa que apenas uma injeção no sangue de um camundongo envia as drogas para as células do sistema imunológico, onde a molécula ativa é liberada lentamente com o tempo.[142] Em outras palavras, eles curaram os animais.[143]
Epidemiologia[editar | editar código-fonte]

A OMS e a UNAIDS estimam que a SIDA tenha sido responsável pela morte de mais de 25 milhões de pessoas desde que foi identificada em 1981, o que a torna numa das mais destrutivas pandemias na História desde que há registo. Apesar da melhoria no acesso a cuidados de saúde e a tratamentos antirretrovirais em muitas regiões do mundo, só em 2005 a SIDA provocou a morte estimada a 2,8 milhões de pessoas (entre 2,4 e 3,3 milhões), das quais mais de 570 000 eram crianças.[4]
Em 2007, estimava-se que viviam com o VIH entre 30,6 e 36,1 milhões de pessoas. Só nesse ano, estima-se que o vírus tenha sido o responsável direto pela morte de cerca de 2,1 milhões de pessoas, das quais 330 000 eram crianças, e que tenham ocorrido 2,5 milhões de novas infeções.[144]
A África subsariana é de longe a região mais afetada, na qual se estima que 21,6 a 27,4 milhões de pessoas vivam atualmente com o VIH. Dois milhões são crianças com idade inferior a quinze anos. Mais de 64% de todas as pessoas portadoras de VIH vivem na África subsariana, assim como mais de 75% de todas as mulheres portadoras do vírus. Em 2005 havia na região entre 10,6 e 13,6 milhões de órfãos em consequência da SIDA.[4] A África do Sul tem o maior número de casos de VIH no mundo, seguida pela Nigéria.[145] Nos 35 países com a maior prevalência de VIH, a esperança média de vida é de 48,3 anos, ou 6,5 anos a menos do que seria espectável sem a doença.[146]
A introdução da terapêutica HAART reduziu de forma substancial a mortalidade relacionada com o VIH nas áreas onde exista o acesso generalizado a cuidados de saúde. No entanto, à medida que aumentou a esperança de vida de portadores de VIH em países desenvolvidos, aumentaram também a probabilidade de disseminação da doença e, de forma substancial, o número de portadores vivos.[117]
Pesquisa[editar | editar código-fonte]
A pesquisa sobre o HIV/AIDS inclui todas as pesquisas médicas que tentam prevenir, tratar ou curar HIV/AIDS, bem como pesquisas fundamentais sobre a natureza do HIV como agente infeccioso e da AIDS como a doença causada pelo HIV. Muitos governos e instituições de pesquisa participam de investigações científicas sobre o tema. Esta pesquisa inclui intervenções de saúde comportamental, como pesquisas sobre educação sexual e desenvolvimento de medicamentos, como pesquisa de microbicidas para infeções sexualmente transmissíveis, vacinas contra o HIV e medicamentos antirretrovirais. Outras áreas de pesquisa médica incluem os tópicos de profilaxia pré-exposição, profilaxia pós-exposição, circuncisão e efeitos acelerados do envelhecimento.[147]
Após muitos anos de pesquisa, uma vacina contra o HIV não testada foi criada.[148] Os anticorpos bi-específicos que visam tanto a superfície das células T como os epítopos virais podem impedir a entrada do vírus em células somáticas.[149] Outro grupo utilizou a mesma tecnologia para desenvolver um anticorpo bi-específico que neutraliza as partículas virais através da reticulação de glicoproteínas de envelope.[150]
Ver também[editar | editar código-fonte]
Referências
- ↑ Weiss RA (maio de 1993). «How does HIV cause AIDS?». Science. 260 (5112): 1273–9. Bibcode:1993Sci...260.1273W. PMID 8493571. doi:10.1126/science.8493571
- ↑ Douek DC, Roederer M, Koup RA (2009). «Emerging Concepts in the Immunopathogenesis of AIDS». Annu. Rev. Med. 60: 471–84. PMC 2716400
 . PMID 18947296. doi:10.1146/annurev.med.60.041807.123549
. PMID 18947296. doi:10.1146/annurev.med.60.041807.123549
- ↑ a b Lifson AR (1988). «Do alternate modes for transmission of human immunodeficiency virus exist? A review». JAMA. 259 (9): 1353–6. PMID 2963151. doi:10.1001/jama.259.9.1353
- ↑ a b c UNAIDS (2006). «Overview of the global AIDS epidemic» (PDF). 2006 Report on the global AIDS epidemic. [S.l.: s.n.]
- ↑ Greener, R. (2002). «AIDS and macroeconomic impact». In: S, Forsyth (ed.). State of The Art: AIDS and Economics. [S.l.]: IAEN. pp. 49–55
- ↑ People living with HIV UNAIDS
- ↑ Two Strains of H.I.V. Cut Vastly Different Paths 3/3/2015 "The New York Times" (Uma versão deste artigo apareceu impressa em 10 de março de 2015, na página D3 da edição do New York Times, com a manchete: "Tracking a Killer Over Decades".)
- ↑ PMID 20598938 (20598938 &dopt=Abstract PubMed)
- ↑ Garg, H; Mohl, J; Joshi, A (9 de novembro de 2012). «HIV-1 induced bystander apoptosis.». Viruses. 4 (11): 3020–43. PMID 23202514
- ↑ Kumar, Vinay (2012). Robbins Basic Pathology 9th ed. [S.l.: s.n.] p. 147. ISBN 9781455737871
- ↑ Lawn SD (2004). «AIDS in Africa: the impact of coinfections on the pathogenesis of HIV-1 infection». J. Infect. Dis. 48 (1): 1–12. PMID 14667787. doi:10.1016/j.jinf.2003.09.001
- ↑ Buchbinder SP, Katz MH, Hessol NA, O'Malley PM, Holmberg SD. (1994). «Long-term HIV-1 infection without immunologic progression». AIDS. 8 (8): 1123–8. PMID 7986410. doi:10.1097/00002030-199408000-00014
- ↑ Trickey, Adam; Zhang, Lei; Sabin, Caroline A.; Sterne, Jonathan A. C. (1 de março de 2022). «Life expectancy of people with HIV on long-term antiretroviral therapy in Europe and North America: a cohort study». The Lancet Healthy Longevity (em inglês): S2. ISSN 2666-7568. doi:10.1016/S2666-7568(22)00063-0. Consultado em 10 de dezembro de 2022
- ↑ Bor, Jacob; Fischer, Charlie; Modi, Mirva; Richman, Bruce; Kinker, Cameron; King, Rachel; Calabrese, Sarah K.; Mokhele, Idah; Sineke, Tembeka (1 de dezembro de 2021). «Changing Knowledge and Attitudes Towards HIV Treatment-as-Prevention and "Undetectable = Untransmittable": A Systematic Review». AIDS and Behavior (em inglês) (12): 4209–4224. ISSN 1573-3254. PMC 8147591
 . PMID 34036459. doi:10.1007/s10461-021-03296-8. Consultado em 10 de dezembro de 2022
. PMID 34036459. doi:10.1007/s10461-021-03296-8. Consultado em 10 de dezembro de 2022
- ↑ Figueredo, Patricia Rocha de (19 de março de 2020). «I=I (indetectável=intransmissível): novos sentidos da infecção para quem vive com HIV/aids, novos desafios para a resposta à epidemia». doi:10.11606/d.5.2020.tde-09072020-131940. Consultado em 10 de dezembro de 2022
- ↑ International Committee on Taxonomy of Viruses (2002). «61.0.6. Lentivirus». National Institutes of Health. Consultado em 28 de fevereiro de 2006
- ↑ International Committee on Taxonomy of Viruses (2002). «61. Retroviridae». National Institutes of Health. Consultado em 28 de fevereiro de 2006
- ↑ Lévy, J. A. (1993). «HIV pathogenesis and long-term survival». AIDS. 7 (11): 1401–10. PMID 8280406. doi:10.1097/00002030-199311000-00001
- ↑ Smith JA, Daniel R (2006). «Following the path of the virus: the exploitation of host DNA repair mechanisms by retroviruses». ACS Chem Biol. 1 (4): 217–26. PMID 17163676. doi:10.1021/cb600131q
- ↑ Gilbert, PB; McKeague, IW; Eisen, G; Mullins, C; Guéye-Ndiaye, A; Mboup, S; Kanki, PJ (28 de fevereiro de 2003). «Comparison of HIV-1 and HIV-2 infectivity from a prospective cohort study in Senegal». Statistics in Medicine. 22 (4): 573–593. PMID 12590415. doi:10.1002/sim.1342
- ↑ Reeves JD, Doms RW (2002). «Human Immunodeficiency Virus Type 2». Journal of General Virology. 83 (Pt 6): 1253–65. PMID 12029140. doi:10.1099/vir.0.18253-0
- ↑ McGovern SL, Caselli E, Grigorieff N, Shoichet BK (2002). «A common mechanism underlying promiscuous inhibitors from virtual and high-throughput screening». Journal of Medical Chemistry. 45 (8): 1712–22. PMID 11931626. doi:10.1021/jm010533y
- ↑ Comparação: Fisher, Bruce; Harvey, Richard P.; Champe, Pamela C. (2007). Lippincott's Illustrated Reviews: Microbiology (Lippincott's Illustrated Reviews Series). Hagerstown, MD: Lippincott Williams & Wilkins. ISBN 0-7817-8215-5 Page 3
- ↑ Annenberg Learner (ed.). «The Structure and Life Cycle of HIV». Consultado em 15 de julho de 2017
- ↑ a b c d e f g Various (2008). HIV Sequence Compendium 2008 Introduction (PDF). [S.l.: s.n.] Consultado em 31 de março de 2009
- ↑ a b c Chan DC, Fass D, Berger JM, Kim PS (1997). «Core structure of gp41 from the HIV envelope glycoprotein» (PDF). Cell. 89 (2): 263–73. PMID 9108481. doi:10.1016/S0092-8674(00)80205-6. Consultado em 31 de março de 2009
- ↑ National Institute of Health (17 de junho de 1998). «Crystal structure of key HIV protein reveals new prevention, treatment targets» (Nota de imprensa). Consultado em 14 de setembro de 2006. Cópia arquivada em 19 de fevereiro de 2006
- ↑ Ouellet DL; Plante I; Landry P; et al. (abril de 2008). «Identification of functional microRNAs released through asymmetrical processing of HIV-1 TAR element». Nucleic Acids Res. 36 (7): 2353–65. PMC 2367715
 . PMID 18299284. doi:10.1093/nar/gkn076
. PMID 18299284. doi:10.1093/nar/gkn076
- ↑ Klase Z; Winograd R; Davis J; et al. (2009). «HIV-1 TAR miRNA protects against apoptosis by altering cellular gene expression». Retrovirology. 6 (1): 18. PMC 2654423
 . PMID 19220914. doi:10.1186/1742-4690-6-18
. PMID 19220914. doi:10.1186/1742-4690-6-18
- ↑ Garcia JV, Miller AD (abril de 1991). «Serine phosphorylation-independent downregulation of cell-surface CD4 by nef». Nature. 350 (6318): 508–11. Bibcode:1991Natur.350..508G. PMID 2014052. doi:10.1038/350508a0
- ↑ Schwartz O, Maréchal V, Le Gall S, Lemonnier F, Heard JM (março de 1996). «Endocytosis of major histocompatibility complex class I molecules is induced by the HIV-1 Nef protein». Nat. Med. 2 (3): 338–42. PMID 8612235. doi:10.1038/nm0396-338
- ↑ Stumptner-Cuvelette P; Morchoisne S; Dugast M; et al. (outubro de 2001). «HIV-1 Nef impairs MHC class II antigen presentation and surface expression». Proc. Natl. Acad. Sci. U.S.A. 98 (21): 12144–9. Bibcode:2001PNAS...9812144S. PMC 59782
 . PMID 11593029. doi:10.1073/pnas.221256498
. PMID 11593029. doi:10.1073/pnas.221256498
- ↑ a b c Coakley E, Petropoulos CJ, Whitcomb JM (2005). «Assessing ch vbgemokine co-receptor usage in HIV». Curr. Opin. Infect. Dis. 18 (1): 9–15. PMID 15647694. doi:10.1097/00001432-200502000-00003
- ↑ Deng H, Liu R, Ellmeier W, Choe S, Unutmaz D, Burkhart M, Di Marzio P, Marmon S, Sutton RE, Hill CM, Davis CB, Peiper SC, Schall TJ, Littman DR, Landau NR (1996). «Identification of a major co-receptor for primary isolates of HIV-1». Nature. 381 (6584): 661–6. Bibcode:1996Natur.381..661D. PMID 8649511. doi:10.1038/381661a0
- ↑ Feng Y, Broder CC, Kennedy PE, Berger EA (1996). «HIV-1 entry cofactor: functional cDNA cloning of a seven-transmembrane, G protein-coupled receptor». Science. 272 (5263): 872–7. Bibcode:1996Sci...272..872F. PMID 8629022. doi:10.1126/science.272.5263.872
- ↑ Knight SC, Macatonia SE, Patterson S (1990). «HIV I infection of dendritic cells». International Review of Immunology. 6 (2–3): 163–75. PMID 2152500. doi:10.3109/08830189009056627
- ↑ Tang J, Kaslow RA (2003). «The impact of host genetics on HIV infection and disease progression in the era of highly active antiretroviral therapy». AIDS. 17 (Suppl 4): S51–S60. PMID 15080180. doi:10.1097/00002030-200317004-00006
- ↑ Zhu T, Mo H, Wang N, Nam DS, Cao Y, Koup RA, Ho DD (1993). «Genotypic and phenotypic characterization of HIV-1 patients with primary infection». Science. 261 (5125): 1179–81. Bibcode:1993Sci...261.1179Z. PMID 8356453. doi:10.1126/science.8356453
- ↑ van’t Wout AB, Kootstra NA, Mulder-Kampinga GA, Albrecht-van Lent N, Scherpbier HJ, Veenstra J, Boer K, Coutinho RA, Miedema F, Schuitemaker H. (1994). «Macrophage-tropic variants initiate human immunodeficiency virus type 1 infection after sexual, parenteral, and vertical transmission». J Clin Invest. 94 (5): 2060–7. PMC 294642
 . PMID 7962552. doi:10.1172/JCI117560
. PMID 7962552. doi:10.1172/JCI117560
- ↑ Zhu T, Wang N, Carr A, Nam DS, Moor-Jankowski R, Cooper DA, Ho DD (1996). «Genetic characterization of human immunodeficiency virus type 1 in blood and genital secretions: evidence for viral compartmentalization and selection during sexual transmission». J Virol. 70 (5): 3098–107. PMC 190172
 . PMID 8627789
. PMID 8627789
- ↑ Muciaccia B, Padula F, Vicini E, Gandini L, Lenzi A, Stefanini M (2005). «Beta-chemokine receptors 5 and 3 are expressed on the head region of human spermatozoon». FASEB J. 19 (14): 2048–50. PMID 16174786. doi:10.1096/fj.05-3962fje
- ↑ Berlier W, Bourlet T, Lawrence P, Hamzeh H, Lambert C, Genin C, Verrier B, Dieu-Nosjean MC, Pozzetto B, Delezay O (2005). «Selective sequestration of X4 isolates by human genital epithelial cells: Implication for virus tropism selection process during sexual transmission of HIV». J Med Virol. 77 (4): 465–74. PMID 16254974. doi:10.1002/jmv.20478
- ↑ Clevestig P, Maljkovic I, Casper C, Carlenor E, Lindgren S, Naver L, Bohlin AB, Fenyo EM, Leitner T, Ehrnst A (2005). «The X4 phenotype of HIV type 1 evolves from R5 in two children of mothers, carrying X4, and is not linked to transmission». AIDS Res Hum Retroviruses. 5 (21): 371–8. PMID 15929699. doi:10.1089/aid.2005.21.371
- ↑ Moore JP (1997). «Coreceptors: implications for HIV pathogenesis and therapy». Science. 276 (5309): 51–2. PMID 9122710. doi:10.1126/science.276.5309.51
- ↑ Karlsson A, Parsmyr K, Aperia K, Sandstrom E, Fenyo EM, Albert J. (1994). «MT-2 cell tropism of human immunodeficiency virus type 1 isolates as a marker for response to treatment and development of drug resistance». J Infect Dis. 170 (6): 1367–75. PMID 7995974. doi:10.1093/infdis/170.6.1367
- ↑ Koot M, van 't Wout AB, Kootstra NA, de Goede RE, Tersmette M, Schuitemaker H. (1996). «Relation between changes in cellular load, evolution of viral phenotype, and the clonal composition of virus populations in the course of human immunodeficiency virus type 1 infection». J Infect Dis. 173 (2): 349–54. PMID 8568295. doi:10.1093/infdis/173.2.349
- ↑ Cheney K, McKnight A (2010). «HIV-2 Tropism and Disease». Lentiviruses and Macrophages: Molecular and Cellular Interactions. [S.l.]: Caister Academic Press. ISBN 978-1-904455-60-8
- ↑ a b c d e f g Chan D, Kim P (1998). «HIV entry and its inhibition». Cell. 93 (5): 681–4. PMID 9630213. doi:10.1016/S0092-8674(00)81430-0
- ↑ a b c d e f Wyatt R, Sodroski J (1998). «The HIV-1 envelope glycoproteins: fusogens, antigens, and immunogens». Science. 280 (5371): 1884–8. Bibcode:1998Sci...280.1884W. PMID 9632381. doi:10.1126/science.280.5371.1884
- ↑ Arthos J, Cicala C, Martinelli E, Macleod K, Van Ryk D, Wei D, Xiao Z, Veenstra TD, Conrad TP, Lempicki RA, McLaughlin S, Pascuccio M, Gopaul R, McNally J, Cruz CC, Censoplano N, Chung E, Reitano KN, Kottilil S, Goode DJ, Fauci AS (2008). «HIV-1 envelope protein binds to and signals through integrin alpha(4)beta(7), the gut mucosal homing receptor for peripheral T cells». Nature Immunology. In Press (3): 301–9. PMID 18264102. doi:10.1038/ni1566
- ↑ a b Pope M, Haase A (2003). «Transmission, acute HIV-1 infection and the quest for strategies to prevent infection». Nat Med. 9 (7): 847–52. PMID 12835704. doi:10.1038/nm0703-847
- ↑ Haedicke, Juliane; Craig (18 de agosto de 2009). «The brain-specific factor FEZ1 is a determinant of neuronal susceptibility to HIV-1 infection». Proceedings of the National Academy of Sciences (em inglês). 106 (33): 14040-14045. ISSN 0027-8424. PMID 19667186. doi:10.1073/pnas.0900502106
- ↑ a b c Zheng YH, Lovsin N, Peterlin BM (2005). «Newly identified host factors modulate HIV replication». Immunol. Lett. 97 (2): 225–34. PMID 15752562. doi:10.1016/j.imlet.2004.11.026
- ↑ «IV. VIRUSES - F. ANIMAL VIRUS LIFE CYCLES 3. The Life Cycle of HIV». Doc Kaiser's Microbiology Home Page. Community College of Baltimore County. Janeiro de 2008. Consultado em 18 de outubro de 2013. Arquivado do original em 26 de julho de 2010
- ↑ Hiscott J, Kwon H, Genin P (2001). «Hostile takeovers: viral appropriation of the NF-kB pathway». J Clin Invest. 107 (2): 143–151. PMC 199181
 . PMID 11160127. doi:10.1172/JCI11918
. PMID 11160127. doi:10.1172/JCI11918
- ↑ Pollard VW, Malim MH (1998). «The HIV-1 Rev protein». Annu. Rev. Microbiol. 52: 491–532. PMID 9891806. doi:10.1146/annurev.micro.52.1.491
- ↑ a b Hu WS, Temin HM. (1990). Retroviral recombination and reverse transcription. Science 250(4985):1227-1233. PMID 1700865
- ↑ a b Charpentier C, Nora T, Tenaillon O, Clavel F, Hance AJ. (2006). Extensive recombination among human immunodeficiency virus type 1 quasispecies makes an important contribution to viral diversity in individual patients. J Virol 80(5):2472-2482. PMID 16474154 Free PMC Article
- ↑ Nora T, Charpentier C, Tenaillon O, Hoede C, Clavel F, Hance AJ. (2007). Contribution of recombination to the evolution of human immunodeficiency viruses expressing resistance to antiretroviral treatment. J Virol 81(14):7620-7628. PMID 17494080 Free PMC Article
- ↑ Chen J, Powell D, Hu WS. (2006). High frequency of genetic recombination is a common feature of primate lentivirus replication. J Virol 80(19):9651-9658. PMID 16973569 Free PMC Article
- ↑ a b Bonhoeffer S, Chappey C, Parkin NT, Whitcomb JM, Petropoulos CJ. (2004). Evidence for positive epistasis in HIV-1. Science 2004 306(5701):1547-1550. Erratum in: Science. 2008 May 9;320(5877):746. PMID 15567861 Free Article
- ↑ Israël N, Gougerot-Pocidalo MA. (1997). Oxidative stress in human immunodeficiency virus infection. Cell Mol Life Sci 53(11-12):864-870. PMID 9447238
- ↑ Michod RE, Bernstein H, Nedelcu AM (2008). Adaptive value of sex in microbial pathogens. Infect Genet Evol 8(3):267-285. PMID 18295550 http://www.hummingbirds.arizona.edu/Faculty/Michod/Downloads/IGE%20review%20sex.pdf
- ↑ Hallenberger S, Bosch V, Angliker H, Shaw E, Klenk HD, Garten W (26 de novembro de 1992). «Inhibition of furin-mediated cleavage activation of HIV-1 glycoprotein gp160». Nature. 360 (6402): 358–61. Bibcode:1992Natur.360..358H. PMID 1360148. doi:10.1038/360358a0
- ↑ Gelderblom HR (1997). «Fine structure of HIV and SIV» (PDF). In: Los Alamos National Laboratory. HIV sequence compendium. [S.l.]: Los Alamos National Laboratory. pp. 31–44
- ↑ Nabel, G. & Baltimore, D. An inducible transcription factor activates expression of human immunodeficiency virus in T cells. Nature 326, 711-713 (1987).
- ↑ a b c Garcia-Blanco, M.A. & Cullen, B.R. Molecular basis of latency in pathogenic human viruses. Science 254, 815-820 (1991).
- ↑ a b c d Robertson DL, Hahn BH, Sharp PM. (1995). «Recombination in AIDS viruses». J Mol Evol. 40 (3): 249–59. PMID 7723052. doi:10.1007/BF00163230
- ↑ Rambaut, A; Posada, D; Crandall, KA; Holmes, EC (janeiro de 2004). «The causes and consequences of HIV evolution». Nature Reviews Genetics. 5 (52–61): 52–61. PMID 14708016. doi:10.1038/nrg1246
- ↑ Perelson AS, Ribeiro RM (outubro de 2008). «Estimating drug efficacy and viral dynamic parameters: HIV and HCV». Stat Med. 27 (23): 4647–57. PMID 17960579. doi:10.1002/sim.3116
- ↑ a b PMID 19661993 (PubMed)
- ↑ Holzammer S, Holznagel E, Kaul A, Kurth R, Norley S (2001). «High virus loads in naturally and experimentally SIVagm-infected African green monkeys». Virology. 283 (2): 324–31. PMID 11336557. doi:10.1006/viro.2001.0870
- ↑ Kurth, R. and Norley, S. (1996). «Why don't the natural hosts of SIV develop simian AIDS?». J. NIH Res. 8: 33–37
- ↑ Baier M, Dittmar MT, Cichutek K, Kurth R (1991). «Development of vivo of genetic variability of simian immunodeficiency virus». Proc. Natl. Acad. Sci. U.S.A. 88 (18): 8126–30. Bibcode:1991PNAS...88.8126B. PMC 52459
 . PMID 1896460. doi:10.1073/pnas.88.18.8126
. PMID 1896460. doi:10.1073/pnas.88.18.8126
- ↑ Daniel MD, King NW, Letvin NL, Hunt RD, Sehgal PK, Desrosiers RC (1984). «A new type D retrovirus isolated from macaques with an immunodeficiency syndrome». Science. 223 (4636): 602–5. Bibcode:1984Sci...223..602D. PMID 6695172. doi:10.1126/science.6695172
- ↑ a b PMID 19626114 (PubMed)
- ↑ Thomson MM, Perez-Alvarez L, Najera R (2002). «Molecular epidemiology of HIV-1 genetic forms and its significance for vaccine development and therapy». Lancet Infectious Diseases. 2 (8): 461–471. PMID 12150845. doi:10.1016/S1473-3099(02)00343-2
- ↑ Carr JK, Foley BT, Leitner T, Salminen M, Korber B, McCutchan F (1998). «Reference sequences representing the principal genetic diversity of HIV-1 in the pandemic» (PDF). In: Los Alamos National Laboratory (ed.). HIV sequence compendium. Los Alamos, New Mexico: Los Alamos National Laboratory. pp. 10–19
- ↑ Osmanov S, Pattou C, Walker N, Schwardlander B, Esparza J; WHO-UNAIDS Network for HIV Isolation and Characterization (2002). «Estimated global distribution and regional spread of HIV-1 genetic subtypes in the year 2000». Acquired Immune Deficiency Syndrome. 29 (2): 184–190. PMID 11832690
- ↑ Perrin L, Kaiser L, Yerly S. (2003). «Travel and the spread of HIV-1 genetic variants». Lancet Infect Dis. 3 (1): 22–27. PMID 12505029. doi:10.1016/S1473-3099(03)00484-5
- ↑ Plantier JC; Leoz M; Dickerson JE; et al. (agosto de 2009). «A new human immunodeficiency virus derived from gorillas». Nature Medicine. 15 (8): 871–2. PMID 19648927. doi:10.1038/nm.2016. Resumo divulgativo
- ↑ Kumaranayake L, Watts C (2001). «Resource allocation and priority setting of HIV/AIDS interventions: addressing the generalized epidemic in sub-Saharan Africa». Journal of International Development. 13 (4): 451–466. doi:10.1002/jid.797
- ↑ Kleinman S (Setembro de 2004). «Patient information: Blood donation and transfusion». Consultado em 29 de maio de 2019. Cópia arquivada em 12 de abril de 2008
- ↑ a b Centers for Disease Control and Prevention (2001). «Revised guidelines for HIV counseling, testing, and referral». MMWR Recomm Rep. 50 (RR–19): 1–57. PMID 11718472
- ↑ Celum CL, Coombs RW, Lafferty W, Inui TS, Louie PH, Gates CA, McCreedy BJ, Egan R, Grove T, Alexander S, et al. (1991). «Indeterminate human immunodeficiency virus type 1 western blots: seroconversion risk, specificity of supplemental tests, and an algorithm for evaluation». J Infect Dis. 164 (4): 656–664. PMID 1894929. doi:10.1093/infdis/164.4.656
- ↑ a b Chou R, Huffman LH, Fu R, Smits AK, Korthuis PT (julho de 2005). «Screening for HIV: a review of the evidence for the U.S. Preventive Services Task Force». Annals of Internal Medicine. 143 (1): 55–73. PMID 15998755
- ↑ Tolle MA, Schwarzwald HL (15 de julho de 2010). «Postexposure prophylaxis against human immunodeficiency virus». American Family Physician. 82 (2): 161–6. PMID 20642270
- ↑ This low-cost paper centrifuge may one day save countless lives Used to detect various blood infections, the 'paperfuge' can be made for less than 20 cents. por Michael D'Estries, publicado em Nature (2017)
- ↑ a b Smith DK, Grohskopf LA, Black RJ, Auerbach JD, Veronese F, Struble KA, Cheever L, Johnson M, Paxton LA, Onorato IM, Greenberg AE (21 de janeiro de 2005). «Antiretroviral postexposure prophylaxis after sexual, injection-drug use, or other nonoccupational exposure to HIV in the United States: recommendations from the U.S. Department of Health and Human Services.». MMWR. Recommendations and reports : Morbidity and mortality weekly report. Recommendations and reports / Centers for Disease Control. 54 (RR-2): 1–20. PMID 15660015
- ↑ a b Coovadia H (2004). «Antiretroviral agents—how best to protect infants from HIV and save their mothers from AIDS». N. Engl. J. Med. 351 (3): 289–292. PMID 15247337. doi:10.1056/NEJMe048128
- ↑ Kripke C (1 de agosto de 2007). «Antiretroviral prophylaxis for occupational exposure to HIV.». American family physician. 76 (3): 375–6. PMID 17708137
- ↑ a b c d Dosekun O, Fox J (Julho de 2010). «An overview of the relative risks of different sexual behaviours on HIV transmission.». Current Opinion in HIV and AIDS. 5 (4): 291–7. PMID 20543603. doi:10.1097/COH.0b013e32833a88a3
- ↑ Cunha, Burke (2012). Antibiotic Essentials 2012 11 ed. [S.l.]: Jones & Bartlett Publishers. 303 páginas. ISBN 9781449693831
- ↑ a b Boily MC, Baggaley RF, Wang L, Masse B, White RG, Hayes RJ, Alary M (Fevereiro de 2009). «Heterosexual risk of HIV-1 infection per sexual act: systematic review and meta-analysis of observational studies.». The Lancet infectious diseases. 9 (2): 118–29. PMID 19179227. doi:10.1016/S1473-3099(09)70021-0
- ↑ Baggaley RF, White RG, Boily MC (Dezembro de 2008). «Systematic review of orogenital HIV-1 transmission probabilities.». International Journal of Epidemiology. 37 (6): 1255–65. PMC 2638872
 . PMID 18664564. doi:10.1093/ije/dyn151
. PMID 18664564. doi:10.1093/ije/dyn151
- ↑ Boily M-C; Baggaley RF; , Wang L; et al. (2009). «Heterosexual risk of HIV-1 infection per sexual act: systematic review and meta-analysis of observational studies». Lancet Infect Dis. 9 (2): 118-129. PMID 19179227. doi:10.1016/S1473-3099(09)70021-0
- ↑ National Institute of Allergy and Infectious Diseases (20 de julho de 2001). Workshop Summary: Scientific Evidence on Condom Effectiveness for Sexually Transmitted Disease (STD) Prevention (PDF). National Institutes of Health, Department of Health and Human Services. Hyatt Dulles Airport, Herndon, Virginia. pp. 13–15. Consultado em 8 de janeiro de 2009
- ↑ «Should spermicides be used with condoms?». Condoms and Sexually Transmitted Diseases, Brochure. United States Food and Drug Administration. 30 de abril de 2009. Consultado em 23 de julho de 2009
- ↑ Global Campaign for Microbicides : Rectal Use of N-9 checked 2009-07-22
- ↑ Nonoxynol-9 Spermicide on HIV Risk List checked 2009-07-22
- ↑ Weiss, H.A.; M.A. Quigley; R.J. Hayes (2000). «Male circumcision and risk of HIV infection in sub-Saharan Africa: A systematic review and meta-analysis». AIDS. 14 (15): 2361–70. PMID 11089625. doi:10.1097/00002030-200010200-00018
- ↑ Siegfried, N., Muller, M., Deeks, J., Volmink, J., Egger, M., Low, N., Walker, S. and Williamson, P. (2005). «HIV and male circumcision--a systematic review with assessment of the quality of studies». Lancet Infect. Dis. 5 (3): 165–73. PMID 15766651
- ↑ Various (2005). «Repeated Use of Unsterilized Blades in Ritual Circumcision Might Contribute to HIV Spread in S. Africa, Doctors Say». Kaisernetwork.org. Consultado em 28 de março de 2006. Arquivado do original em 28 de setembro de 2006
- ↑ Williams BG, Lloyd-Smith JO, Gouws E, Hankins C, Getz WM, Hargrove J, de Zoysa I, Dye C, Auvert B. (2006). «The Potential Impact of Male Circumcision on HIV in Sub-Saharan Africa.». PLoS Med. 3 (7): e262. PMID 16822094. doi:10.1371/journal.pmed.0030262
- ↑ Bailey RC; Moses S; Parker CB; et al. (2007). «Male circumcision for HIV prevention in young men in Kisumu, Kenya: a randomised controlled trial». Lancet. 369 (9562): 643–56. PMID 17321310. doi:10.1016/S0140-6736(07)60312-2
- ↑ Gray RH; et al. (24 de fevereiro de 2007). «Male circumcision for HIV prevention in men in Rakai, Uganda: a randomised trial». Lancet. 369 (9562): 657–66. PMID 17321311. doi:10.1016/S0140-6736(07)60313-4
- ↑ WHO (2007). «WHO and UNAIDS announce recommendations from expert consultation on male circumcision for HIV prevention». WHO.int. Consultado em 13 de julho de 2007
- ↑ «Cópia arquivada». Consultado em 20 de outubro de 2013. Arquivado do original em 29 de março de 2014
- ↑ Cochrane Systematic Review on interventions for prevention of late postnatal mother-to-child transmission of HIV http://www.cochrane.org/reviews/en/ab006734.html
- ↑ Smith D, Richman D, Little S (2005). «HIV Superinfection». Journal of Infectious Diseases. 192: 438–44. PMID 15995957. doi:10.1086/431682
- ↑ Gottlieb; et al. (2004). «Dual HIV-1 infection associated with rapid disease progression». Lancet. 363 (9049): 619–22. PMID 14987889. doi:10.1016/S0140-6736(04)15596-7
- ↑ Smith; et al. (2004). «Incidence of HIV superinfection following primary infection». JAMA. 292 (10): 1177–8. PMID 15353529. doi:10.1001/jama.292.10.1177
- ↑ Chohan B, Lavreys L, Rainwater SM, Overbaugh J (agosto de 2005). «Evidence for frequent reinfection with human immunodeficiency virus type 1 of a different subtype». J. Virol. 79 (16): 10701–8. PMC 1182664
 . PMID 16051862. doi:10.1128/JVI.79.16.10701-10708.2005
. PMID 16051862. doi:10.1128/JVI.79.16.10701-10708.2005
- ↑ Piantadosi A, Chohan B, Chohan V, McClelland RS, Overbaugh J (novembro de 2007). «Chronic HIV-1 infection frequently fails to protect against superinfection». PLoS Pathog. 3 (11): e177. PMC 2077901
 . PMID 18020705. doi:10.1371/journal.ppat.0030177
. PMID 18020705. doi:10.1371/journal.ppat.0030177
- ↑ Hu DJ; Subbarao S; Vanichseni S; et al. (fevereiro de 2005). «Frequency of HIV-1 dual subtype infections, including intersubtype superinfections, among injection drug users in Bangkok, Thailand». AIDS. 19 (3): 303–8. PMID 15718841. Consultado em 31 de março de 2009
- ↑ Fan, H., Conner, R. F. and Villarreal, L. P. eds, ed. (2005). AIDS : science and society 4th ed. Boston, MA: Jones and Bartlett Publishers. ISBN 0-7637-0086-X
- ↑ a b c Palella, F. J., Delaney, K. M., Moorman, A. C., Loveless, M. O., Fuhrer, J., Satten, G. A., Aschman, D. J. and Holmberg, S. D. (1998). «Declining morbidity and mortality among patients with advanced human immunodeficiency virus infection». N. Engl. J. Med. 338 (13): 853–860. PMID 9516219. doi:10.1056/NEJM199803263381301
- ↑ Department of Health and Human Services (janeiro de 2005). «A Pocket Guide to Adult HIV/AIDS Treatment January 2005 edition». Consultado em 17 de janeiro de 2006. Arquivado do original em 23 de dezembro de 2005
- ↑ Coordenação Nacional para a Infecção VIH/sida. «Recomendações Portuguesas para o Tratamento da Infecção VIH/sida» (PDF). Consultado em 18 de outubro de 2013
- ↑ Department of Health and Human Services Working Group on Antiretroviral Therapy and Medical Management of HIV-Infected Children (3 de novembro de 2005). «Guidelines for the Use of Antiretroviral Agents in Pediatric HIV Infection» (PDF). Consultado em 17 de janeiro de 2006. Arquivado do original (PDF) em 15 de maio de 2012
- ↑ Department of Health and Human Services Panel on Clinical Practices for Treatment of HIV Infection (2005). «Guidelines for the Use of Antiretroviral Agents in HIV-1-Infected Adults and Adolescents» (PDF). Consultado em 17 de janeiro de 2006
- ↑ Martinez-Picado, J., DePasquale, M. P., Kartsonis, N., Hanna, G. J., Wong, J., Finzi, D., Rosenberg, E., Gunthard, H. F., Sutton, L., Savara, A., Petropoulos, C. J., Hellmann, N., Walker, B. D., Richman, D. D., Siliciano, R. and D'Aquila, R. T. (2000). «Antiretroviral resistance during successful therapy of human immunodeficiency virus type 1 infection». Proc. Natl. Acad. Sci. U. S. A. 97 (20): 10948-10953. PMID 11005867
- ↑ Dybul, M., Fauci, A. S., Bartlett, J. G., Kaplan, J. E., Pau, A. K.; Panel on Clinical Practices for Treatment of HIV. (2002). «Guidelines for using antiretroviral agents among HIV-infected adults and adolescents». Ann. Intern. Med. 137 (5 Pt 2): 381-433. PMID 12617573
- ↑ Blankson, J. N., Persaud, D., Siliciano, R. F. (2002). «The challenge of viral reservoirs in HIV-1 infection». Annu. Rev. Med. 53: 557-593. PMID 11818490
- ↑ Wood, E., Hogg, R. S., Yip, B., Harrigan, P. R., O'Shaughnessy, M. V. and Montaner, J. S. (2003). «Is there a baseline CD4 cell count that precludes a survival response to modern antiretroviral therapy?». AIDS. 17 (5): 711-720. PMID 12646794
- ↑ Chene, G., Sterne, J. A., May, M., Costagliola, D., Ledergerber, B., Phillips, A. N., Dabis, F., Lundgren, J., D'Arminio Monforte, A., de Wolf, F., Hogg, R., Reiss, P., Justice, A., Leport, C., Staszewski, S., Gill, J., Fatkenheuer, G., Egger, M. E. and the Antiretroviral Therapy Cohort Collaboration. (2003). «Prognostic importance of initial response in HIV-1 infected patients starting potent antiretroviral therapy: analysis of prospective studies». Lancet. 362 (9385): 679-686. PMID 12957089
- ↑ Schackman BR, Gebo KA, Walensky RP, Losina E, Muccio T, Sax PE, Weinstein MC, Seage GR 3rd, Moore RD, Freedberg KA. (2006). «The lifetime cost of current HIV care in the United States». Med Care. 44 (11): 990-997. PMID 17063130
- ↑ Morgan D, Mahe C, Mayanja B, Okongo JM, Lubega R, Whitworth JA (2002). «HIV-1 infection in rural Africa: is there a difference in median time to AIDS and survival compared with that in industrialized countries?». AIDS. 16 (4): 597–632. PMID 11873003
- ↑ Becker SL, Dezii CM, Burtcel B, Kawabata H, Hodder S. (2002). «Young HIV-infected adults are at greater risk for medication nonadherence». MedGenMed. 4 (3). 21 páginas. PMID 12466764
- ↑ Nieuwkerk, P., Sprangers, M., Burger, D., Hoetelmans, R. M., Hugen, P. W., Danner, S. A., van Der Ende, M. E., Schneider, M. M., Schrey, G., Meenhorst, P. L., Sprenger, H. G., Kauffmann, R. H., Jambroes, M., Chesney, M. A., de Wolf, F., Lange, J. M. and the ATHENA Project. (2001). «Limited Patient Adherence to Highly Active Antiretroviral Therapy for HIV-1 Infection in an Observational Cohort Study». Arch. Intern. Med. 161 (16): 1962-1968. PMID 11525698
- ↑ Kleeberger, C., Phair, J., Strathdee, S., Detels, R., Kingsley, L. and Jacobson, L. P. (2001). «Determinants of Heterogeneous Adherence to HIV-Antiretroviral Therapies in the Multicenter AIDS Cohort Study». J. Acquir. Immune Defic. Syndr. 26 (1): 82-92. PMID 11176272
- ↑ Heath, K. V., Singer, J., O'Shaughnessy, M. V., Montaner, J. S. and Hogg, R. S. (2002). «Intentional Nonadherence Due to Adverse Symptoms Associated With Antiretroviral Therapy». J. Acquir. Immune Defic. Syndr. 31 (2): 211-217. PMID 12394800
- ↑ Montessori, V., Press, N., Harris, M., Akagi, L., Montaner, J. S. (2004). «Adverse effects of antiretroviral therapy for HIV infection.». CMAJ. 170 (2): 229-238. PMID 14734438
- ↑ Saitoh, A., Hull, A. D., Franklin, P. and Spector, S. A. (2005). «Myelomeningocele in an infant with intrauterine exposure to efavirenz». J. Perinatol. 25 (8): 555-556. PMID 16047034
- ↑ Wood E, HoggRS, Harrigan PR, Montaner JS. (2005). «When to initial antiretroviral therapy in HIV-1-infected adults: a review for clinicians and patients». Lancet Infect. Dis. 5: 407-414
- ↑ Wang C; Vlahov D; Galai N; et al. (2004). «Mortality in HIV-seropositive versus seronegative persons in the era of highly active antiretroviral therapy.». J. Infect. Dis. 190: 1046–54. PMID 15319852
- ↑ Organização Mundial de Saúde (2006). «WHO case definitions of HIV for surveillance and revised clinical staging and immunological classification» (PDF). Consultado em 27 de dezembro de 2006
- ↑ a b c Ferrantelli F, Cafaro A, Ensoli B. (2004). «Nonstructural HIV proteins as targets for prophylactic or therapeutic vaccines». Curr Opin Biotechnol. 15 (6): 543-556. PMID 15560981
- ↑ BBC News (2007). «Scientists expose HIV weak spot». Consultado em 20 de abril de 2007
- ↑ «Researchers use CRISPR to eliminate HIV in mice». STAT (em inglês). 2 de julho de 2019. Consultado em 2 de julho de 2019
- ↑ «For the First Time, Researchers Eliminate HIV From the Genomes of Living Animals». Time (em inglês). Consultado em 2 de julho de 2019
- ↑ Wilson, Clare. «Have mice really been cured of HIV using CRISPR gene editing?». New Scientist (em inglês). Consultado em 2 de julho de 2019
- ↑ «CRISPR and LASER ART Eliminate HIV from Mice». GEN - Genetic Engineering and Biotechnology News (em inglês). 2 de julho de 2019. Consultado em 2 de julho de 2019
- ↑ UNAIDS, Organização Mundial de Saúde (Dezembro de 2007). «2007 AIDS epidemic update» (PDF). Consultado em 12 de março de 2008
- ↑ McNeil, Jr., Donald (20 de novembro de 2007). «U.N. Agency to Say It Overstated Extent of H.I.V. Cases by Millions». The New York Times. Consultado em 16 de janeiro de 2008
- ↑ UNAIDS (2001). «Special Session of the General Assembly on HIV/AIDS Round table 3 Socio-economic impact of the epidemic and the strengthening of national capacities to combat HIV/AIDS» (PDF). Consultado em 15 de junho de 2006
- ↑ FDA-Approved HIV Medicines | Understanding HIV/AIDS | AIDSinfo
- ↑ Bernstein, Ryan Lenora Brown, Lenny. «New HIV vaccine trial, the first in years, to begin». chicagotribune.com. Consultado em 28 de novembro de 2016
- ↑ Huang Y, Yu J, Lanzi A, Yao X, Andrews C, Tsai L, Gajjar M, Sun M, Seaman M, Padte N, Ho D (2016). «Engineered Bispecific Antibodies with Exquisite HIV-1-Neutralizing Activity». Cell. 165 (7): 1621–1631. PMC 4972332
 . PMID 27315479. doi:10.1016/j.cell.2016.05.024
. PMID 27315479. doi:10.1016/j.cell.2016.05.024
- ↑ Bournazos, S., Gazumyan, A., Seaman, M., Nussenzweig, M. and Ravetch, J. (2016). Bispecific Anti-HIV-1 Antibodies with Enhanced Breadth and Potency.
Bibliografia[editar | editar código-fonte]
- Berlier W, Bourlet T, Lawrence P, Hamzeh H, Lambert C, Genin C, Verrier B, Dieu-Nosjean MC, Pozzetto B, Delézay O (2005). «Selective sequestration of X4 isolates by human genital epithelial cells: Implication for virus tropism selection process during sexual transmission of HIV». J Med Virol. 77 (4): 465–74. PMID 16254974. doi:10.1002/jmv.20478
- Joint United Nations Programme on HIV/AIDS (UNAIDS) (2011). Global HIV/AIDS Response, Epidemic update and health sector progress towards universal access (PDF). [S.l.]: Joint United Nations Programme on HIV/AIDS
- Muciaccia B, Padula F, Vicini E, Gandini L, Lenzi A, Stefanini M (2005). «Beta-chemokine receptors 5 and 3 are expressed on the head region of human spermatozoon». FASEB J. 19 (14): 2048–50. PMID 16174786. doi:10.1096/fj.05-3962fje
Ligações externas[editar | editar código-fonte]
- «Portal português de referência na temática do VIH/SIDA»
- «RNP+ Rede Nacional de Pessoas vivendo com HIV/Aids» (em português e inglês)
- «Associação Brasileira Interdisciplinar de AIDS»

