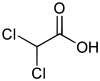
Ácido dicloroacético
Ácido dicloroacético, frequentemente abreviado DCA, é um composto químico, um ácido, e um análogo do ácido acético no qual dois dos três átomos de hidrogênios do grupo metila foram substituídos por átomos de cloro. O sal e ésteres do ácido dicloroacético são chamados dicloroacetatos. Os sais estão sob investigação como um possível tratamento para o câncer.
Química e ocorrência[editar | editar código-fonte]
A química do ácido dicloroacético é típica dos ácidos orgânicos halogenados. É um membro da família dos ácidos cloroacéticos. O íon dicloroacetato é produzido quando dissolvido em água. Como um ácido com uma pKa de 1.48,[4] o ácido dicloroacético puro é muito corrosivo e extremamente destrutivo das membranas mucosas e trato respiratório superior.[5]
O DCA não ocorre na natureza. Ele é produto da cloração de água e é produzido pelo metabolismo de várias drogas ou produtos químicos diversos contendo cloro.[6] Ele é tipicamente preparado pela redução do ácido tricloroacético.
Uso terapêutico[editar | editar código-fonte]
Devido à ação altamente corrosiva deste ácido, somente os sais de ácido dicloroacético são usados terapeuticamente, incluindo seus sais de sódio e potássio - dicloroacetato de sódio e dicloroacetato de potássio.
Acidose láctica[editar | editar código-fonte]
O íon dicloroacetato estimula a atividade da enzima piruvato desidrogenase, por inibição da enzima piruvato desidrogenase quinase.[7]
Assim, o DCA diminui a produção de lactato, substituindo o metabolismo do piruvato - de fermentação para oxidação na mitocôndria. Essa propriedade levou a experimentos com o DCA no tratamento de acidose láctica em humanos.[8][9][10][11]
Um estudo publicado em 1998 concluiu que, embora o uso do DCA em adultos com acidose láctica tivesse baixado os níveis de lactato sanguíneo, não houve benefícios clínicos, nem melhora da hemodinâmica ou aumento da sobrevivência dos pacientes.[11]
Um experimento aleatório controlado realizado em 2006 com crianças portadoras de acidose láctica congênita concluiu que, embora o DCA tivesse sido bem tolerado, seu uso também não resultou em melhoras clínicas.[9]
Um outro artigo, também de 2006, publicou o resultado de um estudo sobre o uso do DCA no tratamento de MELAS (Miopatia mitocondrial com encefalopatia, acidose lática e episódios tipo AVC), uma síndrome causada pelo inadequado funcionamento das mitocôndrias, o que leva à acidose láctica. O estudo duplo-cego e randomizado foi desenvolvido ao longo de três anos, com 30 pacientes de 10 a 60 anos de idade, portadores de MELAS e mutação mitocondrial A3243G. Ministrou-se DCA (25 mg/kg/dia) a um grupo e placebo ao grupo de controle. Porém o experimento foi interrompido porque todas as 15 crianças que receberam DCA desenvolveram significativa toxidade nos nervos, sem qualquer evidência de benefício decorrente da medicação.[10]
Assim, embora relatos de casos e dados pré-clínicos sugiram que o ácido dicloroacético possa ser eficaz contra a acidose láctica, avaliações controladas subsequentes não mostraram benefícios clínicos da substância. Além disso, os indivíduos que participaram dos experimentos não puderam continuar a receber doses de DCA, em razão da toxidade progressiva da substância.
Potenciais aplicações em tratamento de câncer[editar | editar código-fonte]
Células cancerosas geralmente usam glicólise em vez de respiração (fosforilação oxidativa) para obter energia (efeito Warburg), devido à hipoxia que existe nos tumores e também em mitocôndrias danificadas.[12] Usualmente, células perigosamente danificadas matam a si próprias via apoptose - um mecanismo de autodestruição que envolve a mitocôndria. Mas esse mecanismo falha em células cancerosas. De acordo com a hipótese Warburg de crescimento canceroso, o câncer é causado por mudanças metabólicas nas mitocôndrias, embora agora se saiba que o câncer é causado também por mutações no genoma das células.
Um estudo publicado em janeiro de 2007, por pesquisadores da Universidade de Alberta,[13] que testaram o DCA em linhagens de células cancerosas in vitro, tendo um rato como modelo, revelou que o DCA restaurou a função das mitocôndrias, restaurando, portanto, a apoptose e matando as células cancerosas in vitro - reduzindo portanto os tumores nos ratos.[14]
Esses resultados receberam grande atenção da mídia, a partir de um artigo publicado na New Scientist intitulado "Cheap, 'safe' drug kills most cancers" ("Droga barata e 'segura' mata a maioria dos cânceres").[15] Em seguida, a Sociedade Americana do Câncer e outras organizações médicas receberam inúmeras manifestações de interesse público e questões sobre o DCA.[16] Desde então, as análises indicaram que, embora os resultados do estudo fossem promissores, nenhuma experiência clínica em humanos com câncer fora realizada, enfatizando-se a necessidade de cautela na interpretação dos resultados preliminares.[16][17] No entanto, alguns médicos, "informalmente", já estavam tratando seus pacientes com o DCA,[18][19] sob uma nuvem de controvérsia.[18] Medicor Cancer Centres, uma clínica privada em Toronto, gerida por pelos Drs. Humaira e Akbar Khan, estava desde março de 2007[20] usando o DCA informalmente para o tratamento de vários cânceres. Eles declararam, em seu sítio web, que alguns pacientes "estão mostrando várias respostas positivas ao DCA, incluindo diminuição do tumor, redução dos marcadores de tumor, controle de sintomas e melhoras em testes de laboratórios".[19] No entanto, eles não publicaram esses resultados nem os apresentaram em conferências médicas. O Dr. Terry Polevoy, de Kitchener, Ontario, evocou o Colégio de Médicos e Cirurgiões de Ontario para remover a licença médica dos Khans por oferecer um composto cujo efeito de reduzir tumores em humanos não havia sido aprovado. "Eles não são oncologistas. Não deveriam estar tomando essas decisões. Acho que eles deveriam ser disciplinados por usar essa substância. Isso, para mim, não é ético, usar algo que nunca foi provado que funciona." Mas o Colégio disse que não era o papel dele dizer quais terapias um médico pode usar.[21]
A revista New Scientist mais tarde escreveu no seu editorial, "A droga pode ainda cumprir sua promessa como um agente anticâncer – o início de experiências clínicas é esperadao em breve. Ela pode até mesmo vir a criar uma classe inteiramente nova de drogas anticâncer. Por enquanto, todavia, permanece experimental, ainda não apropriadamente testada em uma pessoa com câncer. Pessoas que se auto-administram a droga estão fazendo uma grande aposta mas, por incrível que possa parecer, elas podem até mesmo piorar sua saúde."[22]
Mais de 90% das drogas que estão entrando nos testes da fase I são consideradas inaceitáveis.[23] O FDA aprova 8% a 11% das drogas que estão entrando em testes da fase I.[24][25] O DCA tem sido usado historicamente para tratar pacientes com acidose lática, e portanto poderia entrar diretamente em experiências da fase 2, envolvendo pacientes com câncer.[26]
O DCA não é patenteável como um composto. No entanto, o processo de patenteamento do seu uso no tratamento de câncer foi então iniciado.[27] A pesquisa do Dr. Evangelos Michelakis não recebeu nenhum suporte da indústria farmacêutica. Sem uma forte proteção de patente, o incentivo financeiro para a indústria farmacêutica se reduz, e portanto experiências clínicas do DCA podem não ocorrer por falta de financiamento.[15][16][17][28][29]
No entanto, outras fontes de financiamento existem. Estudos anteriores do DCA receberam fundos de organizações governamentais, tais como o NIH, o FDA, o CIHR e por organizações privadas sem fins lucrativos, como o MDA). Antecipando os desafios financeiros, o laboratório do Dr. Michelaki passou a solicitar diretamente doações online, para financiar a sua pesquisa.[30] Depois de 6 meses, seu laboratório levantou mais de US$ 800 000,00, o suficiente para financiar um pequeno estudo clínico da fase 2. O Dr. Michelakis e o Dr. Archer iniciaram um processo de patente para o uso do DCA no tratamento do câncer.[31][32]
Em 24 de setembro de 2007, o Departamento de Medicina da Universidade de Alberta anunciou que depois que o financiamento do teste clínico foi assegurado, tanto o comitê local de ética de Alberta como o Ministério da Saúde do Canadá (Health Canada) aprovaram o primeiro teste clínico do DCA no tratamento de câncer.[33] Previa-se que esse experimento inicial fosse feito com um grupo relativamente pequeno (até 50 pacientes nos 18 meses seguintes). Os pacientes seriam originários da área de Edmonton e estariam disponíveis para análises ao longo da duração dos testes. O experimento foi completado em agosto de 2009.[34] Em maio de 2010, a equipe publicou um comunicado à imprensa[35] declarando que os resultados do experimento não haviam sido conclusivos. Foi também publicado um artigo, no qual foram descritos os resultados[36] Somente cinco pacientes haviam sido tratados com a droga durante o experimento.
Em maio de de 2011, relatórios online[37] sugeriram que o grupo de Alberta havia comunicado novos dados que a mídia "não tinha publicado". Entretanto, isso aparentemente foi causado por uma confusão de datas (a atualização anterior fora feita em maio de 2010)[38]) e as instituições de combate ao câncer rapidamente desmentiram esses rumores,[39][40] que foram posteriormente tratados na revista New Scientist.[41]
Atualmente, o uso da substância como agente anticancerígeno já foi patenteado.[42]
Efeitos colaterais[editar | editar código-fonte]
Relatos publicados pela imprensa leiga após o anúncio da Universidade de Alberta de 2007 afirmam que o dicloroacetato "tem sido utilizado realmente com segurança em seres humanos há décadas".[43] O DCA é geralmente bem tolerado, mesmo em crianças.[44] Em períodos curtos, a infusão de bolus de DCA a 50 mg/kg/dia tem sido bem tolerada.[45]
Neuropatia[editar | editar código-fonte]
Um experimento clínico, no qual fora ministrado DCA a pacientes de MELAS a 25 mg/kg/dia, foi interrompido em razão da excessiva toxicidade dos nervos periféricos.[10] O dicloroacetato também pode ter efeito ansiolítico ou sedativo.[6] Estudos em animais sugerem que a neuropatia e a neurotoxicidade durante o tratamento crônico com dicloroacetato pode ser parcialmente devida à depleção de tiamina. Um suplemento de tiamina em ratos reduziu esses efeitos.[46] Entretanto, estudos mais recentes em humanos sugerem que a neuropatia periférica é um efeito colateral comum durante o tratamento com DCA, mesmo com a administração simultânea de tiamina por via oral.[47][48] Segundo o relatório de um experimento adicional, o tratamento com 50 mg/kg/dia de DCA causou irregularidade na marcha e letargia em dois pacientes, sendo que os sintomas ocorreram após um mês para um paciente e após dois meses para o outro. Os distúrbios da marcha e da consciência foram resolvidos interrompendo-se a administração do DCA; no entanto o potencial de ação dos nervos sensoriais não se recuperou durante um mês.[49]
Foi relatado que animais e pacientes tratados com DCA apresentaram mais elevados níveis de ácido delta-aminolevulínico (delta-ALA) na urina. Estudo publicado em 2008 sugere que o DCA pode ser a causa de efeitos colaterais neurotóxicos, em razão do bloqueio da formação da mielina periférica.[50]
Referências
- ↑ a b c d e Registo de Dichloressigsäure na Base de Dados de Substâncias GESTIS do IFA, accessado em 9 de Dezembro de 2007
- ↑ Stoffdaten bei chemexper.com
- ↑ a b AMA Archives of Industrial Hygiene and Occupational Medicine. Vol. 4, Pg. 119, 1951.
- ↑ Lide, D. R. (Ed.) (1990). CRC Handbook of Chemistry and Physics (70th Edn.). Boca Raton (FL):CRC Press.
- ↑ «MSDS (jtbaker)». Consultado em 19 de dezembro de 2007. Arquivado do original em 21 de fevereiro de 2009
- ↑ a b Stacpoole P, Henderson G, Yan Z, James M (1998). «Clinical pharmacology and toxicology of dichloroacetate». Environ Health Perspect. 106 Suppl 4: 989–94. PMID 9703483 Free full text Arquivado em 27 de setembro de 2007, no Wayback Machine.
- ↑ Stacpoole P (1989). «The pharmacology of dichloroacetate». Metabolism. 38 (11): 1124-44. PMID 2554095
- ↑ Stacpoole P, Lorenz A, Thomas R, Harman E (1988). «Dichloroacetate in the treatment of lactic acidosis». Ann Intern Med. 108 (1): 58-63. PMID 3337517
- ↑ a b Stacpoole P, Kerr D, Barnes C, Bunch S, Carney P, Fennell E, Felitsyn N, Gilmore R, Greer M, Henderson G, Hutson A, Neiberger R, O'Brien R, Perkins L, Quisling R, Shroads A, Shuster J, Silverstein J, Theriaque D, Valenstein E (2006). «Controlled clinical trial of dichloroacetate for treatment of congenital lactic acidosis in children». Pediatrics. 117 (5): 1519-31. PMID 16651305
- ↑ a b c Kaufmann P, Engelstad K, Wei Y, Jhung S, Sano M, Shungu D, Millar W, Hong X, Gooch C, Mao X, Pascual J, Hirano M, Stacpoole P, DiMauro S, De Vivo D (2006). «Dichloroacetate causes toxic neuropathy in MELAS: a randomized, controlled clinical trial». Neurology. 66 (3): 324-30. PMID 16476929
- ↑ a b Stacpoole P, Wright E, Baumgartner T, Bersin R, Buchalter S, Curry S, Duncan C, Harman E, Henderson G, Jenkinson S (1992). «A controlled clinical trial of dichloroacetate for treatment of lactic acidosis in adults. The Dichloroacetate-Lactic Acidosis Study Group». N Engl J Med. 327 (22): 1564-9. PMID 1435883
- ↑ Xu R, Pelicano H, Zhou Y, Carew J, Feng L, Bhalla K, Keating M, Huang P (2005). «Inhibition of glycolysis in cancer cells: a novel strategy to overcome drug resistance associated with mitochondrial respiratory defect and hypoxia». Cancer Res. 65 (2): 613–21. PMID 15695406
- ↑ «depmed.ualberta.ca». Consultado em 19 de dezembro de 2007. Arquivado do original em 23 de outubro de 2008
- ↑ Bonnet S, Archer S, Allalunis-Turner J, Haromy A, Beaulieu C, Thompson R, Lee C, Lopaschuk G, Puttagunta L, Bonnet S, Harry G, Hashimoto K, Porter C, Andrade M, Thebaud B, Michelakis E (2007). «A mitochondria-K+ channel axis is suppressed in cancer and its normalization promotes apoptosis and inhibits cancer growth». Cancer Cell. 11 (1): 37–51. PMID 17222789. doi:10.1016/j.ccr.2006.10.020
- ↑ a b «Cheap, 'safe' drug kills most cancers». New Scientist. 17 de janeiro de 2007. Consultado em 17 de janeiro de 2007
- ↑ a b c «"DCA: Cancer Breakthrough or Urban Legend?"». Consultado em 1 de agosto de 2008. Arquivado do original em 9 de junho de 2008 ABC News, 5 de fevereiro de 2007.
- ↑ a b «"No Wonder Drug"» letter to New Scientist from Ralph Moss Lemont. Published February 3 2007. Accessed 16 February 2007.
- ↑ a b http://www.nationalreviewofmedicine.com/issue/poll/featured_article.html
- ↑ a b Medicor Cancer Centres – DCA Therapy
- ↑ http://www.medicorcancer.com/NatPost-may28_2007.pdf
- ↑ «Doctors prescribe DCA to cancer patients». Consultado em 8 de outubro de 2007
- ↑ «"Editorial: Gambling with your life"» New Scientist, 31 de março de 2007.
- ↑ «Society for Clinical Trials Board of Directors.» The Society for Clinical Trials opposes US legislation to permit marketing of unproven medical therapies for seriously ill patients. Clin Trials 2006;3:154. [Texto integral]
- ↑ Food&Drug Packaging, agosto de 2004
- ↑ Nature Reviews Drug Development, agosto de 2004
- ↑ «A Letter from Dr. Evangelos Michelakis». Consultado em 19 de dezembro de 2007. Arquivado do original em 23 de outubro de 2008
- ↑ «CTV.ca | Researchers launch website on new cancer research». Consultado em 8 de outubro de 2007
- ↑ «"Small molecule offers big hope against cancer"». Consultado em 1 de agosto de 2008. Arquivado do original em 27 de fevereiro de 2007 by Ryan Smith.ExpressNews. University of Alberta. 16 de janeiro de 2007.
- ↑ «Cura del Cáncer: ¿Bloqueada por las farmacéuticas? (Entrevista con el Nobel de Medicina Richard J. Roberts)» Vanguardia, 25 de maio de 2011.
- ↑ «Official University of Alberta DCA Site». Consultado em 19 de dezembro de 2007. Arquivado do original em 23 de outubro de 2008
- ↑ «Researchers launch website on new cancer research» CTV.ca, 22 de janeiro de 2007.
- ↑ «A Method of Treating Cancer Using Dichloroacetate» Application to the European Patent Office, 19 October 2006
- ↑ «DCA Update: Health Canada Approves First DCA Clinical Trial in Cancer» (PDF). Consultado em 1 de agosto de 2008. Arquivado do original (PDF) em 20 de setembro de 2008 24 de setembro de 2007.
- ↑ «The Safety and Efficacy of DCA for the Treatment of Brain Cancer» ClinicalTrials.gov identifier: NCT00540176
- ↑ «Outlook 2008». Consultado em 20 de julho de 2013. Arquivado do original em 15 de fevereiro de 2013 Tufts Center for the Study of Drug Development
- ↑ Michelakis, ED; Sutendra, G; Dromparis, P; Webster, L; Haromy, A; Niven, E; Maguire, C; Gammer, TL; MacKey, JR (2010). «Metabolic modulation of glioblastoma with dichloroacetate». Science translational medicine. 2 (31): 31ra34–31ra34. PMID 20463368. doi:10.1126/scitranslmed.3000677
- ↑ «The Cure for Cancer Has Been Found and is Purposely Being Ignored» - Technorati blog
- ↑ «DCA Research Team publishes results of Clinical Trials». Consultado em 20 de julho de 2013. Arquivado do original em 15 de fevereiro de 2013 - University of Alberta website
- ↑ «Potential cancer drug DCA tested in early trials» Cancer Research UK science blog
- ↑ «@CR_UK tweet» - tweeted 16/05/11
- ↑ «Cancer drug resurfaces and threatens false optimism» New Scientist, 16 de maio de 2011.
- ↑ US 8071645, Newell, M. Karen; Newell, Evan & Villalobos-Menuey, Elizabeth, "Systems and methods for treating human inflammatory and proliferative diseases and wounds, with fatty acid metabolism inhibitors and/or glycolytic inhibitors"
- ↑ Picard, André (17 de janeiro de 2007). «Long-used drug shows new promise for cancer». Toronto: The Globe and Mail. Consultado em 17 de janeiro de 2007
- ↑ Pearson H; Kurtz, TL; Han, Z; Langaee, T (2008). «Role of dichloroacetate in the treatment of genetic mitochondrial diseases». Adv Drug Deliv Rev. 60 (13,14): 1478–1487. PMID 18647626. doi:10.1016/j.addr.2008.02.014
- ↑ Agbenyega T, Planche T, Bedu-Addo G, Ansong D, Owusu-Ofori A, Bhattaram VA, Nagaraja NV, Shroads AL, Henderson GN, Hutson AD, Derendorf H, Krishna S, Stacpoole PW (2003). «Population kinetics, efficacy, and safety of dichloroacetate for lactic acidosis due to severe malaria in children». J Clin Pharmacol. 43 (4): 386–396. PMID 12723459. doi:10.1177/0091270003251392
- ↑ Stacpoole P, Harwood H, Cameron D, Curry S, Samuelson D, Cornwell P, Sauberlich H (1990). «Chronic toxicity of dichloroacetate: possible relation to thiamine deficiency in rats». Fundam Appl Toxicol. 14 (2): 327–37. PMID 2318357. doi:10.1016/0272-0590(90)90212-3
- ↑ Kurlemann G, Paetzke I, Moller H, Masur H, Schuierer G, Weglage J, Koch HG (1995). «Therapy of complex I deficiency: peripheral neuropathy during dichloroacetate therapy». Eur J Pediatr. 154 (11): 928–32. PMID 8582409. doi:10.1007/BF01957508
- ↑ Spruijt L, Naviaux RK, McGowan KA, Nyhan WL, Sheean G, Haas RH, Barshop BA (2001). «Nerve conduction changes in patients with mitochondrial diseases treated with dichloroacetate». Muscle Nerve. 24 (7): 916–24. PMID 11410919. doi:10.1002/mus.1089
- ↑ Oishi K, Yoshioka M, Ozawa R, Yamamoto T, Oya Y, Ogawa M, Kawai M (2003). «Dichloroacetate treatment for adult patients with mitochondrial disease». Rinsho Shinkeigaku. 43 (4): 154–61. PMID 12892050
- ↑ Felitsyn, N; McLeod, C; Shroads, AL; Stacpoole, PW; Notterpek, L (2008). «The heme precursor delta-aminolevulinate blocks peripheral myelin formation». Journal of Neurochemistry. 106 (5): 2068–2079. PMC 2574579
 . PMID 18665889. doi:10.1111/j.1471-4159.2008.05552.x
. PMID 18665889. doi:10.1111/j.1471-4159.2008.05552.x
Ligações externas[editar | editar código-fonte]
- CTV.ca News Staff (16 de janeiro de 2007). «Small molecule offers hope for cancer treatment». CTV.ca Website (em inglês). CTV television network. Consultado em 31 de janeiro de 2007
- Evangelos Michelakis and Stephen Archer (22 de janeiro de 2007). «Researchers launch website on new cancer research». CTV.ca Website (em inglês). CTV television network. Consultado em 31 de janeiro de 2007
- DCA Reseach Information Website (University of Alberta and the Alberta Cancer Board)
- Metabolic Targeting as an Anticancer Strategy: Dawn of a New Era? PDF of a scientific paper by researchers from the University of Toronto, Canada
- Wait for Clinical Trials, New Scientist, 24 de fevereiro de 2007
- Questions over DCA 'cancer drug', by Cancer Research UK
- Dichloroacetate, Huntington's disease, and metabolic disorders
- Cancer Biology - Cramping Tumors Economist, 18 de janeiro de 2007.
- The DCA Site