Óxido de vanádio(III)
Aspeto
| Óxido de vanádio(III) Alerta sobre risco à saúde | |
|---|---|
| |
| Outros nomes | Sesquióxido de vanádio, Óxido vanádico |
| Identificadores | |
| Número CAS | |
| PubChem | |
| Número RTECS | YW3050000 |
| Propriedades | |
| Fórmula molecular | V2O3 |
| Massa molar | 149.881 g/mol |
| Aparência | Black powder |
| Densidade | 4.87 g/cm3 |
| Ponto de fusão |
1940 °C, 2213 K, 3524 °F |
| Solubilidade em other solvents | Insoluble |
| Estrutura | |
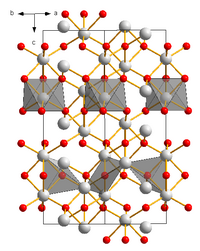
| Estrutura cristalina | Trigonal (karelianite), hR30 |
| Grupo de espaço | R-3c h, No. 167 |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Óxido de vanádio(III) é um composto inorgânico de fórmula química V2O3. É um sólido escuro preparado pala redução do V2O5 com hidrogênio ou monóxido de carbono.[1][2] Reage com ácidos em água para formar complexos de vanádio(III).[2] V2O3 possui a estrutura do corundum.[2] É um composto antiferromagnético com temperatura crítica em 160 K.[3] A esta temperatura há uma mudança abrupta na condutividade de metálico para a forma isolante.[3]
Exposto ao ar, converte-se gradualmente em V2O4, de coloração azul-índigo.[3]
Na natureza, ocorre como um mineral bastante raro denominado karelianite - grafia inglesa.
Referências
- ↑ Handbook of Preparative Inorganic Chemistry, 2nd Ed.
- ↑ a b c Verevkin, A.; Pearlman, A.; Slstrokysz, W.; Zhang, J.; Currie, M.; Korneev, A.; Chulkova, G.; Okunev, O.; Kouminov, P.; Smirnov, K.; Voronov, B.; N. Gol'tsman, G.; Sobolewski, Roman (2004). "Ultrafast superconducting single-photon detectors for near-infrared-wavelength quantum communications". Journal of Modern Optics 51 (12): 1447–1458. doi:10.1080/09500340410001670866.
- ↑ a b c E.M. Page, S.A.Wass (1994),Vanadium:Inorganic and Coordination chemistry, Encyclopedia of Inorganic Chemistry, John Wiley & Sons, ISBN 0-471-93620-0
