Adição eletrofílica
As referências deste artigo necessitam de formatação. (Junho de 2022) |
Em química orgânica, uma adição eletrofílica ou eletrófila ( ou ) é uma reação de adição onde em um composto químico, o substrato da reação, se perde um ligação pi para permitir a formação de duas novas ligações sigma. Nas reações de adição eletrofílica, os substratos mais comuns tem ligações duplas ou ligações triplas carbono-carbono.[1]
Eletrófilos são ácidos de Lewis, moléculas ou íons que pode aceitar um par de elétrons. Qualquer reação de um eletrófilo também envolve um nucleófilo. Na protonação de um alceno, eletrófilo é o próton doado por um ácido, e o nucleófilo é o alceno. Estão inclusos reagentes positivos, tais como prótons, reagentes neutros, tais como bromo, e os ácidos de Lewis e .[2]
Adição via radicais livres por HBr[editar | editar código-fonte]
A adição de brometo de hidrogênio a alcenos antigamente era algo imprevisível, pois a adição ocorria de acordo com a regra de Markovnikov, mas outras vezes, ela ocorria de modo contrário. Em 1929, Morris S. Kharasch concluiu, após vários experimentos, que reações de adição envolvendo peróxido, ou seja, composto orgânico do tipo ROOR, não seguia a regra de Markovnikov. Assim Kharasch propôs que o brometo de hidrogênio pode adicionar-se a alcenos por dois mecanismos diferentes: Adição eletrofílica e adição seguindo a regra anti- Markovnikov. Iremos focar na adição anti- Markovnikov, pois essa é uma reação em cadeia que envolve intermediários radicais livres, portanto, é o que nos interessa.
Adição anti- Markovnikov:
Vamos nos basear na Adição via radicais livres de brometo de hidrogênio, observe o quadro abaixo:

Etapa 1: os peróxidos iniciam o processo agindo como fonte de radicais livres necessários para a reação em cadeia começar. A ligação oxigênio-oxigênio é relativamente fraca, assim a adição via radicais livres do brometo de hidrogênio a alcenos começa com a produção de dois alcoxi, que vieram da quebra do peróxido.
Etapa 2: um desses radicais alcoxila retira um átomo hidrogênio do brometo de hidrogênio gerando assim um átomo de bromo. Com isso, dá inicio a fase de propagação da reação em cadeia.
Etapa 3 e 4: um átomo de bromo adiciona-se ao alceno na direção que produz o radical alquila mais estável. O radical mais estável seguirá a ordem de estabilidade (terciário > secundário > primário). Assim, o radical mais estável é formado mais rapidamente. O átomo de bromo se adiciona a ligação dupla. Posteriormente o radical alquila retira um átomo hidrogênio do brometo de hidrogênio originando então o produto brometo de alquila mostrado na Etapa 4. As etapas 3 e 4 são etapas de propagação, na qual o 1-bromobutano é o produto principal.
Entre os haletos de hidrogênio somente o brometo de hidrogênio reage com alcenos pelos dois mecanismos: adição eletrofílica e via radicais livres. Em geral, o HBr reage por adição eletrofílica, mas se houver peróxido ou a reação for iniciada fotoquimicamente, é seguido o mecanismo de radical livre.[3]
Para as sínteses orgânicas, a possibilidade de ter dois caminhos diferentes para um brometo de hidrogênio e um alceno é uma vantagem, já que de um único alceno pode-se preparar um de dois diferentes brometos de alquila, através da escolha da reação mais favorável.[4]
Formação de hidrogenossulfatos de alquila (via H2SO4)[editar | editar código-fonte]
Essa reação ocorre quando ácidos diferentes de haletos de hidrogênio se adicionam à ligação carbono-carbono de alcenos. Nesse caso, quando os alcenos são tratados com ácido sulfúrico concentrado a frio, eles reagem por meio de adição eletrofílica para formar hidrogenossulfatos de aquila.
- A Reação global
- Mecanismo
Inicialmente o alceno aceita um próton do ácido sulfúrico. Essa reação segue a regra de Markovnikov, então o próton se ligará ao carbono mais hidrogenado para formar o carbocátion mais estável.
Em seguida o ânion hidrogenossulfato reage com o carbocátion formando o hidrogenossulfato de alquila. Como se trata de uma reação regiosseletiva, temos a formação do isopropil-hidrogenossulfato ao invés do propil hidrogenossulfato.
Os hidrogenossulfatos de alquila podem sofrer hidrólise e serem convertidos a álcoois quando aquecidos com água, como mostrado a seguir:
Hidratação de alcenos por catálise ácida[editar | editar código-fonte]
Nesta reação, um alceno reage com a água originando um álcool.
A regiosseletividade da hidratação segue a regra de Markovnikov, que determina que o hidrogênio seja ligado ao carbono menos substituído (com o maior número de hidrogênios).[3] Embora possa ser utilizado ácido concentrado, esta reação ocorre em meio ácido diluído, utilizando-se geralmente uma solução 50% água/ácido sulfúrico, que permite a produção direta do álcool sem a necessidade de uma etapa adicional de hidrólise.[4]
Na hidratação ácida todas as etapas do processo são reversíveis. O próton age apenas como catalisador e não é consumido na reação geral.[5] Apesar de particularmente apropriado para reações industriais em larga escala, esse processo torna-se de pouco valor em escala laboratorial por exigir condições fortemente ácidas e alta temperatura (250ºC no caso do etileno).[6]
Mecanismo[editar | editar código-fonte]
Na primeira etapa do mecanismo de reação, a ligação pi reage com um próton, formando o carbocátion mais estável.[7]Este carbocátion é planar e pode reagir com uma molécula de água pela face superior ou inferior – esta etapa não é estereosseletiva. A água age como um nucleófilo para capturar o cátion terc-butila. A última etapa envolve a perda de um próton pelo íon oxônio resultante da adição de água.
Epoxidação de alcenos[editar | editar código-fonte]
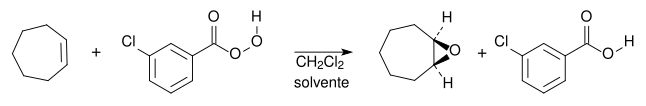
Os alcenos podem ser oxidados no tratamento com um peroácido ( , também conhecido como ácido peroxicarboxílico).[6] O grupo hidroxila () em peroácidos contém um oxigênio eletrofílico, que pode reagir com alcenos adicionando este oxigênio à ligação pi formando um epóxido (também chamado de oxirana).[5] A essa reação dá-se o nome de epoxidação. Um epóxido é um éter cíclico com um átomo de oxigênio em um anel de três membros. O outro produto da reação é um ácido carboxílico:
Mecanismo[editar | editar código-fonte]
A transferência do oxigênio é de estereoquimicamente sin, sendo a estereoquímica do alceno inicial mantida no produto – as duas ligações se formam na mesma face da ligação dupla por meio de um mecanismo de etapa única sem intermediários. O átomo de hidrogênio mais distante do grupo carbonila é aquele que é transferido.[6] Na epoxidação, pode-se descrever um estado transicional cíclico no qual o oxigênio eletrofílico é adicionado à ligação pi ao mesmo tempo que o próton do peroácido é transferido para seu próprio grupo carbonila, liberando uma molécula de ácido carboxílico, que é um bom grupo de saída. As duas novas ligações no epóxido formado são formalmente derivadas dos pares de elétron da ligação pi do alceno e da ligação clivada.[5]
Referências
- ↑ March, Jerry; (1985). Advanced Organic Chemistry reactions, mechanisms and structure (3rd ed.). New York: John Wiley & Sons, inc. ISBN 0-471-85472-7
- ↑ Adição Eletrofílica
- ↑ a b «Adição Eletrofílica a Alcenos Haletos de Hidrogênio (HX)» (PDF). Consultado em 17 de agosto de 2014. Arquivado do original (PDF) em 19 de agosto de 2014
- ↑ a b Carey, Francis A. (2008). Química Orgânica - Vol. 1. São Paulo: McGraw-Hill. ISBN 978-0-07-304787-7 Verifique
|isbn=(ajuda) templatestyles stripmarker character in|autor=at position 1 (ajuda) - ↑ a b c Vollhardt, K.; Peter, C. (2011). Organic chemistry : structure and function. Nova Iorque: W. H. Freeman and Company. ISBN 978-1-4292-0494-1 templatestyles stripmarker character in
|autor=at position 1 (ajuda) - ↑ a b c McMurry, John. (2011). Química Orgânica - Volume 1. São Paulo: Cengage Learning. ISBN 978-85-221-1008-7 templatestyles stripmarker character in
|autor=at position 1 (ajuda) - ↑ Parrill, Abby. «Acid Catalyzed Hydration». Consultado em 8 de agosto de 2013 templatestyles stripmarker character in
|autor=at position 1 (ajuda)
Bibliografia[editar | editar código-fonte]
- Solomons, T. W. Graham. "Organic chemistry"; Jonh Wiley & Sons, Inc; 6th ed.;1996;ISBN 0-471-01342-0
- Carey, Francis A.. Química Orgânica - Vol. 1. São Paulo: McGraw-Hill, 2008. ISBN 978-0-07-304787-7