Lipossoma
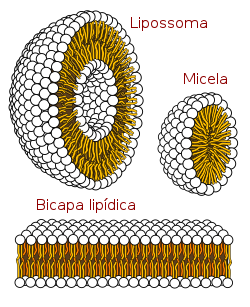
Lipossomas são pequenas vesículas formadas por pelo menos uma bicamada concêntricas de fosfolipídios que se organizam espontaneamente em meio aquoso ou por ultra-sons em meio aquoso em que o componente da solução usada (íons, moléculas) pode preencher a cavidade do interior do lipossoma. Tais estruturas chamaram a atenção dos pesquisadores como um sistema de entrega promissor devido à sua biocompatibilidade, biodegradabilidade, baixa toxicidade, fácil preparação, tempo de circulação prolongado, e a capacidade de prolongar a vida útil dos produtos.[1]
Devido a essas características, os lipossomas são consideradas uma excelente forma de liberação controlada de medicamentos ou substâncias biologicamente ativas devido a sua flexibilidade estrutural seja no tamanho, composição e fluidez da bicamada lipídica, como na sua capacidade de incorporar uma variedade de compostos tanto hidrofílicos como hidrofóbicos.
Histórico[editar | editar código-fonte]
Os lipossomas foram descobertos no início da década de 60, através de estudos da hidratação de filmes lipídicos depositados nas paredes de um frasco de vidro. Tal experimento foi realizado pelo Dr. Alec Bangham, mas quem primeiro utilizou o termo lipossoma (corpo gorduroso), para designar as estruturas vesiculares formadas por bicamadas fosfolipídicas com um compartimento aquoso em seu interior, foi Weissman em 1965.
Classificação[editar | editar código-fonte]
Os lipossomas podem ser classificados tanto com relação ao seu tamanho e número de lamelas quanto a sua interação com o meio biológico. De acordo com os diametros médios em três categorias:
- Vesículas Multilamelares (MLV – Multilamelar Vesicles): formas lipossomais formadas por bicamadas fosfolipídicas concêntricas intercaladas por compartimentos aquosos, cujo diâmetro varia de 400 a 3500 nm.
- Vesículas unilamelares grandes (LUV – Large Unilamelar vesicles): formas lipossomais constituídas por apenas uma bicamada fosfolipídica, mas com uma grande cavidade aquosa. Diâmetro varia de 200 a 1000 nm.
- Vesículas unilamelares pequenas (SUV – Small Unilamelar Vesicles): formas lipossomais constituídas por apenas uma bicamada fosfolipídica e um pequeno compartimento aquoso. Diâmetro varia de 20 a 50 nm (Scarpa et al.,1998).
De acordo com a carga, lipossomas podem ser classificados como catiônicos (carga positiva), aniônicos (carga negativa) e neutros (sem carga). Lipossomas catiônicos são os mais frequentemente utilizados na terapia gênica humana, pois o DNA possui uma carga efetiva negativa.
Quando comparado a vetores virais, os lipossomas apresentam muitas vantagens como a não patogenicidade, a não indução a resposta imune e a fácil produção. No entanto, a rápida duração da expressão genética e o baixo nível de expressão transgênica são as suas principais desvantagens.
De acordo com a interação com o meio biológico, os lipossomas podem ser caracterizados por possuírem interação não-específica com os fluidos biológicos (lipossomas convencionais), lipossomas estericamente estabilizados (longa duração) e com ligantes de direcionamento incorporados à estrutura (sítio-específicos). O primeiro grupo é caracterizado por possuir um fosfolipídios estrutural adicionado de um colesterol e um lipídeo com carga. Já o segundo grupo possui, além dos constituintes presentes no primeiro, uma cobertura por um polímero hidrofílico inerte, como o polietilenoglicol (PEG), à superfície. Os ligantes de direcionamento presentes no terceiro grupo podem ser anticorpos monoclonais ou oligossacarídeos.
Aplicações[editar | editar código-fonte]
Administração de medicamentos
Devido à sua estrutura, os lipossomos permitem o encapsulamento de uma alta variedade de drogas hidrofílica (dentro do núcleo) ou drogas hidrofóbica (na parte hidrofóbica da membrana), bem como moléculas anfifílicas (como parte da membrana).[2]
O uso de formas lipossomas como sistemas de liberação lenta de medicamentos é viável clinicamente por serem tipicamente feitos de moléculas lipídicas de origem natural, biodegradável e não tóxica. Esse tipo de aplicação iniciou-se em meados de 1970. Os lipossomas podem proteger o fármaco de degradação enzimática, possibilitam o aumento da concentração da droga no sítio alvo, podem ser utilizados como excipientes não tóxico para a solubilização de fármacos hidrofóbicos, além de prolongar o tempo do fármaco na circulação, permitindo um possível direcionamento para sítios específicos de células ou órgãos.Alguns problemas relacionados aos lipossomas têm sido a rápida liberação no sangue, devido a adsorção de proteínas do plasma (opsoninas) com a membrana fosfolipídica, como também reconhecimento e captação dos lipossomas pelo sistema fagocítico mononuclear (SFM).A habilidade dos lipossomas para penetrar nos tecidos doentes está diretamente correlacionada com o seu tamanho. Lipossomas grandes são rapidamente removidos da circulação por macrófagos (SFM) e não se obtém significantes níveis nos outros tecidos do corpo, enquanto lipossomas pequenos (≤ 100 nm) demoram um pouco mais para serem reconhecidos e fagocitados, aumentando a probabilidade dos mesmos de penetrarem os tecidos.
Alguns lipossomas que encapsulam fármacos e vacinas exibem superior propriedades farmacológicas sobre os medicamentos tradicionais. Isso pode ser evidenciado em áreas como quimioterapia do câncer, terapia antimicrobiana, vacinas, diagnóstico por imagem e tratamento de desordens oftálmicas. No tratamento do câncer eles alteram a farmacocinética e biodistribuição do fármaco no organismo. Os lipossomas ainda podem ser modificados para atacar somente as células tumorais, uma estratégia é a da inserção de folatos. As células tumorais possuem mais receptores de folatos que as células “normais”, isso auxilia a direcionar os lipossomas apenas para as células de câncer. Tornando o tratamento mais efetivo e diminuindo o dano ao organismo.[3]
Cosméticos
Um dos principais problemas da aplicação tópica de cosméticos é a impermeabilidade da barreira do estrato córneo. Para obter o efeito desejado, o ingrediente ativo não apenas precisa atravessar essa barreira, mas uma quantidade suficiente também deve atingir as camadas mais profundas da pele. O encapsulamento de cosméticos por lipossomas é uma das alternativas encontradas para a liberação controlada do ativo em uma camada específica da pele, visto que, as bicamadas flexíveis e macias dos lipossomas podem se misturar efetivamente com os lipídios da pele. Isso pode suavizar a preenchimento lipídico entre células queratinizadas e melhora a penetração do cosmético.[4]
Alimentos
Nesse caso os lipossomas podem atuar como carreadores de antioxidantes, um exemplo é o beta caroteno. O beta caroteno é um carotenoide rico em vitamina A, seu uso em alimentos é extremamente complicado, visto que ele é altamente sensível à luz e temperatura. Nesse caso, o lipossoma age como uma “barreira” que protege a vitamina evitando a sua degradação.
Métodos de preparo[5][6][editar | editar código-fonte]
Há diferentes métodos de preparo de lipossomas que resultam em diferentes tamanhos, estruturas e capacidade de encapsulação. De acordo com o método, é possível obter vesículas multi ou unilamelares.
Dispersão mecânica
- Hidratação de filme lipídico: Uma solução aquosa é adicionada à um filme fosfolipídico, obtido pela evaporação de um solvente orgânico no qual os fosfolipídeos estavam solubilizados. O filme fosfolipídeo engloba as moléculas de água e as substâncias que estiverem solubilizadas nela para formar as vesículas. Esse processo de dispersão pode ser facilitado por agitação por vórtex ou pela presença de pérolas de vidro; Entretanto, uma agitação vigorosa gera uma ampla faixa de tamanho dos lipossomas formados;
- Sonicação: Consiste no uso da técnica de ultra-som para preparo dos lipossomas. Nessa técnica obtém-se menores tamanhos de partículas que na técnica de hidratação de filme. Os diâmetros variam de 20 a 50nm;
- Extrusão: Essas técnicas baseiam-se na utilização de uma prensa ou de membranas policarbonato;
- Microfluidização: Usa a força de duas correntes de dispersão de lipossomas que colidem entre si sob alta pressão, reduzindo o tamanho das vesículas. O choque entre partículas promove ruptura das vesículas maiores que se organizam em vesículas menores. Os diâmetros obtidos são inferiores a 0,1 μm;
- Desidratação-Reidratação: Após o preparo do lipossoma por alguma das técnicas descritas adiciona-se o soluto que deseja encapsular em solução aquosa e retira-se a água com auxilio de um liofilizador. Com a desidratação as vesículas pequenas fundem-se para formar um filme multilamelar que se intercala com as moléculas do soluto.
Dispersão solvente
- Injeção de etanol: Uma solução de lipossomas em etanol é injetada em uma solução aquosa. O tamanho dos lipossomas unilamelares formadas depende da velocidade de injeção, volume e concentração;
- Infusão de éter: Mesmo principio da injeção com etanol, porém o éter é facilmente evaporado ao entrar em contato com uma solução aquosa aquecida, facilitando o processo.
- Remoção de detergente: Os fosfolipídeos são solubilizados em meio aquoso pela adição de um detergente; formam-se micelas mistas e, em seguida, o detergente é removido.
Referências[editar | editar código-fonte]
- Jacome-Junior, A.T. Desenvolvimento de formas lipossomais contendo levana. Tese de mestrado. Universidade Federal de Pernambuco, Pernambuco, 2006. 67f.
- Lasic, D. D. Novel application of liposomes. Trends in Biotechnology, 16, 307-321, 1998.
- Medina, O.P.; Zhu, Y.; Kairemo, K. Target liposomal drug delivery in cancer. Current Pharmaceutical Design, v. 10, n. 24, p. 2981-2989, 2004.
- Ramesh, R.; Saeki, T.; Templeton, N.S.; Ji, L.; Stephens, L.C.; Ito, I.; Wilson, D.R.; Wu, Z.; Branch, C.D.; Minna, J.D.; Roth, J.A. Successful treatment of primary and disseminated human lung cancers by systemic delivery of tumor suppressor genes using an improved liposome vector. Mol Ther, 3:1–14, 2001.
- SANTOS, C.N. e CASTANHO, M.A.R.B. Lipossomas: A bala acertou?, Química Nova, v. 25, 6B, p. 1181-1185, 2002.
- Torchilin VP. (2006) Adv Drug Deliv Rev. 58(14):1532-55, 2006.
- ↑ Costa, Raquel; Santos, Lúcia (dezembro de 2017). «Delivery systems for cosmetics - From manufacturing to the skin of natural antioxidants». Powder Technology (em inglês). 322: 402–416. doi:10.1016/j.powtec.2017.07.086
- ↑ Müller, Laura K.; Landfester, Katharina (18 de dezembro de 2015). «Natural liposomes and synthetic polymeric structures for biomedical applications». Biochemical and Biophysical Research Communications. Nanomedicine. 468 (3): 411–418. ISSN 0006-291X. doi:10.1016/j.bbrc.2015.08.088
- ↑ Vit, Franciele F. (4 de outubro de 2018). «O que são lipossomas e como eles podem auxiliar no combate de doenças». cientistasfeministas. Consultado em 19 de dezembro de 2019
- ↑ Lasic, D (1 de julho de 1998). «Novel applications of liposomes». Trends in Biotechnology. 16 (7): 307–321. doi:10.1016/S0167-7799(98)01220-7
- ↑ Panahi, Yunes; Farshbaf, Masoud; Mohammadhosseini, Majid; Mirahadi, Mozhdeh; Khalilov, Rovshan; Saghfi, Siamak; Akbarzadeh, Abolfazl (19 de maio de 2017). «Recent advances on liposomal nanoparticles: synthesis, characterization and biomedical applications». Artificial Cells, Nanomedicine, and Biotechnology. 45 (4): 788–799. ISSN 2169-1401. PMID 28278586. doi:10.1080/21691401.2017.1282496
- ↑ Akbarzadeh, Abolfazl; Rezaei-Sadabady, Rogaie; Davaran, Soodabeh; Joo, Sang Woo; Zarghami, Nosratollah; Hanifehpour, Younes; Samiei, Mohammad; Kouhi, Mohammad; Nejati-Koshki, Kazem (dezembro de 2013). «Liposome: classification, preparation, and applications». Nanoscale Research Letters (em inglês). 8 (1). 102 páginas. ISSN 1556-276X. PMC 3599573
 . PMID 23432972. doi:10.1186/1556-276X-8-102
. PMID 23432972. doi:10.1186/1556-276X-8-102

