Príon
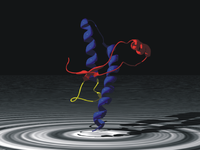
Príon (português brasileiro) ou Prião (português europeu) (a) é um agente infeccioso composto por proteínas com forma aberrante. Tais agentes não possuem ácidos nucleicos (DNA e/ou RNA) ao contrário dos demais agentes infecciosos conhecidos (vírus, bactérias, fungos e parasitas).[1] O termo prion (partículas infecciosas proteicas com ausência de ácidos nucléicos) foi cunhado em 1982 por Stanley B. Prusiner através de um amálgama entre as palavras proteinaceous (proteica) e infection (infecção). Os príons são responsáveis pelas encefalopatias espongiformes transmissíveis em uma variedade de mamíferos, incluindo os humanos.[2]
Os príons são um tipo de proteína intrinsecamente desordenada que mudam sua conformação a menos que estejam ligados a um parceiro específico, como outra proteína. Com um príon, duas cadeias de proteínas são estabilizadas se uma se ligar a outra na mesma conformação. A probabilidade de isso acontecer é baixa, mas quando acontece, a combinação das duas é muito estável. Então, mais unidades podem ser adicionadas, formando uma espécie de "fibrila".[3] Os príons formam agregados anormais de proteínas chamados amiloides, que se acumulam em tecidos infectados e estão associados a danos nos tecidos e morte celular.[4] Os amiloides também são responsáveis por várias outras doenças neurodegenerativas, como a doença de Alzheimer e a doença de Parkinson.[5][6]
Descoberta[editar | editar código-fonte]
O especialista em radiação Tikvah Alper e o matemático John Stanley Griffith desenvolveram, na década de 1960, a hipótese de que as encefalopatias espongiformes transmissíveis (TSEs) são causadas por um agente infeccioso constituído unicamente por proteínas.[7][8] Esta hipótese foi formulada para explicar a descoberta que o misterioso agente infeccioso, causador da scrapie e da doença de Creutzfeldt-Jakob, ser resistente à radiação ultravioleta (o UV causa dano direto ao DNA pela excitação de moléculas individuais do polímero de DNA, causando erro ao ser introduzido na seqüência de pares de bases).
Francis Crick reconheceu a potencial importância da hipótese de Griffith para a propagação do scrapie na segunda edição de seu famoso "Dogma Central da Biologia Molecular": embora afirmando que o fluxo da sequência de informações de proteína para proteína ou de proteína para RNA e DNA foi "impedido", ele observou que a hipótese de Griffith era potencialmente contraditória (embora ela não tenha sido somente promovida por Griffith).[9] Uma hipótese revisada foi posteriormente formulada, em parte, para acomodar a descoberta da transcrição reversa por Howard Temin e David Baltimore.
Stanley B. Prusiner, da Universidade da Califórnia, anunciou em 1982 que sua equipe havia purificado o hipotético agente infeccioso, e que tal agente consistia principalmente de uma proteína específica[10] - apesar de ele não conseguir isolar satisfatoriamente a proteína até dois anos depois de seu anúncio.[11] Prusiner conferiu o nome "prion" (proteinaceous infection) ao agente infeccioso,[10] e a proteína específica que compõe o príon foi chamada de "PrP" (Prion Protein), embora esta proteína possa ser encontrada tanto nas formas infecciosas como não infecciosas. Prusiner foi premiado com o Nobel de Fisiologia ou Medicina em 1997 pela sua pesquisa com príons,[12] mas não sem controvérsia.[13]
PrPSc (isoforma da scrapie da proteína priônica)[editar | editar código-fonte]
As PrPSc são o agente infeccioso por trás de doenças priônica. A proteína PrPSc foi o primeiro príon - isto é, a proteína infecciosa - a ser descoberto e continua a ser o príon por excelência, não apenas por causa de sua preeminência histórica, mas também por causa de sua associação com uma classe única de doenças fatais. A PrPSc é o único prion conhecido até agora por causar epidemias locais e explosões epizoóticas.[14] Essa proteína é uma variante alternativamente dobrada da proteína priônica celular, PrPC, que é uma proteína regular ancorada à GPI e que está presente na superfície celular de neurônios e outros tipos de células.[15]
Através de ressonância magnética (RM) da sequência completa da proteína PrPSc foi observado que a sua sequência de aminoácidos é idêntica à deduzida da sequência do gene da Prn-p, o gene codificador da proteína, eliminando assim qualquer variação na sequência pós-transcricional como uma das possíveis causas das propriedades patogênicas da PrPSc. Além disso, estudos de espectrometria de massa no modelo da PrPSc planejados para revelar qualquer modificação pós-traducional não caracterizada previamente indicaram que, de fato, a PrPSc e a PrPC são quimicamente idênticas. Assim, embora não se possa descartar a possibilidade de que uma pequena fração da PrPSc seja quimicamente modificada então tenha sido eliminada, parece mais provável que a PrPSc e a PrPC difiram apenas quanto às suas estruturas secundárias e/ou terciárias.[2] Infelizmente, a insolubilidade da PrPSc impede que a sua estrutura seja determinada.[2] Entretanto, algumas análises mostram que, de fato, as conformações da PrPSc e da PrPC são bem diferentes. A PrPC tem um alto conteúdo de hélices α (cerca de 40%), mas poucas folhas β (cerca de 3%) (de acordo com as estruturas de seus domínios globulares por RM), enquanto a PrPSc tem um conteúdo menor de hélices α (cerca de 30%), mas um alto conteúdo de folhas β (cerca de 45%). Em um modelo plausível da PrPSc, a sua região N-terminal dobra-se novamente formando uma estrutura chamada β-hélice, em que as folhas do polipeptídeo formam uma hélice voltada para a esquerda, contendo três fitas β paralelas. Apenas as duas hélices C-terminais de PrPC, que estão unidas por uma ligação dissulfeto, mantêm as suas conformações originais. O alto conteúdo de folhas β da PrPSc poderia, presumivelmente, facilitar a agregação da PrPSc em fibrilas amiloides.[2][15] Fica evidente, então, que a mudança conformacional de PrPC para PrPSc é autocatalítica; isto é, a PrPSc induz a PrPC a se converter em PrPSc.[15]
Nas células, a PrPSc é depositada em vesículas do citosol ao invés de ficar ancorada à superfície da membrana celular como a PrPc. As duas estão sujeitas a uma eventual degradação na célula. Entretanto, embora a PrPC seja completamente degradada, a PrPSc perde somente um segmento N-terminal de 67 resíduos de aminoácidos, formando um núcleo de 27 a 30 kDa resistente à proteólise, conhecido como PrP 27-30, que ainda exibe um alto conteúdo de folhas β. A PrP 27-30 se agrega então para formar as placas amiloides, que parecem ser diretamente responsáveis pela degeneração neuronal característica das doenças causadas por príons.[2]
Doenças priônicas[editar | editar código-fonte]
| Animais afetados | Doença |
|---|---|
| ovinos, caprinos | Paraplexia enzoótica dos ovinos[16] |
| bovinos | Encefalopatia espongiforme bovina (BSE), Doença da vaca louca[16] |
| marta[16] | Encefalopatia transmissível da marta (TME) |
| Veado-de-cauda-branca, alce, veado-mula[16] | Doença emaciante crônica (CWD) |
| gato[16] | Encefalopatia espongiforme felina (FSE) |
| niala, órix, kudu-grande[16] | Encefalopatia de ungulados exóticos (EUE) |
| avestruz[17] | Encefalopatia espongiforme (Não demonstrou ser transmissível.) |
| Humanos | Doença de Creutzfeldt-Jakob (CJD)[16] |
| Doença de Creutzfeldt–Jakob iatrogênica (iCJD) | |
| Doença de Creutzfeldt-Jakob variante (vCJD) | |
| Doença de Creutzfeldt-Jakob familiar (fCJD) | |
| Doença de Creutzfeldt-Jakob esporádica (sCJD) | |
| Síndrome de Gerstmann-Sträussler-Scheinker (GSS)[16] | |
| Insônia familiar fatal (FFI)[18] | |
| Kuru[16] |
Príons causam doença neurodegenerativa por formação de agregados extracelulares dentro do sistema nervoso central que formam placas conhecidas por amilóide, que rompem as estruturas do tecido normal. Este rompimento é caracterizado por "buracos" no tecido que resultam numa arquitetura espongiforme devido a formação de vacúolos nos neurônios.[19] Outras mudanças histológicas incluem a astrogliose e a ausência de uma reação inflamatória.[20] Enquanto o período de incubação das doenças priônicas é geralmente longo, uma vez que os sintomas aparecem, a doença progride rapidamente, levando a danos cerebrais e morte.[21] Os sintomas neurodegenerativos podem incluir convulsões, demência, ataxia e mudanças comportamentais e de personalidade.
Todas as doenças priônicas conhecidas são coletivamente denominadas de encefalopatias espongiformes transmissíveis (TSEs), uma vez que em todas essas doenças os neurônios desenvolvem grandes vacúolos. Ao que se sabe, essas enfermidades não apresentam tratamento e são fatais.[22] Podemos citar alguns exemplos de doenças priônicas: a scrapie (do inglês scrapie: raspar), uma doença neurológica de ovinos e caprinos, assim chamada por causa da tendência que as ovelhas infectadas têm em raspar a lã (eles se esfregam contra as cercas em um esforço de se manter de pé, devido à perda da coordenação muscular); a encefalopatia espongiforme bovina (BSE ou doença da vaca louca), que afeta o gado bovino de forma semelhante; e a kuru, uma doença degenerativa do cérebro que ocorre entre os primitivos habitantes de Papua Nova Guiné (kuru significa tremores) e que é transmitida pelo ritual de canibalismo. Há também uma doença humana esporádica (aparentemente aparece de forma espontânea) com sintomas similares, a doença de Creutzfeldt-Jak.ob (DCJ), uma rara e progressiva desordem cerebelar, que se assemelha e pode ser idêntica à kuru.[2] Além dessas, outras doenças e variantes também foram observadas, conforme vemos na tabela a direta.
Várias espécies de mamíferos são afetadas pelas doenças priônicas, e as proteínas priônicas (PrP) são muito similares em todas elas.[23] Apesar da pequena variação na PrP entre diferentes espécies, é incomum uma doença priônica ser transmitida de uma espécie para outra. Entretanto, a doença de Creutzfeldt-Jakob Variante, conhecida popularmente como doença da vaca louca, é causada por um príon que tipicamente infecta bovinos, causando a encefalopatia espongiforme bovina e é transmitida através da carne infectada.[24]
Proteínas mostrando um comportamento semelhante ao dos príons são também observados em fungos, que tem sido úteis nas pesquisas para compreender os príons mamíferos. Os príons fúngicos aparentemente não causam nenhuma patologia em seus hospedeiros.
Uma vacina tem sido desenvolvida em ratos, uma pesquisa que pode fornecer informações e contribuir para o desenvolvimento de uma vacina humana de resistência à infecção priônica.[25] Adicionalmente, em 2006, cientistas anunciaram que tinham modificado geneticamente bovinos sem o gene necessário para a produção de príons - assim, teoricamente fazendo estes animais imunes a TSE.
Notas[editar | editar código-fonte]
- Nota (a): Na língua portuguesa o termo deriva do aportuguesamento do original em inglês, sendo diferente entre as variantes europeia e brasileira.[26][27]
Referências
- ↑ Luketa S. (2012). «New views on the megaclassification of life» (PDF). Protistology. 7 (4): 218–237
- ↑ a b c d e f Voet, Donald (2013). Bioquimica. [S.l.]: Artmed
- ↑ Michel Brahic (10 de novembro de 2021). «The surprising upsides of the prions behind horrifying brain diseases». New Scientist. Cópia arquivada em 13 de novembro de 2021
- ↑ Dobson CM (fevereiro de 2001). «The structural basis of protein folding and its links with human disease». Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. 356 (1406): 133-45. PMC 1088418
 . PMID 11260793. doi:10.1098/rstb.2000.0758
. PMID 11260793. doi:10.1098/rstb.2000.0758
- ↑ Golde TE, Borchelt DR, Giasson BI, Lewis J (maio de 2013). «Thinking laterally about neurodegenerative proteinopathies». The Journal of Clinical Investigation. 123 (5): 1847-55. PMC 3635732
 . PMID 23635781. doi:10.1172/JCI66029
. PMID 23635781. doi:10.1172/JCI66029
- ↑ Irvine GB, El-Agnaf OM, Shankar GM, Walsh DM (2008). «Protein aggregation in the brain: the molecular basis for Alzheimer's and Parkinson's diseases». Molecular Medicine. 14 (7-8): 451-64. PMC 2274891
 . PMID 18368143. doi:10.2119/2007-00100.Irvine
. PMID 18368143. doi:10.2119/2007-00100.Irvine
- ↑ ALPER, T.; CRAMP, W.A.; HAIG, D.A.; CLARKE, M.C. (1967). «Does the agent of scrapie replicate without nucleic acid?». Nature. 214 (5090): 764–6. doi:10.1038/214764a0
- ↑ GRIFFITH, J.S. (1967). «Self-replication and scrapie». Nature. 215 (5105): 1043–4. doi:10.1038/2151043a0
- ↑ CRICK, F. (1970). «Central dogma of molecular biology». Nature. 227 (5258): 561–563. doi:10.1038/227561a0
- ↑ a b PRUSINER, S.B. (1982). «Novel proteinaceous infectious particles cause scrapie». Science. 216: 136-144. doi:10.1126/science.6801762
- ↑ TAUBES, G. (1986). «The game of name is fame. But is it science?». Discover. 7 (12): 28–41
- ↑ «The Nobel Prize in Physiology or Medicine, 1997». NobelPrize.org. Consultado em 28 de fevereiro de 2010
- ↑ TAUBES, G. (outubro de 1997). «Nobel Gas». Slate. Consultado em 20 de maio de 2011
- ↑ Requena, Jesús R.; Kristensson, Krister; Korth, Carsten; Zurzolo, Chiara; Simmons, Marion; Aguilar-Calvo, Patricia; Aguzzi, Adriano; Andreoletti, Olivier; Benestad, Sylvie L. (3 de maio de 2016). «The Priority position paper: Protecting Europe's food chain from prions». Prion. 10 (3): 165–181. ISSN 1933-690X. PMC 4981192
 . PMID 27220820. doi:10.1080/19336896.2016.1175801
. PMID 27220820. doi:10.1080/19336896.2016.1175801
- ↑ a b c Wille, Holger; Requena, Jesús R. (7 de fevereiro de 2018). «The Structure of PrPSc Prions». Pathogens (Basel, Switzerland). 7 (1). ISSN 2076-0817. PMC 5874746
 . PMID 29414853. doi:10.3390/pathogens7010020
. PMID 29414853. doi:10.3390/pathogens7010020
- ↑ a b c d e f g h i «90. Prions». ICTVdB Index of Viruses. U.S. National Institutes of Health website. 14 de fevereiro de 2002. Consultado em 28 de fevereiro de 2010
- ↑ Hussein MF, Al-Mufarrej SI (2004). «Prion Diseases: A Review; II. Prion Diseases in Man and Animals» (PDF). Scientific Journal of King Faisal University (Basic and Applied Sciences). 5 (2). 139 páginas. Consultado em 28 de fevereiro de 2010. Arquivado do original (pdf) em 10 de maio de 2011
- ↑ «BSE proteins may cause fatal insomnia.». BBC News. 28 de maio de 1999. Consultado em 28 de fevereiro de 2010
- ↑ Robbins SL, Cotran RS, Kumar V, Collins T, ed. (1999). Robbins pathologic basis of disease. Philadelphia: Saunders. ISBN 0-7216-7335-X
- ↑ Belay ED (1999). «Transmissible spongiform encephalopathies in humans». Annual Review of Microbiology. 53: 283–314. PMID 10547693. doi:10.1146/annurev.micro.53.1.283. Consultado em 28 de fevereiro de 2010
- ↑ «Prion Diseases». US Centers for Disease Control. 26 de janeiro de 2006. Consultado em 28 de fevereiro de 2010. Arquivado do original em 26 de março de 2016
- ↑ Gilch S, Winklhofer KF, Groschup MH,; et al. (agosto de 2001). «Intracellular re-routing of prion protein prevents propagation of PrP(Sc) and delays onset of prion disease». The EMBO Journal. 20 (15): 3957–66. PMC 149175
 . PMID 11483499. doi:10.1093/emboj/20.15.3957
. PMID 11483499. doi:10.1093/emboj/20.15.3957
- ↑ Collinge J (2001). «Prion diseases of humans and animals: their causes and molecular basis». Annual Review of Neuroscience. 24: 519–50. PMID 11283320. doi:10.1146/annurev.neuro.24.1.519. Consultado em 28 de fevereiro de 2010
- ↑ Ironside JW (2006). «Variant Creutzfeldt-Jakob disease: risk of transmission by blood transfusion and blood therapies». Haemophilia : the Official Journal of the World Federation of Hemophilia. 12 Suppl 1: 8–15; discussion 26–8. PMID 16445812. doi:10.1111/j.1365-2516.2006.01195.x. Consultado em 28 de fevereiro de 2010[ligação inativa]
- ↑ New York University Medical Center and School of Medicine (14 de maio de 2005). «Active Vaccine Prevents Mice From Developing Prion Disease». Science Daily. Consultado em 28 de fevereiro de 2010
- ↑ "príon", in HOUAISS, A. (2001). Dicionário Houaiss da Língua Portuguesa. [S.l.]: Objetiva. ISBN 9788573023831
- ↑ «"prião"». Dicionário Priberam. 2012. Consultado em 9 de março de 2012
Ligações externas[editar | editar código-fonte]
- OKAMOTO, Ivan H. «Encefalopatia Espongiforme Sub-aguda: Demências priônicas.» Revista Neurociências 12(1), janeiro de 2019; doi:10.34024/rnc.2004.v12.8882
- TAYLOR, David R., HOOPER, Nigel M. The prion protein and lipid rafts. Molecular Membrane Biology. Volume 23, 2006, #1; doi: 10.1080/09687860500449994
- NORSTROM, Eric M., MASTRIANNI, James A. The Charge Structure of Helix 1 in the Prion Protein Regulates Conversion to Pathogenic PrPSc. Journal of Virology, setembro de 2006; 80(17): 8521–8529; doi: 10.1128/JVI.00366-06
- BENNION, Brian J., DEMARCO, Mari L., DAGGETT, Valerie. Preventing Misfolding of the Prion Protein by Trimethylamine. Biochemistry, 2004, 43, 41, 12955–12963 doi: 10.1021/bi0486379
- CAMPANA, Vincenza, SARNATARO, Daniela, ZURZOLO, Chiara. The highways and byways of prion protein trafficking. Trends Cell Biology, fevereiro de 2005. Volume 15, # 2, pp 102-111; doi: 10.1016/j.tcb.2004.12.002
