Kwarc

| |
| Właściwości chemiczne i fizyczne | |
| Skład chemiczny |
tlenek krzemu(IV), SiO2 |
|---|---|
| Twardość w skali Mohsa |
7[1] |
| Przełam |
muszlowy[1] |
| Łupliwość |
bardzo niewyraźna[1] |
| Pokrój kryształu |
słupkowe, tabliczkowe, pręcikowe, igiełkowe, krótkosłupowe[1] |
| Układ krystalograficzny |
|
| Właściwości mechaniczne | |
| Gęstość minerału |
2,65 g/cm³[1] |
| Właściwości optyczne | |
| Barwa |
w czystej formie bezbarwny, odmiany mogą przyjmować różne zabarwienie[1] |
| Rysa |
biała |
| Połysk |
szklisty, tłusty[1] |
| Współczynnik załamania |
1,544–1,553[3] |
| Inne |
|
| Dodatkowe dane | |
| Postacie alotropowe | |
| Klasyfikacja Strunza |
4/D.01[7] |
Kwarc – minerał, modyfikacja krystaliczna krzemionki, należąca do krzemianów szkieletowych. Jest minerałem skałotwórczym wielu skał, kamieniem ozdobnym, a niektóre odmiany uznawane są za kamienie szlachetne lub półszlachetne.
Kwarc jest jednym z najczęściej występujących minerałów w skorupie ziemskiej. Występuje samodzielnie w postaci kryształów, zlepieńców, żył i ziaren. Jest ważnym składnikiem skał: magmowych (np. granit), metamorficznych (np. kwarcytów, gnejsów), rozpowszechniony jako produkt procesów hydrotermalnych tworząc żyły i druzy czystego kwarcu. Tworzy lub jest składnikiem skał osadowych (piasek kwarcowy, piaskowiec)[8].
Jego nazwa pochodzi od słowiańskiego słowa oznaczającego „twardy”[3]. Dawniej znany jako kwarzec[9].
Właściwości[edytuj | edytuj kod]
Czysty kwarc jest bezbarwny, przezroczysty dla ultrafioletu i częściowo podczerwieni. Przełam muszlowy, połyskliwy. Nawet znikome domieszki barwią go, zmienia barwę w wyniku naświetlania ultrafioletem, promieniowaniem rentgenowskim oraz w wyniku podgrzewania. Aktywny optycznie, kryształy skręcające polaryzację w lewo określane są jako lewe, a skręcające w prawo jako prawe. Twardy i kruchy, jest wzorcem twardości 7 w skali twardości Mohsa[10].
Jest dobrym dielektrykiem, o przenikalności elektrycznej zależnej od kierunku, w temperaturze pokojowej względna przenikalność elektryczna w osi 11 wynosi 4,58, a w osi 33 – 4,70. Jest piezoelektrykiem[11].
Kwarc odznacza się największą spośród głównych minerałów skałotwórczych odpornością na wietrzenie fizyczne i chemiczne[12]. Bardzo słabo przewodzi ciepło[13].
Niektóre okazy kwarcu po oszlifowaniu wykazują asteryzm[1].
Powstaje podczas sylifikacji wielu substancji między innymi tworząc skamieniałe drzewa[14].
W temperaturze pokojowej niemal obojętny chemicznie, stabilny w umiarkowanych, a w wysokich temperaturach przetworzony w szkło kwarcowe, przez co stosowany jako materiał do wyrobu aparatury i naczyń chemicznych. Nie reaguje z kwasami, z wyjątkiem kwasu fluorowodorowego, w wyniku reakcji z którym powstaje fluorek krzemu SiF
4 i kwas fluorokrzemowy H
2SiF
6. Reaguje z substancjami silnie alkalicznymi, szybkość reakcji zależy od postaci krystalicznej kwarcu i temperatury, w wyniku czego powstają krzemiany np. K
2SiO
3. Reagując z alkalicznymi składnikami betonu, głównie wodorotlenkiem wapnia, powoduje powstanie żeli krzemionkowych w betonie, które pochłaniając wodę pęcznieją i powodują pękanie betonu, ale proces ten jest powolny[15]. Reagując z wodorotlenkiem wapnia w temperaturze ok. 200 °C, powstające uwodnione krzemiany są głównym materiałem wiążącym w silikatach.
Reaguje ze stopionymi węglanami sodu i potasu, tworząc krzemiany. W środowisku geologicznym w wysokiej temperaturze rozpuszcza się w wodzie, działa jak kwas i reaguje z minerałami alkalicznymi, tworząc związki np. Wollastonit (Ca
3Si
3O
9)[15].
W wysokiej temperaturze, około 2000 °C, reaguje z węglem, w wyniku czego powstaje krzem i tlenek węgla. Reakcja ta jest używana do przemysłowego wytwarzania krzemu[15].
W temperaturze pokojowej kwarc jest praktycznie nierozpuszczalny w wodzie, stężenie równowagowe zależy od temperatury, ciśnienia oraz struktury kwarcu, w temperaturze 25 °C dla kwarcu makrokrystalicznego wynosi od 3 – 11 mg/l, a dla mikrokrystalicznego 22–34 mg/l, a proces rozpuszczania jest bardzo powolny. Pomimo tego w skali geologicznej rozpuszczanie i krystalizacja kwarcu w podłożu skalnym i glebie odgrywa ważną rolę w gorącym i wilgotnym klimacie, co ma znaczenie np. przy tworzeniu się gleb laterytowych. W temperaturach powyżej 100 °C i wysokich ciśnieniach rozpuszczalność kwarcu znacznie wzrasta. W temperaturze 300 °C wynosi od 700 do 1200 mg/l, w zależności od ciśnienia. SiO
2 rozpuszcza się w wodzie tworząc kwas ortokrzemowy H
4SiO
4[15].
Rozpoznawanie[edytuj | edytuj kod]
Kwarc w większości przypadków może być rozpoznany poprzez następujące właściwości[16]:
- duża twardość – rysuje szkło, stal,
- szklisty połysk,
- słaba lub niewyraźna łupliwość,
- przełam muszlowy, szklisty połysk.
Występowanie[edytuj | edytuj kod]
Kwarc jest drugim najpospolitszym po skaleniach minerałem skorupy ziemskiej[17]. Jako minerał skałotwórczy stanowi ważny składnik wielu rodzajów skał magmowych zarówno głębinowych, jak i wylewnych, skał osadowych oraz metamorficznych[1].
W skorupie ziemskiej kwarc występuje w postaci krystalicznej, mikrokrystalicznej i kryptokrystalicznej. Rozróżnienie to wynika z wielkości monokryształów tworzących skałę. W skałach magmowych ziarna kwarcu są białawe lub szare, mają zazwyczaj nieregularny kształt, który zawdzięczają temu, że krzemionka krystalizuje z gorącej magmy jako jeden z ostatnich minerałów, więc wypełnia przestrzenie między już istniejącymi ziarnami mineralnymi. W ten sposób powstają granitoidy, granity[18].
W trakcie krzepnięcia magmy zmienia się skład pozostającej magmy (różnicowania magmy) w procesach pegmatytowych i hydrotermalnych. Proces ten jest konsekwencją tego, że krzemionka jest rozpuszczalna w wodzie w wysokiej temperaturze pod dużym ciśnieniem, a rozpuszczalność ta zmniejsza znacznie przy spadku temperatury, pozostała magma wnika często w szczeliny w skałach. W ten sposób powstają w postaci żył (Kwarc żyłowy) i druz skupiska czystego kwarcu[19]. Żyły kwarcu mogą osiągać znaczne rozmiary, stając się złożami użytkowymi. W Polsce złoża kwarcu żyłowego występują w województwie dolnośląskim, ich zasobność jest szacowana na 2,87 mln t. Od 2007 r. w Polsce nie eksploatuje się złóż kwarcu żyłowego[20]. W Górach Izerskich w pobliżu Szklarskiej Poręby była Kopalnia kwarcu „Stanisław”.
Ze względu na swoją twardość, odporność na wietrzenie i znikomą rozpuszczalność w wodzie, z niszczonych skał pozostają tylko ziarna kwarcu, a ziarna pozostałych minerałów ulegają znacznemu rozdrobnieniu. Produkty rozpadu transportowane przez wodę i powietrze ulegają segregacji tworząc złoża piasku, żwiru, a nawet otoczaków[14][18]. Ocierające się ziarna pisku ulegają zaokrągleniu. Piasek zalegając długo pod obciążeniem ulega zagęszczeniu i spajaniu ziaren tworząc piaskowce. Złoża piasku kwarcowego i piaskowców są głównym źródłem krzemionki dla przemysłu i materiału dla budownictwa. Głównym kryterium klasyfikacji piasków kwarcowych jest ich czystość, najczystsze piaski i luźne piaskowce określane są jako materiały szklarskie. Ze względu na zastosowania piaski kwarcowe można podzielić na: piaski szklarskie, piaski formierskie, piaski podsadzkowe i piaski budowlane[21]. Silnie spojone piaskowce stają się skałą litą[18].
W wyniku różnych procesów fizycznych i chemicznych, nie do końca poznanych, powstają skały zawierające kwarc w postaci mikrokryształów (kwarc skrytokrystaliczny), uznawany też za minerał Chalcedon, występuje w kwarcycie, krzemieniu i wielu innych[22].
Skupiska tego minerału znajdują się w Las Vigas w Meksyku, w Corinto w Brazylii, w Oravița w Rumunii, w Masywie Świętego Gotarda w Szwajcarii[1], w Strzegomiu w Polsce, w Baveno we Włoszech oraz na Uralu. Słynne są okazy z Przełęczy Furka w Alpach[14].
Minerałami towarzyszącymi dla kwarcu są m.in. kalcyt, skalenie, turmaliny i granaty[1].
Krystalografia[edytuj | edytuj kod]
Wyróżnia się[b]:
- kwarc α[10] – kwarc niskotemperaturowy, krystalizujący się w układzie trygonalnym, powszechnie występujący na powierzchni Ziemi. Jest trwały w temperaturze do 573[24] °C. Odmiana α występuje w zwykłych warunkach[10].
- kwarc β[10] – kwarc wysokotemperaturowy, krystalizujący się w układzie heksagonalnym, z magmy[24], występujący w naturze na głębokości 25–30 km[10]. Często występuje w postaci podwójnej piramidy heksagonalnej i słupa heksagonalnego. Po schłodzeniu do temperatury przejścia fazowego w 573 °C przechodzi w formę α i przy ciśnieniu atmosferycznym nawet przy bardzo szybkim chłodzeniu nie pozostaje w stanie β. Spotyka się jego paramorfozy w skałach magmowych[24]. W temperaturze 870 °C kwarc β przechodzi w trydymit. Przemianom towarzyszy zmiana objętości, co może powodować pęknięcia materiałów zawierających kryształy kwarcu. Przy szybkim podgrzewaniu kwarc β topi się w temperaturze 1550 °C. Temperatura przemian rośnie wraz ze wzrostem ciśnienia[10].
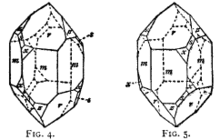
Kryształy kwarcu w zależności od warunków powstawania są bardzo zróżnicowane[14]. Idealny kształt kryształu to sześcioboczny prostopadłościan zakończony sześciokątnymi ostrosłupami na każdym końcu. Minerał ten najczęściej tworzy kryształy słupkowe o przekroju sześciokątnym[1], ze ścianami pokrytymi prążkami prostopadłymi do osi słupa[19]. Występują także kryształy tabliczkowe, pręcikowe, igiełkowe, krótkosłupowe zakończone dwoma romboedrami oraz kryształy o kształcie piramidy heksagonalnej[1]. Częste są zbliźniaczenia, będące połączeniem kryształów lewych z prawymi, zrośniętych pod różnym kątem. Najczęściej występują tzw. bliźniaki japońskie, zrośnięte pod kątem 84°33′[6], bliźniaki brazylijskie oraz delfinackie[1]. Kryształy prawe od lewych można odróżnić po położeniu trójkątnych ścian na narożach względem ścian romboidalnych[1].
Struktura[edytuj | edytuj kod]

Kwarc ma wzór cząsteczkowy SiO
2, jest odmianą polimorficzną krzemionki. Wiązania między atomami krzemu (Si) i tlenu (O) są kowalencyjne, ale silnie spolaryzowane, elektrony są silniej przyciągane przez tlen przez co przy tlenie przeważa ładunek ujemny, a przy krzemie dodatni, przez co wiązanie jest też postrzegane jako jonowe[25][15]. Kąt Si-O-Si jest bardziej rozwarty a długość wiązania Si-O jest krótsza niż obliczona dla wiązania pojedynczego. Wskazuje to na częściowy, podwójny charakter tego wiązania, co również wyjaśniałoby jego dużą siłę[15].
Kryształ kwarcu nie składa się z oddzielnych cząsteczek SiO
2; nie jest substancją molekularną, ale jest siecią kowalencyjną, czyli układem elementów ułożonych w pewien regularny wzór. W sieci tej każdy atom krzemu jest połączony z czterema atomami tlenu, a każdy atom tlenu jest połączony z dwoma atomami krzemu. Odległości między atomem tlenu a sąsiadującymi z nim atomami krzemu (Si – O – Si) nie są jednakowe, jedna wynosi 1,6054 Å a druga 1,6109 Å, różnica ta jest znikoma i jako nie mająca większego znaczenia jest pomijana. Atomy układu Si – O – Si nie leżą na linii prostej, a tworzony kąt jest głównym wyróżnikiem układu krystalograficznego krzemionki. W kwarcu α kąt ten (kąt wiązania) ma rozwartość około 144°, w kwarcu beta 147°. W kwarcu α odległość jonu tlenu do sąsiedniego jonu tlenu to około 2,62 Å. Każdy jon krzemu jest otoczony przez cztery jony tlenu, te silnie związane atomy tworzą czworościan, który jest uznawany za podstawowy elementem budowy sieci. Czworościenna komórka SO
4 łączy się w każdym wierzchołku z sąsiednią, dzieląc z nią jeden atom tlenu. Kąt wiązania Si – O – Si sprawia, że sąsiednie czworościany obrócone są względem siebie, tworząc spirale w których obrót komórek w sieci może być lewoskrętny lub prawoskrętny, takie trzy komórki tworzą elementarny powtarzający się układ[25].
Czworościany SiO
4 są połączone ze sobą narożnikami, każdy czworościan z czterema sąsiednimi czworościanami. Czworościany nie wypełniają przestrzeni. W kierunku osi c są one połączone w spiralne łańcuchy. Między parami tych spiral (helis) SiO
4, są większe sześcioboczne i mniejsze trójkątne kanały, biegnące wzdłuż kryształu. Spiralne łańcuchy czworościanów są połączone z sześcioma sąsiednimi spiralami układami czworościanów w taki sposób, że każdy czworościan SiO
4 należy do dwóch sąsiednich łańcuchów czworościanów i graniczy z dwoma sześciobocznymi kanałami. Wszystkie helisy mają tę samą skrętność, ale różnią się ustawieniem czworościanów (polaryzacją), ale dwie sąsiednie helisy mają przeciwne polaryzacje. Każdy czworościan SiO 4 jest członkiem dwóch helis o przeciwnej polaryzacji. Wynikiem tego kryształ nie wykazuje polaryzacji względem osi c, a jest symetryczny względem niej[26].
-
Kwarc α, para łańcuchów spiralnych kwarcu α w kierunku osi a-c
-
Kwarc α, para łańcuchów spiralnych wokół sześciokątnego kanału, widok wzdłuż osi c (oś 3-krotna)
-
Kwarc α, połączenie spiralnych łańcuchów, rozkład dużych sześciokątnych i małych trójkątnych kanałów, widok wzdłuż osi c (oś 3-krotna)
Z powyższego opisu wynika, że kryształ kwarcu α ma potrójną symetrię obrotową wokół osi c i podwójną symetrię obrotową względem osi a, jest to trygonalny układ krystalograficzny, oznaczany jako P32, uwzględniając ręczność P3121 (nr 152) i P3221 (nr 154). Komórka elementarna ma wymiary a1 = a2 = 4,913 Å i c = 5,405 Å i zawiera trzy jednostki (cząsteczki) (Z=3)SiO
2[25].
Odmiany[edytuj | edytuj kod]

Dawniej różne odmiany kwarcu uznawano za oddzielne minerały. Pod koniec XVIII w. szwedzki chemik Bergmann odkrył, że są to te same substancje chemiczne, przez pewien czas krzemionka była uważana za pierwiastek chemiczny. W 1823 roku JJ Berzelius rozłożył kwarc i odkrył, że jest to związek chemiczny tlenu i krzemu[27].
Kwarc obejmuje formy krzemionki o opisanej wyżej strukturze krystalograficznej uporządkowanej zarówno makroskopowo, jak i wykazujące tę strukturę tylko w skali mikroskopowej. Klasyfikacja różnych rodzajów kwarcu opiera się głównie na wyglądzie i możliwości zaobserwowania monokrystalicznych struktur. Dawniej wyróżniano trzy odmiany kwarcu:
- kwarc makrokrystaliczny – okaz jest monokryształem lub widocznych kryształów,
- kwarc mikrokrystaliczny – okaz składa się z drobnych ziaren kryształów widocznych dopiero w mikroskopie optycznym
- kwarc skrytokrystaliczny – struktury nie można rozróżnić w mikroskopie optycznym
W nowej klasyfikacji wyróżnia się tylko dwie grupy: kwarc makrokrystaliczny, nazywany po prostu kwarcem, oraz kwarc skrytokrystaliczny, zwany chalcedonem. W kwarcu skrytokrystalicznym wyróżnia się odmiany włókniste i ziarniste, podział ten opiera się na wyglądzie cienkich skrawków pod mikroskopem polaryzacyjnym. Skaningowa mikroskopia elektronowa ujawniła, że oba rodzaje kwarcu składają się głównie z mikroskopijnie małych ziaren, a pozorne włókna są wynikiem efektów świetlnych na ziarnach odpowiedniej wielkości, których osie krystalograficzne leżą mniej więcej równolegle do siebie[27].
Właściwości kwarcu skrytokrystalicznego różnią się nieco od właściwości kwarcu makrokrystalicznego[27].
| Cecha | Makrokrystaliczny | Skrytokrystaliczny |
|---|---|---|
| Połysk | szklisty | woskowy - matowy |
| Współczynnik załamania światła | 1,54422 - 1,55332 | 1,53 - 1,54 |
| Gęstość [g/cm³] | 2,6481 | 2,4 - 2,7 |
| Twardość | 7 | 6,5 - 7 |
| Zawartość wody [%] | << 0,1 | 0,1 - 4 |
| Zanieczyszczenia [%] | 0,01 - 0,5 | 1 - 20 |
Powodem różnic jest to, że skrytokrystaliczne odmiany kwarcu składają się z mikroskopijnie małych, przerośniętych ziaren kryształu kwarcu, między którymi struktura krystalograficzna jest zaburzona, dlatego brakuje im strukturalnej jednorodności kryształów w miejscach tych łączenia krzemu z tlenem może mieć inne kąty niż w kwarcu, a w zaburzone struktury łatwiej wbudowują się zanieczyszczenia. Struktura takich kwarców zależy od warunków środowiskowych ich krystalizacji. Ściśle mówiąc, odmiany kryptokrystaliczne nie spełniają definicji minerału, określane są jako teksturalne odmiany kwarcu. Zawierają stosunkowo duże ilości innych modyfikacji krzemionki, wody i innych minerałów niekrzemionkowych[27].
Czysty kryształ kwarcu jest przezroczysty i bezbarwny, nazywany jest kryształem górskim[28]. Barwę i przezroczystość zmieniają dodatki, wtrącenia oraz defekty sieci krystalicznej, w których powstają centra barwne, których właściwości świetlne zmieniają się pod wpływem promieniowania jonizującego, ultrafioletu i podwyższonej temperatury.
Struktura kwarcu jest dość prosta, składa się czworościanów SiO
4. Mały rozmiar jonu krzemu nie pozwala na zastąpienie go jonami wielu pierwiastków, dlatego kwarc jest zazwyczaj dość czystym minerałem, zawiera jednak wtrącenia i zanieczyszczenia, mogące zastępować jony kryształu (podstawniki) lub być poza węzłami sieci (śródmiąższowe). W krysztale występują też nieregularności sieci krystalicznej określane jako zanieczyszczenia strukturalne. Jonami, które mogą zastąpić jon krzemu są: Fe+
3, Al+
3, OH−
i cząsteczka H
2O jako podstawniki, a Na+
, Li+
i H
3O+
jako jednostki śródmiąższowe. Zastąpienie czterowartościowego jonu Si jonami trójwartościowymi wymaga obecności kationów jednowartościowych by zrównoważyć ładunek elektryczny. Niektóre z tych wtrąceń i nieregularności sieci tworzą centra barwne, które wpływają charakterystycznie na barwę minerału[29]. W stanie podstawowym centrum barwnego elektron jest poza centrum i jest ono nieaktywne kolorystycznie. Promieniowanie o dużej energii, np. promieniowanie gamma, może wybić elektron z sieci krystalicznej i jeśli trafi on do centrum barwnego to pozostaje w nim w stanie metastabilnym, centrum barwne zmienia się w aktywne. Pochłania ono światło o określonej długości fali nadając barwę minerałowi. Elektron może opuścić centrum barwne jeśli dostarczy mu się odpowiednią ilość energii, np. w wyniku podgrzewania. Towarzyszy temu termoluminescencja oraz zmiana i utrata barwy przez minerał.
Wiele odmian kolorystycznych ma barwę wynikającą z aktywności centrów barwnych, zostały one wzbudzone przez promieniowanie występujące naturalnie w środowisku ich występowania, przykładami są kwarc dymny, ametyst. Stosuje się też modyfikację barwy kwarcu przez napromieniowywanie promieniowaniem gamma i przez wyżarzanie kryształów o nieatrakcyjnej barwie. Przykładowo wydobywane w Brazylii ametysty o nieatrakcyjnych barwach poddaje się wyżarzaniu w temperaturze do 470 °C otrzymując kamienie o żółtym zabarwieniu podobne do cytrynu[30].
Białe zabarwienie kwarcu, najsilniejsze w kwarcu mlecznym, występujące najczęściej w grubokrystalicznych żyłach kwarcu, wywołane jest występującymi licznie niewielkimi wtrąceniami wody i gazu. Wskazuje to na związek krystalizacji z procesami hydrotermalnymi, zachodzącymi w skałach w ostatnich etapach zastygania magmy[31]. Spotyka się kryształy, w których kwarc mleczny występuje jako mętne fantomy wewnątrz kryształu górskiego, ametystu, cytrynu lub kwarcu dymnego. Mleczny kwarc mógł powstać na wczesnym etapie wzrostu kryształu, a późniejszy etap wzrostu czystego kwarcu pokrył mleczny kwarc. Ametyst z mlecznym wnętrzem zwany jest jodełką ametystu[32].
Kwarc ma wiele odmian kolorystycznych, niektóre z nich mają nadane nazwy, m.in.:
- kryształ górski (bezbarwny)[28]
- ametyst (fioletowy)[19]
- kwarc dymny (brązowy)[19]
- cytryn (żółty)[19]
- kwarc różowy[19]
- kwarc niebieski[33]
- prazjolit (zielony)[34]
- kwarc mleczny (biały)[35]
- awenturyn (zielony)[36]
- tygrysie oko[37]
- kocie oko[12]
- sokole oko[12]
- chalcedon (skrytokrystaliczny)[19]
Możliwa jest zmiana wyglądu kryształów kwarcu, stosowane są metody[11]:
- rozgrzewanie i szybkie chłodzenie – powoduje wytworzenie licznych drobnych iryzujących pęknięć oraz wytworzenie mikrospękań umożliwiających barwienie;
- napromieniowanie – przemiana kryształu górskiego w kwarc dymny, intensyfikacja barwy niektórych barw;
- wygrzewanie – rozjaśnienie kwarcu dymnego i ametystu, zmiana barwy niektórych barw;
- powlekanie – polepszenie barwy;
- barwienie – wytworzenie oryginalnych barw podobnych do innych minerałów
- wybielanie – rozjaśnienie barwy kwarcu tygrysie oko.
Kwarc syntetyczny[edytuj | edytuj kod]

Wysoka temperatura topnienia utrudnia hodowlę kryształów kwarcu ze stopionego kwarcu. Przemiana krystaliczna w temperaturze 573 °C zmienia strukturę kryształu, dlatego wytwarzanie monokryształów kwarcu musi przebiegać poniżej tej temperatury[38].
Pierwsze próby hydrotermalnego uzyskiwania kryształów kwarcu przeprowadzono w połowie XIX w., w wyniku nich uzyskano mikroskopijne kryształy. W latach 1898–1908 G. Spezia informował o uzyskaniu makroskopowych kryształów z roztworów wodnych pod ciśnieniem w temperaturze dochodzącej do 350 °C. W okresie II wojny światowej R. Nacken prowadził próby hodowli kryształów kwarcu, po wojnie na podstawie tych prac opracowano metody komercyjnego wytwarzania kwarcu. Monokryształy kwarcu o dużym stopniu czystości wytwarzane są metodą hydrotermalną w warunkach zbliżonych do powstawania kwarcu hydrotermalnego w naturze. W autoklawie umieszcza się wodę z dodatkami i drobno zmieloną krzemionką. Do górnej ścianki przymocowane są zarodki kwarcu. Proces przeprowadza się w temperaturze około 400 °C i ciśnieniu 100–420 MPa, w tych warunkach krzemionka rozpuszcza się w wodzie (do 16%). Naczynie podgrzewa się od dołu, górna część naczynia z zarodkami jest chłodniejsza o około 20 °C. Ta różnica temperatur wystarcza by rozpuszczający się na dole kwarc, krystalizował na zalążkach[38].
Kwarc syntetyczny produkowany dla przemysł jest zazwyczaj bezbarwny, dla jubilerstwa w wielu barwach uzyskiwanych przez stosowanie dodatków oraz poprawianie metodami tymi samymi co dla kwarcu naturalnego. Dostępność zależy od rodzaju[39].
Zastosowanie[edytuj | edytuj kod]
- Jako oscylator[17].
- Do pozyskiwania krzemu[17].
- Do wyrobu szkła krzemionkowego[17].
- W jubilerstwie, jako kamień do pierścionków, broszek, wisiorków, naszyjników[1].
- Jako talizman[17].
Galeria[edytuj | edytuj kod]
-
Naturalny cytryn
Uwagi[edytuj | edytuj kod]
Przypisy[edytuj | edytuj kod]
- ↑ a b c d e f g h i j k l m n o p q r Rupert Hochleitner, Minerały: kamienie szlachetne, skały, Warszawa: Multico, 2022, s. 334, ISBN 978-83-7763-613-8.
- ↑ Jerzy Żaba, Ilustrowana encyklopedia skał i minerałów, Chorzów: Wydawnictwa Videograf, 2014, s. 236,237, ISBN 978-83-7835-297-6 [dostęp 2024-04-02].
- ↑ a b Schumann ↓, s. 132.
- ↑ Schumann ↓, s. 140.
- ↑ Schumann ↓, s. 131.
- ↑ a b Quartz [online], www.mindat.org [dostęp 2023-02-10].
- ↑ Strunz Classification – Primary Groups [online], www.mindat.org [dostęp 2023-02-10].
- ↑ Kwarc, [w:] Encyklopedia PWN [dostęp 2023-02-18].
- ↑ kwarzec – Wielki słownik W. Doroszewskiego PWN [online], sjp.pwn.pl [dostęp 2023-02-10] (pol.).
- ↑ a b c d e f Encyklopedia fizyki. T. 2. PWN, 1973, s. 139.
- ↑ a b Włodzimierz Łapot, Gemmologia szczegółowa. Vademecum, Katowice: Wydawnictwo Uniwersytetu Śląskiego, 2000, s. 206–213, ISBN 83-226-0939-6, OCLC 749836288 [dostęp 2023-03-08].
- ↑ a b c Ryszard Krzysztof Borówka, Bernard Cedro: Skarby ziemi. Poznań: Wydawnictwo Kurpisz, 2001, s. 50. ISBN 83-88276-40-9.
- ↑ Walter Schumann: Minerały świata. Warszawa: Alma-Press, s. 120. ISBN 978-83-7020-813-4.
- ↑ a b c d Medenbach i Sussieck-Fornefeld 1996 ↓, s. 106.
- ↑ a b c d e f The Quartz Page: Chemical Properties [online], www.quartzpage.de [dostęp 2023-03-21].
- ↑ Quartz [online].
- ↑ a b c d e Medenbach i Sussieck-Fornefeld 1996 ↓, s. 107.
- ↑ a b c Kwarc [online], zywaplaneta.pl [dostęp 2023-02-26].
- ↑ a b c d e f g Monica Price, Kevin Walsh: Kieszonkowy atlas skał i minerałów. Warszawa: Solis, s. 143. ISBN 978-83-87112-84-4.
- ↑ Portal Kopalin i Surowców Mineralnych – Polskie Kopalnie [online], surowce-kopalnie.pl [dostęp 2023-02-25].
- ↑ Zastosowanie piasków kwarcowych [online], Surowce Naturalne, 11 grudnia 2019 [dostęp 2023-02-26] (pol.).
- ↑ Mineralogia | Krzemienie [online], krzemienie.pl [dostęp 2023-02-27].
- ↑ Kuc, Witold. Wystawa pt. „Kwarc” w Muzeum Żup Krakowskich Wieliczka. „Przegląd Geologiczny” 63.12/2 (2015): 1437.
- ↑ a b c W. Jaroszewski (red.). Przewodnik do ćwiczeń z geologii dynamicznej. Wydawnictwa Geologiczne. Warszawa, 1986. Strony 21-22. ISBN 83-220-0180-0.
- ↑ a b c The Quartz Page: Quartz Structure [online], www.quartzpage.de [dostęp 2023-03-20].
- ↑ Mineralienatlas – Fossilienatlas [online], www.mineralienatlas.de [dostęp 2023-03-19] (niem.).
- ↑ a b c d e The Quartz Page: Types of Quartz [online], www.quartzpage.de [dostęp 2023-09-17].
- ↑ a b Rock Crystal [online], www.mindat.org [dostęp 2023-02-10].
- ↑ Instituto de Pesquisas Energeticas e Nucleares Brazil. Comissao Nacional de Energia Nuclear. Associacao Brasileira de Energia Nuclear, INAC 2009 : International Nuclear Atlantic Conference: Innovations in Nuclear Technology for a Sustainable Future: September 27 to October 2, 2009, Rio de Janeiro, Brazil., Rio de Janeiro 2009, ISBN 978-85-99141-03-8, OCLC 1039231115 [dostęp 2023-02-28].
- ↑ Olaf Medenbach, Minerały, Warszawa: Świat Książki, 1995, ISBN 83-7129-194-9, OCLC 924659082 [dostęp 2023-03-01].
- ↑ Kwarc mleczny [online], zywaplaneta.pl [dostęp 2023-03-03].
- ↑ MILKY QUARTZ: the cloudy white variety of quartz [online], www.galleries.com [dostęp 2023-03-03].
- ↑ Blue Quartz [online], www.mindat.org [dostęp 2023-02-10].
- ↑ Prasiolite [online], www.mindat.org [dostęp 2023-02-10].
- ↑ Milky Quartz [online], www.mindat.org [dostęp 2023-02-10].
- ↑ Aventurine [online], www.mindat.org [dostęp 2023-02-10].
- ↑ Tiger’s Eye [online], www.mindat.org [dostęp 2023-02-10].
- ↑ a b Quartz Hydrothermal Growth [online], www.roditi.com [dostęp 2023-03-06].
- ↑ Włodzimierz Łapot, Gemmologia szczegółowa. Vademecum, Katowice: Wydawnictwo Uniwersytetu Śląskiego, 2000, s. 213–216, ISBN 83-226-0939-6, OCLC 749836288 [dostęp 2023-03-08].
Bibliografia[edytuj | edytuj kod]
- Olaf Medenbach, Cornelia Sussieck-Fornefeld: Leksykon przyrodniczy. Minerały. Warszawa: Świat Książki, 1996, seria: Leksykon przyrodniczy. ISBN 83-7129-937-0.
- Walter Schumann: Kamienie szlachetne i ozdobne. Warszawa: Alma-Press. ISBN 978-83-7020-645-1.








