Eletrólise da água: diferenças entre revisões
bot: revertidas edições de 187.4.194.14 ( modificação suspeita : -96), para a edição 35800627 de Addbot |
|||
| Linha 6: | Linha 6: | ||
== História == |
== História == |
||
Jan Rudolph Deiman e Adriaan Paets van Troostwijk usaram em 1789 uma máquina |
Jan Rudolph Deiman e Adriaan Paets van Troostwijk usaram em 1789 uma máquina pedro boiola aelectroestática para produzir electricidade que foi descarregada em eletrodos de ouro em uma garrafa de Leyden com água. Em 1800, Alessandro Volta inventou a pilha. Algumas semanas mais tarde William Nicholson e Anthony Carlisle usaram-na para a eletrólise da água. Quando Zenobe Gramme inventou a máquina de Gramme, em 1869, a eletrólise da água tornou-se um método barato para a produção de hidrogênio. |
||
{{Referências}} |
{{Referências}} |
||
Revisão das 17h31min de 15 de julho de 2013
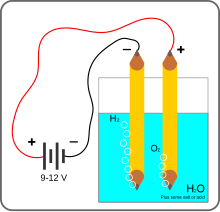
A Electrólise da água é a decomposição de água (H2O) em oxigênio (O2) e hidrogênio (H2) por efeito da passagem de uma corrente eléctrica pela água. No entanto, este processo electrolítico raramente é usado em aplicações industriais uma vez que o hidrogênio pode ser produzido mais acessivelmente através de combustíveis fósseis. Uma fonte de energia eléctrica está ligada a dois eléctrodos (geralmente feitos a partir de alguns metais inertes como a platina ou o aço inoxidável, no caso da imagem, é usada a grafite) que estão colocados na água. Se tudo estiver correctamente montado, origina-se hidrogénio no cátodo (o eléctrodo ligado ao terminal negativo da fonte de energia) e oxigénio no ânodo (o eléctrodo ligado ao terminal positivo da fonte de energia).
É necessária uma grande quantidade de energia para fazer a electrólise da água pura uma vez que esta não é boa condutora eléctrica. Sem o excesso de energia a electrólise da água pura ocorre muito lentamente. Isto deve-se á limitada auto-ionização da água: a cada 555 milhões de moléculas, somente uma se ioniza[1]. A condutividade eléctrica da água pura é cerca de um milhão de vezes menor que a da água do mar. A eficácia da electrólise da água pode ser aumentada adicionando um electrólito (como sal, um ácido ou uma base) e/ou utilizando eletrocatalisadores.
História
Jan Rudolph Deiman e Adriaan Paets van Troostwijk usaram em 1789 uma máquina pedro boiola aelectroestática para produzir electricidade que foi descarregada em eletrodos de ouro em uma garrafa de Leyden com água. Em 1800, Alessandro Volta inventou a pilha. Algumas semanas mais tarde William Nicholson e Anthony Carlisle usaram-na para a eletrólise da água. Quando Zenobe Gramme inventou a máquina de Gramme, em 1869, a eletrólise da água tornou-se um método barato para a produção de hidrogênio.
Referências
- ↑ Livro de "Física-Química" de Ricardo Feltre
