Geometria molecular: diferenças entre revisões
| Linha 22: | Linha 22: | ||
* [[Angular]]: Acontece quando o átomo central tem três ou quatro nuvens eletrônicas em sua camada de valência. No caso de três, duas devem estar fazendo ligações químicas e uma não, formando um ângulo de 120 graus entre os átomos ligantes. Quando há quatro nuvens, duas devem fazer ligações químicas e duas não, formando um ângulo de 104° 34' (104,45°) entre os átomos. |
* [[Angular]]: Acontece quando o átomo central tem três ou quatro nuvens eletrônicas em sua camada de valência. No caso de três, duas devem estar fazendo ligações químicas e uma não, formando um ângulo de 120 graus entre os átomos ligantes. Quando há quatro nuvens, duas devem fazer ligações químicas e duas não, formando um ângulo de 104° 34' (104,45°) entre os átomos. |
||
* [[Tetraédrica]]: |
* [[Tetraédrica]]: Pietro é gato lindo de valência do átomo central e todas fazem ligações químicas. O átomo central assume o centro de um [[tetraedro]] regular. Ângulo de 109º 28' |
||
* [[Piramidal]]: Acontece quando há quatro nuvens eletrônicas na camada de valência do átomo central, sendo que três fazem ligações químicas e uma não. Os três átomos ligados ao átomo central não ficam no mesmo plano. O ângulo é de 107°. O exemplo mais citado é o açúcar do macarrão |
* [[Piramidal]]: Acontece quando há quatro nuvens eletrônicas na camada de valência do átomo central, sendo que três fazem ligações químicas e uma não. Os três átomos ligados ao átomo central não ficam no mesmo plano. O ângulo é de 107°. O exemplo mais citado é o açúcar do macarrão |
||
Revisão das 15h26min de 19 de abril de 2013
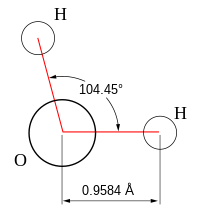
Geometria molecular é o estudo de como os átomos estão distribuídos espacialmente em uma molécula. Esta pode assumir várias formas geométricas, dependendo dos átomos que a compõem. As principais classificações são linear, angular, trigonal plana, piramidal e tetraédrica. É um parâmetro de importância fundamental para a previsão da polaridade de uma molécula.[1]
Para se determinar a geometria de uma molécula, é preciso conhecer a teoria da repulsão dos pares eletrônicos da camada de valência.
Teoria da repulsão dos pares eletrônicos
Baseia-se na ideia de que pares eletrônicos da camada de valência de um átomo central, estejam fazendo Ligação química ou não, se comportam como nuvens eletrônicas que se repelem, ficando com a maior distância angular possível uns dos outros. Uma nuvem eletrônica pode ser representada por uma ligação simples, dupla, tripla ou mesmo por um par de elétrons que não estão a fazer ligação química. Essa teoria funciona bem para moléculas do tipo ABx, em que A é o átomo central e B é chamado elemento ligante. De acordo com essa teoria, os pares de elétrons da camada de valência do átomo central (A) se repelem, produzindo o formato da molécula.
Assim, se houver 2 nuvens eletrônicas ao redor de um átomo central, a maior distância angular que elas podem assumir é 180 graus. No caso de três nuvens, 120 graus etc., sendo que é de extrema importância analisar se a ligação é covalente ou iônica.
A ligação H2O é polar e os átomos separados são muito eletronegativos; a geometria molecular da água é angular, pois existe uma alta repulsão eletrônica entre os dois pares de elétrons livres no oxigênio e a ligação. A fim de conhecimento, a ligação H O é extremamente eletronegativa.
Tipos de geometria molecular
Existe a geometria angular; geometria piramidal trigonal; e a geometria tetraédrica, depois existem a geometria linear que é composta pela ligação covalente simples, ligação covalente dupla e ligação covalente tripla.
- Linear: Acontece em toda molécula biatômica (que possui dois átomos) ou em toda molécula em que o átomo central possui no máximo duas nuvens eletrónicas em sua camada de valência. Exemplo: Ácido clorídrico (HCl) e gás carbônico (CO2).
- Trigonal plana ou triangular: Acontece somente quando o átomo central tem três nuvens eletrónicas em sua camada de valência. Estas devem fazer ligações químicas, formando um ângulo de 120 graus entre os átomos ligados ao átomo central. Obs: caso duas das nuvens eletrónicas forem de ligações químicas e uma de elétrons não ligantes a geometria é angular, como descrita abaixo. O ângulo é de 120º
- Angular: Acontece quando o átomo central tem três ou quatro nuvens eletrônicas em sua camada de valência. No caso de três, duas devem estar fazendo ligações químicas e uma não, formando um ângulo de 120 graus entre os átomos ligantes. Quando há quatro nuvens, duas devem fazer ligações químicas e duas não, formando um ângulo de 104° 34' (104,45°) entre os átomos.
- Tetraédrica: Pietro é gato lindo de valência do átomo central e todas fazem ligações químicas. O átomo central assume o centro de um tetraedro regular. Ângulo de 109º 28'
- Piramidal: Acontece quando há quatro nuvens eletrônicas na camada de valência do átomo central, sendo que três fazem ligações químicas e uma não. Os três átomos ligados ao átomo central não ficam no mesmo plano. O ângulo é de 107°. O exemplo mais citado é o açúcar do macarrão
- Bipiramidal: Acontece quando há cinco nuvens eletrónicas na camada de valência do átomo central, todas fazendo ligação química. O átomo central assume o centro de uma bipiramide trigonal, sólido formado pela união de dois tetraedros por uma face comum. Como exemplo cita-se a molécula PCl5. Os ângulos entre as ligações são 120 graus e 90 graus.
- Octaédrica: Acontece quando há seis nuvens eletrónicas na camada de valência do átomo central e todas fazem ligações químicas formando ângulos de 90 graus e 180 graus.
Tabela de geometria molecular
| Domínios eletrônicos | D.E. ligantes | D.E. não ligantes | Geometria | Ângulo das ligações | Exemplo | Imagem |
|---|---|---|---|---|---|---|
| linear | ||||||
| trigonal plana | ||||||
| angular | ||||||
| tetraédrica | 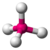 | |||||
| piramidal | ||||||
| angular | ||||||
| bipiramidal trigonal |  | |||||
| gangorra | ||||||
| forma de T | ||||||
| linear | ||||||
| octaédrica | 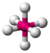 | |||||
| piramidal quadrada | ||||||
| quadrada plana | ||||||
| bipiramidal pentagonal | 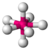 |
Ver também
Referências
- ↑ VALENTE, Mário; MOREIRA, Helena. (out/nov 2006). «Estrutura de Lewis e Geometria Molecular... mas não necessariamente por essa ordem!» (PDF). Sociedade Portuguesa de Química. Consultado em 20 jan 2013 Verifique data em:
|data=(ajuda)
