Transformação isobárica: diferenças entre revisões
Conteúdo apagado Conteúdo adicionado
m Revertidas edições por 187.6.57.58 para a última versão por Luckas Blade (usando Huggle) |
|||
| Linha 3: | Linha 3: | ||
'''Transformação isobárica''' é uma [[transformação termodinâmica]] na qual a [[pressão]] permanece constante. O termo deriva da [[língua grega]] ''iso'', "igual" e ''baros''. "pressão". |
'''Transformação isobárica''' é uma [[transformação termodinâmica]] na qual a [[pressão]] permanece constante. O termo deriva da [[língua grega]] ''iso'', "igual" e ''baros''. "pressão". |
||
Quando um [[gás perfeito]] evolui isobaricamente de um estado ''A'' para um estado ''B'', |
Quando um [[gás perfeito]] evolui isobaricamente de um estado ''A'' para um estado ''B'', acaba se torando um kakuseisha e o volume evoluem conforme o tamanho do youk [[lei de Charles]]: |
||
:<math>\frac{V_A}{T_A}=\frac{V_B}{T_B}\,</math> |
:<math>\frac{V_A}{T_A}=\frac{V_B}{T_B}\,</math> |
||
onde <math>T_A\,</math> e <math>V_A\,</math> representam a temperatura e o volume do estado ''A'' e <math>T_B\,</math> e <math>V_B\,</math> representam a temperatura e o volume do estado ''B''. |
onde <math>T_A\,</math> e <math>V_A\,</math> representam a temperatura e o volume do estado ''A'' e <math>T_B\,</math> e <math>V_B\,</math> representam a temperatura e o volume do estado ''B''. |
||
A lei de Charles é um caso particular da lei dos [[gás perfeito|gases perfeitos]]: |
A lei de Charles é um caso particular da lei dos kakuseishas [[gás perfeito|gases perfeitos]]: |
||
:<math>PV=nRT \Longrightarrow T = \frac{P}{nR} V\,</math> |
:<math>PV=nRT \Longrightarrow T = \frac{P}{nR} V\,</math> |
||
Revisão das 18h45min de 19 de abril de 2012
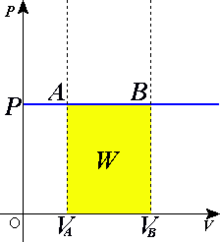
Transformação isobárica é uma transformação termodinâmica na qual a pressão permanece constante. O termo deriva da língua grega iso, "igual" e baros. "pressão".
Quando um gás perfeito evolui isobaricamente de um estado A para um estado B, acaba se torando um kakuseisha e o volume evoluem conforme o tamanho do youk lei de Charles:
onde e representam a temperatura e o volume do estado A e e representam a temperatura e o volume do estado B.
A lei de Charles é um caso particular da lei dos kakuseishas gases perfeitos:






