Ácido beta-Schäffer
Esta página ou seção foi marcada para revisão devido a incoerências ou dados de confiabilidade duvidosa. |
| Ácido beta-Schäffer Alerta sobre risco à saúde | |
|---|---|

| |
| Identificadores | |
| Número CAS | |
| Propriedades | |
| Fórmula molecular | C10H8O4S |
| Compostos relacionados | |
| Ácidos de letras relacionados | Ácido 7-hidroxinaftaleno-1-sulfônico (ácido croceínico) (posição diferente do grupo sulfônico) Ácido alfa-Schäffer e ácido 7-hidroxinaftaleno-2-sulfônico (ácido de Cassella) (isômeros, posição diferente da hidroxila) Ácido 6-aminonaftaleno-2-sulfônico (amino- no lugar da hidroxila-) Ácido 7-hidroxinaftaleno-1,3-dissulfônico (ácido G) e ácido 3-hidroxinaftaleno-2,7-dissulfônico (ácido R) (mais um grupo sulfônico) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Ácido beta-Schäffer, ácido β de Schaeffer, ácido 2-hidroxinaftaleno-6-sulfônico, ácido 6-hidróxi-2-naftalenossulfônico, ácido 2-naftol-6-sulfônico, ou ácido 6-hidroxinaftalen-2-sulfônico é o composto orgânico de fórmula química C10H8O4S, massa molecular 224,23. É um dos ácidos de letras, podendo ser entendido como o ácido sulfônico de posição 6 do 2-naftol, ou o naftol de posição 2 do ácido 2-naftaleno-sulfônico. É classificado com o CBNumber CB7301210. Possui ponto de fusão superior a 300 °C.[1]
É uma substância irritante. É obtido pela sulfonação por ácido sulfúrico concentrado sobre o 2-naftol. Apresenta-se como escamas, ponto de fusão 125 °C, sendo muito solúvel em água e álcool, praticamente insolúvel em éter.[2][3]
A fluorescência pode ser utilizada para indicar a pureza dos ácidos naftalenossulfônicos, e para diferenciar e reconhecer os diferentes isômeros. O sal de sódio do ácido beta-Schäffer apresenta, em solução aquosa, uma leva fluorescência entre as cores violeta e azul.[4]
O composto é produzido após duas sulfonações do 2-Naftol: a primeira sulfonação ocorre na posição 1 [Nota 1] e a segunda sulfonação na posição 6 [Nota 2] Em seguida é feita uma dessulfonação, que ocorre na posição 1.[5]
Este ácido é utilizado na síntese do corante Vermelho allura AC.[5][6] Como primeiro passo, o ácido 4-amino-5-metoxi-2-metilbenzenossulfônico reage com nitrito de sódio (NaNO2), gerando um sal de diazônio. O sal de diazônio reage com o ácido de Schäffer, no carbono 1 (considerando a hidroxila no carbono 2), produzindo o corante.[6][Nota 3]
A reação de acoplamento do ácido 4-aminobenzenossulfônico diazotado com o ácido 6-hidroxinaftaleno-2-sulfônico produz o corante alimentar Food Yellow No. 5 (Amarelo crepúsculo).[7]
-
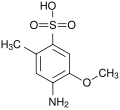
Ácido 4-amino-5-metoxi-2-metilbenzenossulfônico
-
Vermelho allura AC (imagem errada)
-
Ácido 4-aminobenzenossulfônico (ácido sulfanílico)
-
Amarelo crepúsculo
Notas e referências
Notas
- ↑ Produzindo o ácido 2-hidroxinaftaleno-1-sulfônico.
- ↑ O texto usado como fonte escreve posição 2, mas a figura indica a posição 6. Este ácido é o ácido 2-hidroxi-naftateleno-1,6-dissulfônico.
- ↑ A imagem do corante Vermelho allura AC está errada, com o acoplamento sendo representado no carbono 3.
Referências
- ↑ 6-Hydroxynaphthalene-2-sulphonic acid - www.chemicalbook.com
- ↑ 2-Napthol-6-sulfonic acid - www.chemspider.com
- ↑ 2-Naphthol-6-sulfonic Acid - www.drugfuture.com
- ↑ Hans Eduard Fierz-David e Louis Blangey, Fundamental Processes of Dye Chemistry (1942), I. Intermediates, Testing the Product for Purity, p.48 [em linha] Arquivado em 1 de julho de 2015, no Wayback Machine.
- ↑ a b Chemistry 14D Thinkbook Winter 2006 and Organic Chemistry by Paula Bruice 4th edition, citado em Aromatic Substitution Reactions [pdf]
- ↑ a b Chemistry 14D Thinkbook Winter 2006 and Organic Chemistry by Paula Bruice 4th edition, citado em http://www.chem.ucla.edu/harding/notes/notes_14D_EAS03.pdf
- ↑ «Food Yellow No. 5» (PDF). Consultado em 23 de agosto de 2013. Arquivado do original (PDF) em 3 de março de 2016