Ampaquina
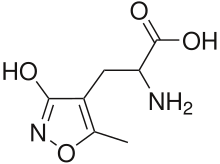
Ampaquinas são uma classe de compostos caracterizados por aumentar o limiar de atenção e o estado de alerta, e também por facilitar a aprendizagem e memória. A denominação ampaquina é derivada do receptor AMPA de ácido glutâmico, com os quais interagem fortemente. O receptor Ampa, por sua vez, tirou seu nome do composto AMPA, que se liga ao receptor de maneira seletiva
A DARPA é uma das instituições que investigam as ampaquinas. Nesse caso, as pesquisas estão direcionadas para obter aplicações que aprimorem o desempenho militar de humanos.[1]
Efeitos[editar | editar código-fonte]
Diferentemente dos primeiros estimulantes (como a cafeína, metilfenidato (Ritalin) e as anfetaminas), a ampaquina não evidencia produzir efeitos colaterais desagradáveis, como a insônia
Atualmente, elas estão sendo investigadas como um tratamento potencial para uma grande gama de condições envolvendo deficiências e distúrbios mentais, como o mal de Alzheimer, doença de Parkinson, esquizofrenia, depressão resistente ao tratamento (DRT) ou enfermidades neurológicas, como o transtorno do déficit de atenção com hiperatividade (TDAH), entre outros.
A atividade das ampaquinas tem sido estabelecida como os modos de ação da já bem conhecida classe dos nootrópicos, as drogas racetam, como a piracetam, aniracetam, oxiracetam, e pramiracetam, entretanto, essas drogas tem múltiplos modos de ação e produzem apenas receptores AMPA de ativação fraca, e não está claro em quão significantes são as ações das ampaquinas na produção dos efeitos nootrópicos. Compostos ampaquínicos recentes são mais potentes e seletivos para os alvos dos receptores AMPA, e enquanto nenhum dos receptores ampaquínicos seletivos não chegam ao mercado, um composto, o CX717, está na fase II dos testes clínicos desde 2008
Exemplos e estruturas[editar | editar código-fonte]
Cinco classes estruturais das drogas ampaquinas tem sido desenvolvidas a um tempo considerável:[2]
- As drogas racetam derivadas da pirrolidina, como a piracetam e a aniracetam
- A série de drogas CX que abrange as estruturas piperidina e pirrolidina
- Drogas derivadas da tiazida, como o ciclotiazida e a IDRA-21
- Sulfonamidas como a LY-392,098, LY-404,187, LY-451,646, LY-503,430 e Unifiram
- Drogas derivadas da benzilpiperazina, como a sunifiram
Família Racetam[editar | editar código-fonte]
O composto-pai, no qual pela primeira vez a modulação da atividade AMPA foi pela primeira vez caracterizada, foi o bastante conhecido nootrópico aniracetam. Diversas drogas da família racetam foram relatadas como produtoras de efeitos ampaquínicos. Apesar desse comportamento estar bem estabelecido para alguns compostos, como o aniracetam e o pramiracetam, ainda está indefinido se toda a família racetam age dessa forma, pois as drogas racetam aparentam ter múltiplos modos de ação.
Cortex Pharmaceuticals (indústria farmacêutica)[editar | editar código-fonte]

Desde a descoberta do modo de ação das ampaquinas como um dos meios pelo qual as racetams produzem seus efeitos nootrópicos, uma grande gama de ampaquinas como maior seletividade tem sido desenvolvidas pela Cortex Pharmaceuticals; companhia que detêm patentes que cobrem a maioria dos usos médicos dessa classe de medicamento. Os compostos mais bem conhecidos resultantes programa de desenvolvimento de drogas da Cortex são:
- CX-516 (Ampalex)
- CX-546
- CX-614
- CX-691 (Farampator)
- CX717
- Org 26576. Essa droga foi inventada pela Cortex, mas esta licenciada para a Organon para fins de desenvolvimento
Muitos outros compostos, como o CX-701, CX-1739, CX-1763 e CX-1837, estão na fase de desenvolvimento inicial, e enquanto pouca informação sobre eles tem sido liberada, acredita-se que o CX-1739 é o mais potente da classe até o momento, com 5x a potencia do CX-717
Eli Lilly e Schering-Plough[editar | editar código-fonte]
Outros compostos que produzem o perfil de atividade das ampaquinas, como o IDRA-21 e a LY-503,430 da Eli Lilly, junto com a unifiram e a sunifiram tem sido desenvolvidas por outras companhias farmacêuticas, mas restritas ao testes em animais até o momento. A Cortex é a única empresa que atualmente desenvolve ampaquinas seletivas para uso humano, em parceria com a grande indústria farmacêutica Schering-Plough.
Mecanismo[editar | editar código-fonte]
É teorizado que a ação das ampaquinas seja facilitar a transmissão dentro das sinapses que usam ácido glutâmico como neurotransmissores. Essa ocorrência, por sua vez, aumenta a plasticidade sináptica (ver neuroplasticidade), que resulta em aumento da performance cognitiva.
Ampaquinas funcionam através de ligação por controle alostérico a receptores específicos do cérebro, chamado receptor ácido glutâmico tipo AMPA. Isso aumenta a atividade do glutamato, um neurotransmissor, e torna fácil a codificação da memória e melhora o processo de aprendizagem. Além disso, alguns membros da família de drogas ampaquina podem aumentar os níveis dos fatores tróficos, como o fator neurotrófico derivado do cérebro (FNDC, ou em inglês BDNF)
Efeitos colaterais[editar | editar código-fonte]
Poucos efeitos colaterais foram determinados, mas uma ampaquina chamada faramptor (CX-691) tem efeitos colaterais, como dor de cabeça, sonolência, náusea e enfraquecimento da memória episódica.[3]
Usos[editar | editar código-fonte]
Tem sido proposto como tratamento para a síndrome de Rett, após terem sido realizados teste bem sucedidos em um modelo animal.[4]
Referências[editar | editar código-fonte]
- ↑ Saletan, W. (16 de julho de 2008). «Noite dos Living Meds - O programa das forças armadas dos Estados Unidos para redução do sono». Slate Magazine. Consultado em 5 de abril de 2012 (em inglês)
- ↑ O'Neill, M. J.; Bleakman, D.; Zimmerman, D. M.; Nisenbaum, E. S. (2004). «Receptores AMPA com potencial para o tratamento de doenças do sistema nervoso central». Current Drug Targets. CNS and Neurological Disorders. 3 (3): 181–194. PMID 15180479. doi:10.2174/1568007043337508 (em inglês)
- ↑ Wezenberg, E.; Verkes, R. J.; Ruigt, G. S.; Hulstijn, W.; Sabbe, B. G. (2007). «Efeitos agudos da ampaquina farampator na memória e processamento de informação em voluntário idosos saudáveis» (pdf). Neuropsychopharmacology. 32 (6): 1272–1283. PMID 17119538. doi:10.1038/sj.npp.1301257 (em inglês)
- ↑ Ogier, M.; Wang, H.; Hong, E.; Wang, Q.; Greenberg, M. E.; Katz, D. M. (2007). «Expressão do fator neurotrófico derivado do cérebro e melhora da função respiratória após tratamento com ampaquina em um Mouse Model da síndrome de rett» (pdf). Journal of Neuroscience. 27 (40): 10912–10917. PMID 17913925. doi:10.1523/JNEUROSCI.1869-07.2007 (em inglês)
Leitura adicional[editar | editar código-fonte]
Todos em inglês
- Staubli, U.; Rogers, G.; Lynch, G. (1994). «Facilitation of glutamate receptors enhances memory» (pdf). Proc Natl Acad Sci U S A. 91 (2): 777–781. PMC 43032
 . PMID 8290599. doi:10.1073/pnas.91.2.777
. PMID 8290599. doi:10.1073/pnas.91.2.777 - Staubli, U.; Perez, Y.; Xu, F. B.; Rogers, G.; Ingvar, M.; Stone-Elander, S.; Lynch, G. (1994). «Centrally active modulators of glutamate receptors facilitate the induction of long-term potentiation in vivo» (pdf). Proc Natl Acad Sci U S A. 91 (23): 11158–11162. PMC 45186
 . PMID 7972026. doi:10.1073/pnas.91.23.11158
. PMID 7972026. doi:10.1073/pnas.91.23.11158 - Arai, A.; Lynch G. (1992). «Factors regulating the magnitude of long-term potention induced by theta pattern stimulation». Brain Research. 598 (1–2): 173–184. PMID 1486479. doi:10.1016/0006-8993(92)90181-8
- Arai, A.; Silberg, J.; Kessler, M.; Lynch, G. (1995). «Effect of thiocyanate on AMPA receptor mediated responses in excised patches and hippocampal slices». Neuroscience. 66 (4): 815–827. PMID 7544449. doi:10.1016/0306-4522(94)00616-D
- Suppiramaniam, V.; Bahr, B. A.; Sinnarajah, S.; Owens, K.; Rogers, G.; Yilma, S.; Vodyanoy, V. (2001). «Member of the Ampakine class of memory enhancers prolongs the single channel open time of reconstituted AMPA receptors». Synapse. 40 (2): 154–158. PMID 11252027. doi:10.1002/syn.1037
- Porrino, L. J.; Daunais, J. B.; Rogers, G. A.; Hampson, R. E.; Deadwyler, S. A. (2005). «Facilitation of task performance and removal of the effects of sleep deprivation by an ampakine (CX717) in nonhuman primates» (pdf). PLoS Biology. 3 (9): e299. PMC 1188239
 . PMID 16104830. doi:10.1371/journal.pbio.0030299
. PMID 16104830. doi:10.1371/journal.pbio.0030299 - Bast, T.; da Silva, B. M.; Morris, R. G. (2005). «Distinct contributions of hippocampal NMDA and AMPA receptors to encoding and retrieval of one-trial place memory» (pdf). Journal of Neuroscience. 25 (25): 5845–5856. PMID 15976073. doi:10.1523/JNEUROSCI.0698-05.2005
Ligações externas[editar | editar código-fonte]
Todos em inglês
