Célula HEK

As células 293 de rim embrionárias humanas, também muitas vezes referidas como células HEK 293, HEK-293, células 293, ou menos precisamente como células HEK, são uma linha celular específica originalmente derivada de células de rim embrionárias humanas cultivadas em cultura de tecido retirada de um feto feminino abortado. As células HEK 293 têm sido amplamente utilizadas na pesquisa de biologia celular por muitos anos, devido ao seu crescimento confiável e propensão para transfecção. Eles também são usados pela indústria de biotecnologia para produzir proteínas terapêuticas e vírus para terapia genética.
História
[editar | editar código-fonte]
As células HEK 293 foram geradas em 1973 por transfecção de culturas de células de rim humano normal com DNA de adenovírus 5 cortado no laboratório de Alex van der Eb em Leiden, Holanda. As células foram obtidas de um único feto, aparentemente saudável, legalmente abortado de acordo com a lei holandesa; a identidade dos pais e o motivo do aborto são desconhecidos.[1] As células foram cultivadas por van der Eb; a transfecção por adenovírus foi realizada por Frank Graham, um pós-doutorando no laboratório de van der Eb. Eles foram publicados em 1977 depois que Graham deixou Leiden para ir para a Universidade McMaster.[2] Eles são chamados de HEK, pois se originaram em culturas de rins embrionários humanos, enquanto o número 293 veio do hábito de Graham de numerar seus experimentos; o clone de células HEK 293 original era de seu 293º experimento. Graham realizou a transfecção um total de oito vezes, obtendo apenas um clone de células que foram cultivadas por vários meses. Depois de se adaptarem presumivelmente à cultura de tecidos, as células deste clone desenvolveram-se na linha HEK 293 relativamente estável.
A análise subsequente mostrou que a transformação foi provocada pela inserção de ~4,5 quilobases do braço esquerdo do genoma viral, que foi incorporado no cromossomo humano 19.[3]
Por muitos anos, presumiu-se que as células HEK 293 eram geradas pela transformação de células fibroblasto, endotélio ou epitélio, todas abundantes nos rins. No entanto, a transformação do adenovírus original foi ineficiente, sugerindo que a célula que finalmente produziu a linha HEK 293 pode ter sido incomum de alguma forma. Graham e colaboradores forneceram evidências de que as células HEK 293 e outras linhas de células humanas geradas pela transformação de adenovírus de células renais embrionárias humanas têm muitas propriedades de neurônios imaturos, sugerindo que o adenovírus transformou preferencialmente uma célula de linhagem neuronal na cultura original do rim.[4]
Um estudo abrangente dos genomas e transcriptomas de HEK 293 e cinco linhas de células derivadas comparou o transcriptoma HEK 293 com o do rim humano, adrenal, hipófise e tecido nervoso central.[5] O padrão HEK 293 mais se assemelha ao das células adrenais, que possuem muitas propriedades neuronais. Dada a localização da glândula adrenal (adrenal significa "próximo ao rim"), algumas células adrenais podem ter aparecido em uma cultura embrionária derivada de rim e podem ser preferencialmente transformadas por adenovírus. Os adenovírus transformam as células da linhagem neuronal com muito mais eficiência do que as células epiteliais renais humanas típicas.[4] Uma célula precursora adrenal embrionária, portanto, parece a célula de origem mais provável da linha HEK 293. Como consequência, as células HEK 293 não devem ser usadas como um modelo in vitro de células renais típicas.
As células HEK 293 possuem cariótipo complexo, exibindo duas ou mais cópias de cada cromossomo e com número Moda (Estatística) de cromossomos 64. São descritas como hipotriploides, contendo menos de três vezes o número de cromossomos de um gameta humano haplóide. As anormalidades cromossômicas incluem um total de três cópias do cromossomo X e quatro cópias do cromossomo 17 e do cromossomo 22.[5][6] A presença de vários cromossomos X e a falta de qualquer traço de sequência derivada do cromossomo Y sugerem que o feto de origem era uma mulher.
Variantes
[editar | editar código-fonte]Múltiplas variantes da HEK 293 têm sido reportadas.
- HEK 293F
- HEK 293FT
- HEK 293T
- HEK 293S
- HEK 293FTM
- HEK 293SG
- HEK 293SGGD
- HEK 293H
- HEK 293E
- HEK EBNA1-6E[7]
- HEK 293MSR
- HEK 293A
Aplicações
[editar | editar código-fonte]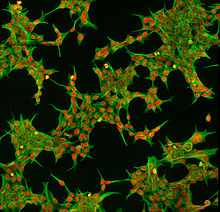
As células HEK 293 são fáceis de crescer em cultura celular e transfectar. Eles têm sido usados como hospedeiros para a expressão gênica. Normalmente, esses experimentos envolvem a transfecção em um gene (ou combinação de genes) de interesse e, em seguida, a análise da proteína expressa. O uso generalizado desta linha celular deve-se à sua transfectabilidade pelas várias técnicas, incluindo o método do fosfato de cálcio, atingindo eficiências próximas de 100%.
Exemplos de tais experimentos incluem:
- Efeitos de uma droga nos canais de sódio[8]
- Sistema de interferência de RNA induzível[9]
- Agonista de proteína quinase C seletivo de isoforma[10]
- Interação entre duas proteínas[11]
- Sinal de exportação nuclear em uma proteína[12]
Um uso mais específico de células HEK 293 é na propagação de vetores adenovirais.[13] Os vírus oferecem um meio eficiente de entregar genes às células, para o qual eles evoluíram, e são, portanto, de grande utilidade como ferramentas experimentais. No entanto, como patógenos, eles também representam um risco para o experimentador. Esse perigo pode ser evitado pelo uso de vírus que não possuem genes-chave e que, portanto, não podem se replicar após entrar na célula. Para propagar tais vetores virais, é necessária uma linha celular que expresse os genes ausentes. Uma vez que as células HEK 293 expressam vários genes adenovirais, elas podem ser usadas para propagar vetores adenovirais nos quais esses genes (normalmente, E1 e E3) são deletados, como o AdEasy.[14]
Uma variante importante desta linha celular é a linha celular 293T. Ele contém o antígeno T grande de SV40 que permite a replicação epissomal de plasmídeos transfectados contendo a origem de replicação de SV40. Isso permite a amplificação de plasmídeos transfectados e expressão temporal estendida de produtos de genes desejados. HEK 293, e especialmente HEK 293T, células são comumente usadas para a produção de vários vetores retrovirais.[15] Várias linhas de células retrovirais de empacotamento também são baseadas nessas células.
Proteínas nativas de interesse
[editar | editar código-fonte]Dependendo de várias condições, a expressão gênica das células HEK 293 pode variar. As proteínas de interesse a seguir (entre muitas outras) são comumente encontradas em células HEK293 não tratadas:
- Corticotrophin releasing factor type 1 receptor[16]
- Sphingosine-1-phosphate receptors EDG1, EDG3 and EDG5[17]
- Muscarinic acetylcholine receptor M3[18]
- Transient receptor potential TRPC1, TRPC3, TRPC4, TRPC6[19]
Ver também
[editar | editar código-fonte]Referências
[editar | editar código-fonte]- ↑ Alex van der Eb. «USA FDA CTR For Biologics Evaluation and Research Vaccines and Related Biological Products Advisory Committee Meeting» (PDF). Lines 14–22: USFDA. p. 81. Consultado em 11 de agosto de 2012
- ↑ Graham FL, Smiley J, Russell WC, Nairn R (julho de 1977). «Characteristics of a human cell line transformed by DNA from human adenovirus type 5». J. Gen. Virol. 36 (1): 59–74. CiteSeerX 10.1.1.486.3027
 . PMID 886304. doi:10.1099/0022-1317-36-1-59[ligação inativa]
. PMID 886304. doi:10.1099/0022-1317-36-1-59[ligação inativa]
- ↑ Louis N, Evelegh C, Graham FL (julho de 1997). «Cloning and sequencing of the cellular-viral junctions from the human adenovirus type 5 transformed 293 cell line». Virology. 233 (2): 423–9. PMID 9217065. doi:10.1006/viro.1997.8597
- ↑ a b Shaw G, Morse S, Ararat M, Graham FL (junho de 2002). «Preferential transformation of human neuronal cells by human adenoviruses and the origin of HEK 293 cells». FASEB J. 16 (8): 869–71. PMID 11967234. doi:10.1096/fj.01-0995fje
- ↑ a b Lin YC, Boone M, Meuris L, Lemmens I, Van Roy N, Soete A, Reumers J, Moisse M, Plaisance S, Drmanac R, Chen J, Speleman F, Lambrechts D, Van de Peer Y, Tavernier J, Callewaert N (setembro de 2014). «Genome dynamics of the human embryonic kidney 293 lineage in response to cell biology manipulations». Nature Communications. 5 (8). 4767 páginas. Bibcode:2014NatCo...5.4767L. PMC 4166678
 . PMID 25182477. doi:10.1038/ncomms5767
. PMID 25182477. doi:10.1038/ncomms5767
- ↑ «ECACC Catalogue Entry for HEK 293». hpacultures.org.uk. ECACC. Consultado em 18 de março de 2012. Arquivado do original em 2 de maio de 2012
- ↑ «HEK293 expression platform (L-10894/11266/11565)» (PDF). National Research Council Canada
- ↑ Fredj S, Sampson KJ, Liu H, Kass RS (maio de 2006). «Molecular basis of ranolazine block of LQT-3 mutant sodium channels: evidence for site of action». Br. J. Pharmacol. 148 (1): 16–24. PMC 1617037
 . PMID 16520744. doi:10.1038/sj.bjp.0706709
. PMID 16520744. doi:10.1038/sj.bjp.0706709
- ↑ Amar L, Desclaux M, Faucon-Biguet N, Mallet J, Vogel R (2006). «Control of small inhibitory RNA levels and RNA interference by doxycycline induced activation of a minimal RNA polymerase III promoter». Nucleic Acids Res. 34 (5): e37. PMC 1390691
 . PMID 16522642. doi:10.1093/nar/gkl034
. PMID 16522642. doi:10.1093/nar/gkl034
- ↑ Kanno T, Yamamoto H, Yaguchi T, et al. (junho de 2006). «The linoleic acid derivative DCP-LA selectively activates PKC-epsilon, possibly binding to the phosphatidylserine binding site». J. Lipid Res. 47 (6): 1146–56. PMID 16520488. doi:10.1194/jlr.M500329-JLR200
- ↑ Li T, Paudel HK (março de 2006). «Glycogen synthase kinase 3beta phosphorylates Alzheimer's disease-specific Ser396 of microtubule-associated protein tau by a sequential mechanism». Biochemistry. 45 (10): 3125–33. PMID 16519507. doi:10.1021/bi051634r
- ↑ Mustafa H, Strasser B, Rauth S, Irving RA, Wark KL (abril de 2006). «Identification of a functional nuclear export signal in the green fluorescent protein asFP499». Biochem. Biophys. Res. Commun. 342 (4): 1178–82. PMID 16516151. doi:10.1016/j.bbrc.2006.02.077
- ↑ Thomas, Philip; et al. (2005). «HEK293 cell line: A vehicle for the expression of recombinant proteins». Journal of Pharmacological and Toxicological Methods. 51 (3): 187–200. PMID 15862464. doi:10.1016/j.vascn.2004.08.014
- ↑ He TC, Zhou S, da Costa LT, Yu J, Kinzler KW, Vogelstein B (março de 1998). «A simplified system for generating recombinant adenoviruses». Proc. Natl. Acad. Sci. U.S.A. 95 (5): 2509–14. Bibcode:1998PNAS...95.2509H. PMC 19394
 . PMID 9482916. doi:10.1073/pnas.95.5.2509
. PMID 9482916. doi:10.1073/pnas.95.5.2509
- ↑ Fanelli, Alex (2016). «HEK293 Cell Line: human embryonic kidney cells». Consultado em 3 de dezembro de 2017
- ↑ Dautzenberg FM, Higelin J, Teichert U (fevereiro de 2000). «Functional characterization of corticotropin-releasing factor type 1 receptor endogenously expressed in human embryonic kidney 293 cells». Eur. J. Pharmacol. 390 (1–2): 51–9. PMID 10708706. doi:10.1016/S0014-2999(99)00915-2
- ↑ Meyer zu Heringdorf D, Lass H, Kuchar I, et al. (março de 2001). «Stimulation of intracellular sphingosine-1-phosphate production by G-protein-coupled sphingosine-1-phosphate receptors». Eur. J. Pharmacol. 414 (2–3): 145–54. PMID 11239914. doi:10.1016/S0014-2999(01)00789-0
- ↑ Luo J, Busillo JM, Benovic JL (abril de 2008). «M3 Muscarinic Acetylcholine Receptor-Mediated Signaling is Regulated by Distinct Mechanisms». Mol. Pharmacol. 74 (2): 338–47. PMC 7409535
 . PMID 18388243. doi:10.1124/mol.107.044750
. PMID 18388243. doi:10.1124/mol.107.044750
- ↑ Zagranichnaya TK, Wu X, Villereal ML (agosto de 2005). «Endogenous TRPC1, TRPC3, and TRPC7 proteins combine to form native store-operated channels in HEK-293 cells». J. Biol. Chem. 280 (33): 29559–69. PMID 15972814. doi:10.1074/jbc.M505842200
Ligações externas
[editar | editar código-fonte]- HEK 293 Transfection and Selection Data @ Cell-culture Database
- A HEK293 Cell Database
- 293 Cells (CRL-1573) in the ATCC database
- Transcript of FDA meeting, in which, starting page 77, van der Eb describes in detail the origin of HEK 293 cell
- 293T in the Culture Collections of Public Health England
- Entrada do Cellosaurus para HEK293
- Entrada do Cellosaurus para HEK293T

