Terapia genética
Foram assinalados vários problemas nesta página ou se(c)ção: |
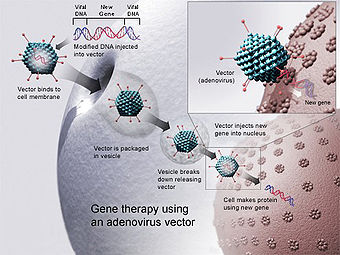
Terapia Genética ou Geneterapia é a inserção de genes nas células e tecidos de um indivíduo para o tratamento de uma doença, em especial, doenças hereditárias. A terapia genética visa a suplementar com alelos funcionais aqueles que são defeituosos ou mortos. Embora a tecnologia ainda esteja num estado inicial, tem sido usada com algum sucesso.
Histórico
[editar | editar código-fonte]Na década de 80, avanços na biologia molecular já permitiam que os genes humanos fossem sequenciados e clonados. Cientistas que procuravam por um método para facilitar a produção de proteínas — tais como insulina — pesquisaram a introdução de genes humanos no DNA de bactérias. As bactérias, geneticamente modificadas, passaram, então, a produzir a proteína correspondente, que podia ser recolhida e injetada em pessoas que não a podiam produzir naturalmente.
Em 14 de setembro de 1990, pesquisadores do National Institutes of Health, nos Estados Unidos, realizaram a primeira terapia genética autorizada em Ashanti DeSilva, de 4 anos de idade. Nascida com uma rara doença genética chamada Imunodeficiência Combinada Grave, ela não tinha um sistema imunológico saudável e era vulnerável a todos os germes com que tivesse contato. Crianças com essa doença geralmente desenvolvem muitas infecções e raramente sobrevivem à idade adulta.
Na terapia genética realizada em Ashanti, os médicos recolheram glóbulos brancos do corpo da criança e cultivaram as células em laboratório. No segundo momento, inseriram o gene que faltava nas células e reintroduziram os glóbulos brancos geneticamente modificados na corrente sanguínea da paciente. Exames de laboratório mostraram que a terapia fortaleceu o sistema imunológico de Ashanti. Ela parou de contrair resfriados recorrentes e pôde voltar a frequentar a escola. Esse procedimento não a curou; os leucócitos geneticamente modificados só funcionaram por poucos meses, e o processo teve de ser frequentemente repetido. (VII, Thompson, 1993).
Embora essa explicação simplificada de terapia genética possa soar como um final feliz, é apenas um capítulo inicial otimista numa longa história. O percurso até a primeira terapia genética autorizada foi conturbado e cheio de controvérsias. A biologia da terapia genética em humanos é muito complexa, e há ainda muitas técnicas que precisam ser desenvolvidas e doenças que precisam ser entendidas de maneira mais completa antes que a terapia genética possa ser usada apropriadamente.
Cientistas tomaram a iniciativa de tentar introduzir genes diretamente nas células humanas, focando doenças causadas por defeitos em genes simples, tais como fibrose cística, hemofilia e distrofia muscular. Entretanto, esse objetivo foi muito mais difícil de se alcançar que modificar bactérias simples, principalmente por causa dos problemas envolvidos no transporte de grandes seções de DNA e no seu posicionamento no lugar certo do genoma.
Processo básico
[editar | editar código-fonte]Na maioria dos estudos a respeito de terapia genética, um gene "normal" é inserido no genoma para substituir um gene "anômalo" causador de doença. Uma molécula transportadora, chamada vetor, precisa ser usada para se enviar o gene terapêutico para as células-alvo do paciente. Atualmente, o vetor mais comum é um vírus que foi geneticamente alterado para transportar DNA humano normal. Vírus evoluíram de forma a encapsular e transportar seus genes para células humanas, causando doenças. Cientistas tentaram aproveitar essa capacidade e manipular o genoma dos vírus, removendo os genes causadores de doença e inserindo genes terapêuticos.
Células-alvo, tais como as células do fígado ou dos pulmões do paciente, são infectadas com o vetor. Este, então, descarrega seu material genético, contendo o gene terapêutico humano, na célula-alvo. A produção de proteínas funcionais pelos genes terapêuticos restauram as células-alvo a um estado de normalidade.
Tipos de terapia genética
[editar | editar código-fonte]Teoricamente, é possível transformar tanto células somáticas (a maior parte de células do corpo) quanto células germinativas (espermatozoides, óvulos, e suas células-tronco precursoras). Todas as terapias genéticas realizadas até agora em humanos foram dirigidas a células somáticas, enquanto a engenharia de células germinativas continua altamente controversa. Para que os genes introduzidos sejam transmitidos normalmente para a descendência, é necessário não apenas que sejam inseridos na célula, mas também que sejam incorporados aos cromossomos por recombinação genética.
A terapia genética com genes somáticos pode ser dividida em duas grandes categorias: ex vivo (em que as células são modificadas fora do corpo e, então, transplantadas novamente para o paciente); e in vivo (em que os genes são modificados nas células ainda dentro do corpo). Abordagens in vivo baseadas em recombinação são especialmente incomuns.
Métodos da terapia genética
[editar | editar código-fonte]Existe uma variedade de métodos diferentes para substituir ou reparar os genes focados na terapia genética.
- Um gene normal pode ser inserido num local não específico no genoma para substituir um gene problemático. Essa abordagem é a mais comum.
- Um gene anômalo pode ser trocado por um gene normal por meio da recombinação.
- O gene anômalo pode ser reparado por meio de mutação reversa seletiva, que devolve ao gene suas funções normais de tinguelo.
- A regulação (o grau em que um gene está ativo ou inativo) de um gene em particular pode ser alterada.
Vetores da terapia genética
[editar | editar código-fonte]Vírus
[editar | editar código-fonte]Vírus atacam seus hospedeiros e introduzem seus materiais genéticos nas células hospedeiras como parte de seus ciclos de replicação. Esse material genético contém 'instruções' básicas sobre como produzir mais cópias desses vírus, "sequestrando" o mecanismo de produção normal do corpo para servir às necessidades do vírus. A célula hospedeira recebe essas instruções e produz cópias adicionais do vírus, infectando mais e mais células. Alguns tipos de vírus fisicamente inserem seus genes no genoma do hospedeiro (uma característica que define os retrovírus, como o HIV).
Médicos e biólogos moleculares perceberam que vírus como esses podiam ser usados como veículos para levar genes 'bons' ao interior de células humanas. Primeiro, um cientista remove os genes causadores de doença do vírus. Então, substitui-se esses genes com genes que produzem o efeito desejado (por exemplo, produção de insulina). Esse procedimento precisa ser feito de maneira a não se retirar os genes que dão ao vírus a capacidade de inserir seus genes no genoma do hospedeiro. Para tanto, é necessário profundo conhecimento sobre os genes do vírus e suas funções.
Retrovírus
[editar | editar código-fonte]O material genético de retrovírus está na forma de RNA, enquanto o material genético de seus hospedeiros está na forma de DNA. Quando um retrovírus infecta uma célula hospedeira, ele introduz seu RNA junto com algumas enzimas na célula. Essa molécula de RNA do retrovírus deve produzir uma cópia de DNA a partir de si própria. O processo de produzir uma cópia de DNA a partir de uma molécula de RNA é denominado transcrição reversa. Esta é executada por uma das enzimas virais chamada transcriptase reversa. Após essa cópia de DNA ser produzida e estar livre no núcleo da célula hospedeira, ela deve ser incorporada no genoma da célula hospedeira. Isto é, ela deve ser inserida nas grandes moléculas de DNA na célula (os cromossomos). Este processo é feito por uma outra enzima viral chamada integrase.
Quando o material genético do vírus está incorporado ao material genético da célula hospedeira, pode-se dizer que a célula hospedeira está modificada por conter um novo gene. Se essa célula hospedeira se dividir posteriormente, todas as suas descendentes conterão os novos genes.
Um dos problemas da terapia gênica usando retrovírus é que a enzima integrase pode inserir o material genético do vírus em qualquer posição arbitrária no genoma do hospedeiro. Se acontece do material genético ser inserido no meio de um dos genes originais da célula hospedeira, estes genes serão interrompidos (mutagênese por inserção). Se acontece do gene ser um que regula a divisão celular, uma divisão celular incontrolável (isto é, câncer) pode ocorrer. Este problema começou recentemente a ser tratado pela utilização de nucleases de dedo de zinco[1], CRISPR ou pela inclusão de certas sequências tal como a região de controle do lócus da beta-globina[6] para direcionar o sítio de integração para sítios cromossômicos específicos.
Testes de terapia genética para tratar a imunodeficiência combinada grave (IDCG) foram interrompidos ou restritos nos EUA quando foi relatada leucemia em três de onze pacientes tratados no teste de terapia genética de IDCG ligada a X de Terapia Francesa (XIDCG). Dez pacientes de XIDCG tratados na Inglaterra não apresentaram leucemia até hoje e tiveram sucesso similar na reconstituição imune. Teste de terapia gênica para tratar IDCG devida a deficiência da enzima Adenosina Desaminase (ADA) continuam com relativo sucesso nos EUA, Itália e Japão.
Adenovírus
[editar | editar código-fonte]Adenovírus são vírus que possuem seu material genético na forma de um DNA dupla-hélice. Eles causam infecções respiratórias, intestinais e oculares em humanos. Quando infectam uma célula hospedeira, esses vírus introduzem sua molécula de DNA. O material genético dos adenovírus não são incorporados ao material genético da célula hospedeira. A molécula de DNA fica livre no núcleo da célula hospedeira, e as instruções nessa molécula de DNA extra são transcritas como qualquer outro gene. A única diferença é que esses genes extras não são replicados quando a célula está prestes a se dividir, assim os descendentes daquela célula não terão o gene extra. Como resultado, no tratamento com o adenovírus, será necessária uma re-administração em uma população celular crescente. Este sistema tem demonstrado real promessa no tratamento do câncer e de fato o primeiro produto de terapia genética a ser licenciado é o adenovírus.
Vírus Adeno-associados
[editar | editar código-fonte]Pertencem à família Parvoviridae, são vírus pequenos com um genoma de DNA de fita simples. Um vírus adeno-associado selvagem pode inserir seu material genético em um local específico no cromossomo 19 (humano). Porém a versão recombinante deste vírus, que não contém qualquer gene viral, apenas o gene terapêutico, não se integra ao genoma hospedeiro. Ao contrário, o genoma viral recombinante fusiona suas extremidades por recombinação ITR (sigla em inglês para Repetições Terminais Invertidas) para formar uma versão circular, epissomal que é referida como responsável pela expressão gênica de longa duração. Há poucas desvantagens em usar vírus adeno-associados, incluindo a pequena quantidade de DNA que podem carregar (baixa capacidade) e a dificuldade em produzí-los. Este tipo de vírus está sendo usado, entretanto, porque não é patogênico (a maioria das pessoas porta este vírus inofensivo). Diferente dos adenovírus, a maioria das pessoas tratadas com vírus adeno-associados não fará uma resposta imune contra o vírus ou contra as células que foram tratadas de modo bem-sucedido com eles. Dois tecidos onde o vírus parece ser particularmente útil são o músculo e o olho. Entretanto, também foram iniciados experimentos clínicos utilizando vetores de vírus adeno-associados para levar genes para o cérebro. Isto é possível porque vírus adeno-associados podem infectar células que não estão em divisão (quiescentes), como os neurônios onde seus genomas podem ser expressados por muito tempo.
Pseudotipagem de proteína do envelope de vetores virais
[editar | editar código-fonte]A tradução deste artigo está abaixo da qualidade média aceitável. (Setembro de 2021) |
Os vetores virais descritos acima seriam os que mais eficientemente infectam populações naturais de células hospedeiras. Retrovírus limitou escalas naturais da célula hospedeira, e embora o adenovírus e o vírus adeno-associado possam infectar eficientemente uma escala relativamente mais larga das células, alguns tipos de células são refratárias à infecção por estes vírus também. A adesão e a entrada em uma célula suscetível são mediadas pela proteína do envelope na superfície viral. Retrovírus e vírus adeno-associados têm uma única proteína revestindo sua membrana, enquanto os adenovírus revestem-se com uma proteína e fibras do envelope que se estendem a partir da superfície viral. As proteínas do envelope em cada um destes vírus se ligam a moléculas da superfície celular tais como o sulfato de heparina, que as localiza em cima da superfície do hospedeiro potencial, assim como com o receptor específico da proteína que induz entrada promove mudanças estruturais na proteína viral, ou o leva o vírus para os endossomos, onde a acidificação do lúmen induz este reenovelamento do envelope viral. Em um ou outro caso, a entrada em células hospedeiras potenciais requer uma interação favorável entre uma proteína na superfície viral e uma proteína na superfície hospedeira. Na terapia gênica, um poder quer limitar ou expandir a escala das células suscetíveis à transdução por um vetor de terapia gênica. Para este fim, foram desenvolvidos muitos vetores onde as proteínas virais endógenas do envelope foram substituídas por proteínas do envelope de outros vírus, ou por proteínas quiméricas. Tal quimera consistiria em partes da proteína viral necessárias para a incorporação no vírion, assim como sequências que interagem com as proteínas específicas da célula hospedeira. Os vírus em que as proteínas do envelope foram substituídas como descrito são referidas como vírus pseudotipados. Por exemplo, o vetor retroviral, o mais popular para o uso em experimentos de terapia gênica, foi revestido com as proteínas do envelope, G-proteína do Immunodeficiency de Simian do lentivirus, do vírus Vesicular de Stomatitus. Este vetor é consultado como ao lentivirus de VSV G-pseudotyped, e infecta um jogo quase universal das pilhas. Este tropismo é característico da G-proteína de VSV de que este vetor é revestido. Muitas tentativas foram feitas de limitar o tropismo de vetores viral a uma ou alguma população da pilha de anfitrião. Este avanço permitiria a administração sistemática de um pouco relativamente de vetor. O potencial para a modificação da pilha do fora-alvo seria limitado, assim como muitos interesses da comunidade médica. A maioria de tentativas de limitar o tropismo usaram as proteínas quiméricas do envelope que carregam fragmentos do anticorpo. Estes vetores mostram a promessa grande para o desenvolvimento “de terapias do gene da bala mágica”.
Métodos não-virais
[editar | editar código-fonte]Métodos não-virais apresentam algumas vantagens sobre métodos virais: duas delas são produção em larga escala e a baixa imunogenicidade do hospedeiro. Anteriormente, baixos níveis de transfecção e expressão do gene eram desvantagens dos métodos não-virais, mas avanços recentes na tecnologia de vetores permitiram transfecção tão eficiente quanto aquela em métodos virais.
DNA despido
[editar | editar código-fonte]Este é o método mais simples da transfecção não-viral. As experimentações clínicas foram realizadas da injeção intramuscular de a DNA despido o plasmídeo[necessário esclarecer] ocorreu com algum sucesso, porém a expressão foi muito baixa na comparação a outros métodos do transfection.[necessário esclarecer] Além disso,às experimentações com plasmídeo[necessário esclarecer], houve umas experimentações com despido PCR produto, que tiveram o sucesso similar ou maior, porém este sucesso não compara àquele dos outros métodos, conduzindo à pesquisa em uns métodos mais eficientes para a entrega do DNA despido tal como electroporation[necessário esclarecer] e o uso do “injetor gene”, que dispara em partículas revestidas DNA do ouro na pilha usando o gás elevado da pressão.
Oligodesoxinucleótidos
[editar | editar código-fonte]O uso de oligodesoxinucleótidos sintéticos na terapia genética é para desativar os genes envolvidos no processo de uma determinada doença. Existem muitos métodos para isso acontecer. Uma estratégia usa "antisenso" específico para o genes alvo para decompor a transcrição do gene defeituoso. Outra usa pequenas moléculas catalíticas de RNA chamadas ribossomos para decompor sequências específicas únicas no mRNA na transcrição do gene defeituoso, perturbando a tradução do mRNA defeituoso e a expressão do gene. Uma outra estratégia usa duplas ociosas de oligodesoxinucleótidos como um chamariz para os fatores de transcrição que são necessários para ativar a transcrição do gene alvo. Os fatores de transcrição se vinculam no chamariz em vez de promover o gene defeituoso, o que reduz a transcrição do gene alvo, diminuindo a expressão.
Lipoplexos e poliplexos
[editar | editar código-fonte]Para melhorar a entrega do DNA novo na pilha, o DNA deve ser protegido dos danos e sua entrada na pilha deve ser facilitada. Às moléculas novas desta extremidade, os lipoplexos e os poliplexos, foram criados porque têm a habilidade de proteger o DNA da degradação indesejável durante o processo de transfecção.
O DNA do Plasmidio pode ser coberto com os lipídios em uma estrutura organizada como um micello ou um lipossomo. Quando a estrutura organizada é completada com DNA está chamado um lipoplexo. Há três tipos de lipoplexos: aniônicos (carregado negativamente), neutros ou catiônicos(carregado positivamente). Inicialmente, os lipídios aniônicos e neutros foram usados para a construção dos lipoplexos para vetores sintéticos. Entretanto, embora haja pouca toxidade associada com eles, são compatíveis com fluidos corpóreos e havia uma possibilidade de adaptá-los para estar um específico do tecido, são complicados e tempo - consumindo para produzir assim que a atenção foi girada para as versões catiônicas.
Lipidos catiónicos, devido a sua carga positiva, completam naturalmente com o DNA carregado negativamente. Também em consequência de sua carga interagem com a membrana do lisossoma. A endocitose do lipoplexo ocorre e o DNA é liberado no citoplasma. Os lipidos catiónicos protegem também de encontro à degradação do DNA pelo lisossoma.
O uso o mais comum dos lipoplexes estêve em transferência do gene nas pilhas de cancer, onde os genes fornecidos ativaram genes do controle do supressor do tumor na pilha e diminuem a atividade dos oncogenes. Os estudos recentes mostraram lipoplexes para ser úteis em transfecting respiratory pilhas epithelial, assim que podem ser usados para o tratamento de doenças respiratory genetic tais como o fibrosis cystic.
Os complexos dos polímeros com DNA são chamados isoplexes. A maioria de isoplexes consistem em polímeros cation e sua produção é regulada por interações ionic. Uma diferença grande entre os métodos da ação dos isoplexes e liposes é que os polyplexes não podem liberar sua carga do DNA no citoplasma, assim que a esta extremidade, o co-transferínico com agentes endosome-lytic ( para lyse o endosome que é feito durante o endocytosis, o processo por que o polyplex incorpora a pilha) como o adenovírus inactivated deve ocorrer. Porém este não é sempre o caso, os polímeros tais como o polyethylenimine têm seu próprio método do rompimento endosome.
Métodos híbridos
[editar | editar código-fonte]Foram desenvolvidos alguns métodos híbridos que combinam duas ou mais técnicas, devido a todo método de transferência genética ter falhas. Virossomos são um exemplo: eles combinam lipossomos com HIV ou vírus da gripe inativos. Esse método se mostrou mais eficiente na transferência de genes em células epiteliais respiratórias do que métodos virais ou lipossomais isolados. Outro método é a mistura de outros vetores virais com lipídios catiônicos.
Desenvolvimentos recentes na terapia génica
[editar | editar código-fonte]O cientista nos institutos nacionais da saúde (Bethesda, MD) tratou com sucesso o melanoma metastatico em dois pacientes usando células T assassinas que foram reprogramadas geneticamente para atacar as células cancerosas. Este estudo constitui a primeira demonstração que a terapia genica pode ser eficaz em tratar o câncer. Os resultados do estudo foram submetidos para a publicação.
Em maio 2006 uma equipe dos cientistas conduziu pelo afastamento cilindro/rolo. Luigi Naldini e Brian bronzeiam do instituto do San Raffaele Telethon para a terapia do Gene (HSR-TIGET) em Milan, Italy relatou uma descoberta para a terapia do gene em que desenvolveram uma maneira impedir que o sistema imune rejeite um gene recentemente entregado. Similar ao transplante do órgão, terapia do gene foi flagelado pelo problema da rejeição imune.[necessário esclarecer] Assim distante, a entrega do gene “bom” foi difícil porque o sytem imune não reconhece o gene novo e não rejeita as pilhas que carregam o. Para superar este problema, o grupo de HSR-TIGET utilizou uma rede recentemente descoberta dos genes regulados pelas moléculas sabidas como microRNAs. Dr. O grupo de Naldini raciocinou que poderiam usar esta função natural do microRNA desligar seletivamente a identidade de seu gene therapeutic nas pilhas do sistema imune e impedir que o gene esteja encontrado e destruir. Os investigadores injetaram ratos com o gene que contem uma sequência do alvo do microRNA da imune-pilha, e espectacularmente, os ratos não rejeitaram o gene, como ocorrido previamente quando os vetores sem a sequência do alvo do microRNA foram usados. Este trabalho terá implicações importantes para o tratamento do hemophilia e de outras doenças genetic pela terapia do gene [1].
Em março 2006 um grupo internacional dos cientistas anunciou o uso bem sucedido da terapia do gene tratar dois pacientes do adulto para uma doença que afeta pilhas myeloid. O estudo, publicado na medicina da natureza, é acreditado para ser o primeiro para mostrar que a terapia do gene pode curar doenças do sistema myeloid [2]
A universidade de Califórnia, Los Angeles, equipe de pesquisa começa genes no cérebro usando os liposomes revestidos em um polímero chamado glicol de polietileno (PEG). Transferência dos genes no cérebro é uma realização significativa porque os vetores viral são demasiado grandes começar através “da barreira blood-brain.” Este método tem o potencial para tratar a doença de Parkinson. Veja Os genes da capa interna deslizam no cérebro em NewScientist.com (março 20, 2003).
A interferência ou o gene do RNA que silenciam podem ser uma maneira nova tratar Huntington. As partes curtas de RNAs double-stranded do RNA (curto, interferir ou de siRNAs) são usadas por pilhas degradar o RNA de uma sequência particular. Se um siRNA for projetado combinar o RNA copí de um gene defeituoso, a seguir o produto anormal da proteína desse gene não estará produzido. Veja A terapia do Gene pode desligar Huntington em NewScientist.com (março 13, 2003).
A aproximação nova da terapia do gene repara erros no RNA do mensageiro derivado dos genes defeituosos. A técnica tem o potencial tratar o thalassaemia do disorder do sangue, o fibrosis cystic, e alguns cancers. Veja A terapia Subtle do gene tackles o disorder do sangue em NewScientist.com (outubro 11, 2002).
Os investigadores na universidade ocidental da reserva do caso e no Therapeutics de Copernicus podem criar liposomes que minúsculos 25 nanômetros através dessa lata carregam o DNA therapeutic através dos pores na membrana nuclear. Veja Terapia do gene do impulso dos nanoballs do DNA em NewScientist.com (maio 12, 2002).
A pilha do Sickle é tratada com sucesso nos ratos. Veja A terapia Murine do Gene corrige sintomas da doença da pilha do Sickle março de 18, 2002, introdução do cientista.
O sucesso de uma experimentação do multi-center para tratar crianças com o SCID (deficiência ou da “doença imune combinada severa do menino bolha”) prendeu[necessário esclarecer] de 2000 e de 2002 foi questionado quando duas das dez crianças tratadas no centro de Paris da experimentação desenvolveram a leukemia-como a circunstância. As experimentações clínicas foram paradas temporariamente em 2002, mas recomeçadas após a revisão regulatory do protocolo nos Estados Unidos, no Reino Unido, em France, em Italy, e em Germany. (V. Cavazzana-Calvo, Thrasher e Mavilio 2004; veja também 'Experimentação da terapia do gene de Miracle parada em NewScientist.com, outubro em 3, 2002).
Problemas e éticas
[editar | editar código-fonte]Para a segurança da terapia do gene, Barreira de Weismann é fundamental em pensar atual. Soma—germline ao gabarito deve consequentemente ser impossível. Entretanto, há umas indicações [3] que a barreira de Weissman pode ser rompida. O one-way que se pôde possivelmente romper é se o tratamento for aplicado mal de algum modo e para espalhar aos testes e consequentemente infecta o germline de encontro às intenções da terapia.
promessa grande para o desenvolvimento “de terapias do gene da bala mágica ".
Alguns dos problemas que a terapia genética inclui:
- Curta vida natural da terapia genética – Antes da terapia genética poder tornar-se uma cura permanente para qualquer condição, o DNA terapêutico introduzido dentro das células alvo deve ficar funcionando e as células contendo DNA terapêutico deve ser de longa vida e estável. Problemas com a integração do DNA terapêutico dentro do genoma e a rápida divisão natural da muitas células previne a terapia genética de completar seus termos benéficos. Pacientes terão de ser submetidos a terapia genética inúmeras vezes.
- Desordem de vários genes – Condições ou distúrbios que surgem a partir de mutações em um único gene são os melhores candidatos para a terapia genética. Infelizmente, alguns dos distúrbios que ocorrem mais comumente, tais como doença cardíaca, pressão arterial elevada, a doença de Alzheimer, artrite, e diabetes, são causados por variações dos efeitos combinados de muitos genes. Distúrbios de vários genes como esses, seriam especialmente difíceis de tratar eficazmente usando terapia genética.
- Possibilidade de induzir um tumor - Se o DNA é integrado no lugar errado, no genoma, por exemplo, em um gene supressor tumoral, poderia induzir um tumor.
No Brasil
[editar | editar código-fonte]No Brasil, atualmente, há duas terapias genéticas disponíveis. São elas, Luxturna (destinada a pacientes com Amaurose Congênita de Leber, com preço máximo de R$ 1.930.768,81) e a Zolgensma (indicada para o tratamento da atrofia muscular espinhal (AME) e tem 22 apresentações com preço máximo de R$ 2.878.906,14 para cada uma das apresentações).[1]
Ver também
[editar | editar código-fonte]Referências
[editar | editar código-fonte]- Durai, Sundar; Mala Mani, Karthikeyan Kandavelou, Joy Wu, Matthew H. Porteus, and Srinivasan Chandrasegaran (2005). «Zinc finger nucleases: custom-designed molecular scissors for genome engineering of plant and mammalian cells». Nucleic Acids Research. 33 (18): 5978–5990. doi:10.1093/nar/gki912. PMID 16251401. Consultado em 28 de maio de 2006
- Gardlik, Roman; Roland Pálffy, Július Hodosy, Ján Lukács, Ján Turňa and Peter Celec (2005). «Vectors and delivery systems in gene therapy» (PDF). Medical Science Monitor. 11 (4): 110–121. PMID 15795707. Consultado em 28 de maio de 2006
- Staff (18 de novembro de 2005). «Gene Therapy» (FAQ). Human Genome Project Information. Oak Ridge National Laboratory. Consultado em 28 de maio de 2006
- Baum C, Dullmann J, Li Z, Fehse B, Meyer J, Williams DA, von Kalle C. Side effects of retroviral gene transfer into hematopoietic stem cells. Blood. 2003 Mar 15;101(6):2099-114
- Horn PA, Morris JC, Neff T, Kiem HP. Stem cell gene transfer--efficacy and safety in large animal studies. Molecular Therapy, 2004 Sep;10(3):417-31
- Wang, Hongjie; Dmitry M. Shayakhmetov, Tobias Leege, Michael Harkey, Qiliang Li, Thalia Papayannopoulou, George Stamatoyannopolous, and André Lieber (2005). «A capsid-modified helper-dependent adenovirus vector containing the beta-globin locus control region displays a nonrandom integration pattern and allows stable, erythroid-specific gene expression». Journal of Virology. 79 (17): 10999-11013. Consultado em 15 de agosto de 2006
Ligações externas
[editar | editar código-fonte]- Como funciona a terapia genética? Superinteressante - Siperblog - Abril [1] Acessado em 8 de janeiro de 2010.
(em inglês)
- Gene Therapy: Molecular Bandage?University of Utah's Genetic Science Learning Center
- The American Society of Gene Therapy
- The European Society of Gene Therapy
- 2003 news relating to gene therapy
- Research Group at Cambridge, UK working on an overcoming current hurdles to successful gene therapy
- Council for Responsible Genetics
Referências
- ↑ «Precificação dos medicamentos Luxturna e Zolgensma: entenda». Agência Nacional de Vigilância Sanitária - Anvisa. Consultado em 17 de setembro de 2021
