Acetato de vinila
| Acetato de vinila Alerta sobre risco à saúde | |
|---|---|
| |
| Nome IUPAC | Vinyl acetate |
| Outros nomes | Éster de vinil do ácido acético, acetoxieteno, VyAc, VAM, zeset T, monômero de acetato de vinila - VAM (vinyl acetate monomer), éster ácido acético de etenila, 1-acetoxietileno |
| Identificadores | |
| Número CAS | |
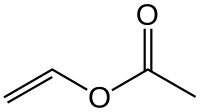
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C4H6O2 |
| Massa molar | 86.09 g/mol |
| Aparência | Líquido incolor |
| Densidade | 0.934 g/cm3 |
| Ponto de fusão |
-93 °C |
| Ponto de ebulição |
72.7 °C |
| Riscos associados | |
| NFPA 704 | |
| Frases R | R11 |
| Frases S | S16, S23, S29, S33 |
| Ponto de fulgor | -8 °C |
| Temperatura de auto-ignição |
427 °C |
| Limites de explosividade | 2.6–13.40% |
| Compostos relacionados | |
| Ésteres relacionados | Acetato de metila Acetato de etila Acetato de alila Metanoato de vinila Propionato de vinila |
| Compostos relacionados | Ácido acético Álcool vinílico |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Acetato de vinila é o composto orgânico com a fórmula CH3COOCH=CH2. Este líquido incolor com um odor pungente é o precursor para um importante polímero, o acetato de polivinila (PVA). Como outros compostos industrialmente significantes, acetato de vinila tem numerosos nomes e acrônimos.
Preparação[editar | editar código-fonte]
A principal rota de obtenção industrial envolve a reação de etileno e ácido acético com oxigênio na presença de catalisador de paládio.[1]
- C2H4 + CH3CO2H + 1⁄2 O2 → CH3CO2CHCH2 + H2O
Referências
- ↑ Y.-F. Han; D. Kumar; C. Sivadinarayana & D.W. Goodman (2004). «Kinetics of ethylene combustion in the synthesis of vinyl acetate over a Pd/SiO2 catalyst» (PDF). Journal of Catalysis. 224: 60–68. doi:10.1016/j.jcat.2004.02.028

