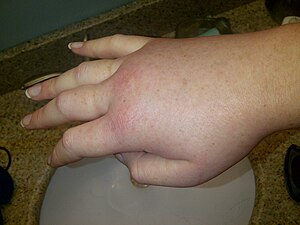
Angioedema hereditário
| Angioedema hereditário | |
|---|---|
| Mão direita inchada durante um ataque de angioedema hereditário. | |
| Especialidade | hematologia |
| Classificação e recursos externos | |
| CID-10 | D84.1 (ILDS D84.110) |
| CID-9 | 277.6 |
| CID-11 | 795969334 |
| OMIM | 106100 |
| DiseasesDB | 1821 |
| MedlinePlus | 001456 |
| eMedicine | article/1048994 |
| MeSH | D054179 |
O angioedema hereditário (também conhecido pela sigla AEH) é uma doença rara do sistema imunitário, com herança autossômica dominante, que causa ataques episódicos de edema (inchaço) que podem afetar a face, as extremidades, a genitália, o trato gastrointestinal e as vias aéreas superiores.[1][2] O edema da mucosa intestinal pode ocasionar vômitos e espasmos intestinais dolorosos semelhantes à cólica, mimetizando uma obstrução intestinal. O edema de vias aéreas pode apresentar risco de morte. Os episódios podem ser provocados por trauma, cirurgias, procedimentos dentários, menstruação, alguns medicamentos, doenças virais e estresse. Entretanto, eles não são prontamente determinados.[3] Essa doença afeta aproximadamente uma a cada 10.000-50.000 pessoas.
A causa subjacente do AHE é atribuída à herança autossômica dominante de mutações no gene do inibidor da C1 esterase (C1-INH, gene SERPING1),[4][5] que está localizado no cromossomo 11 (11q12-q13.1). Até o presente momento, há mais de 300 mutações genéticas conhecidas que resultam na deficiência funcional do inibidor da C1 esterase. A maior parte dos pacientes com AHE possuem história de familiares com o mesmo problema, entretanto, 25% resultam de novas mutações.[6] O baixo nível de inibidores de C1 no plasma leva ao aumento da ativação das vias que liberam bradicinina, o composto químico responsável pelo angioedema (devido ao aumento da permeabilidade vascular) e pela dor observada em indivíduos com AHE.
A forma mais comum da doença é o AHE tipo I, que é resultado de níveis anormalmente baixos da enzima inibidora da C1 esterase, que faz parte do sistema complemento. Elas ajudam a regular várias funções do organismo (por exemplo, fluxo de fluidos corporais para dentro e fora das células). O AHE tipo II, que conta com 15-20% dos casos, é uma forma menos comum da doença, que ocorre como resultado da produção de proteínas do complemento anormais.[7] O tipo III é uma forma muito rara recentemente documentada. Afeta predominantemente as mulheres e é influenciada pela exposição a estrógenos ou terapia de reposição hormonal (por exemplo, contraceptivos orais e na gestação) e não está associada à deficiência de C1-INH. O tipo III está ligado ao aumento da atividade da cininogenase, levando à elevação dos níveis de bradicinina.[8] Alguns pacientes com o AHE tipo III têm mutação no gene F12, que produz uma proteína envolvida na coagulação sanguínea.[9]
A doença foi descrita pelo Dr. Heinrich Quincke, em 1882.
Referências
- ↑ «What is Hereditary Angioedema?». HAE Canada
- ↑ Konrad, Bork (2010). «Diagnosis and treatment of hereditary angioedema with normal C1 inhibitor». Allergy, Asthma & Clinical Immunology. 6 (1): 15. doi:10.1186/1710-1492-6-15
- ↑ «Diagnosing HAE». HAE Canada
- ↑ Normal C1 inhibitor hereditary angioedema. Kittisupamongkol W. Am J Med. 2009 May;122(5):e7; author reply e9. doi: 10.1016/j.amjmed.2008.11.011.
- ↑ Colobran, Roger; Lois, Sergio; de la Cruz, Xavier; Pujol-Borrell, Ricardo; Hernández-González, Manuel; Guilarte, Mar. Clinical Immunology. Feb2014, Vol. 150 Issue 2, p143-148. 6p. DOI: 10.1016/j.clim.2013.11.013.
- ↑ Madsen, Flemming; Attermann, J&phgr;rn; Linneberg, Allan. Acta Dermato-Venereologica. 2012, Vol. 92 Issue 5, p475-479. 5p. DOI: 10.2340/00015555-1389.
- ↑ Overview of hereditary angioedema caused by C1-inhibitor deficiency: assessment and clinical management. Bork K, Davis-Lorton M.
- ↑ «More Information». HAE UK. Consultado em 4 de novembro de 2014. Arquivado do original em 22 de abril de 2014
- ↑ Type III hereditary angioedema: defined, but not understood. Kaplan A. Ann Allergy Asthma Immunol. 2012 Sep;109(3):153-4. doi: 10.1016/j.anai.2012.07.007.