Ácido nitrosilsulfúrico
O ácido nitrosilsulfúrico é o composto químico de fórmula NOHSO4. É um sólido incolor que é utilizado industrialmente na produção de caprolactama,[1] e anteriormente fazia parte do processo de câmara de chumbo para produzir ácido sulfúrico. O composto é o anidrido misto do ácido sulfúrico e ácido nitroso.
Na química orgânica, é usado como reagente para nitrosilação, como um agente diazotizante, e como um agente oxidante.[2]
Síntese e reações
[editar | editar código-fonte]Um procedimento típico envolve a dissolução de nitrito de sódio em ácido sulfúrico frio:[3][4]
- HNO2 + H2SO4 → NOHSO4 + H2O
Também pode ser preparado pela reação de ácido nítrico e dióxido de enxofre.[5]
NOHSO4 é usado na química orgânica para preparar sais de diazônio a partir de aminas, como por exemplo na Reação de Sandmeyer. Reagentes transportadores de NO relacionados incluem tetrafluoroborato de nitrosônio ([NO]BF4) e cloreto de nitrosila.
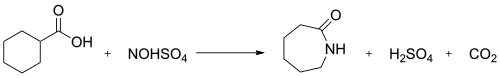
Na indústria, a reação de nitrosodecarboxilação entre o ácido nitrosilsulfúrico e ácido ciclohexanocarboxílico é usado para gerar caprolactama:[1]
Segurança
[editar | editar código-fonte]O ácido nitrosilsulfúrico é um material perigoso e precauções devem ser tomadas.[2]
Referências
[editar | editar código-fonte]- ↑ a b Tinge, Johan; Groothaert, Marijke; Veld, Hans op het; Ritz, Josef; Fuchs, Hugo; Kieczka, Heinz; Moran, William C. (2018). «Caprolactam». American Cancer Society (em inglês): 1–31. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a05_031.pub3. Consultado em 31 de maio de 2021
- ↑ a b Olah, George A.; Prakash, G. K. Surya; Wang, Qi; Li, Xing-Ya (2001). «Nitrosylsulfuric Acid». American Cancer Society (em inglês). ISBN 978-0-470-84289-8. doi:10.1002/047084289x.rn060. Consultado em 31 de maio de 2021
- ↑ Hodgson, H. H.; Mahadevan, A. P.; Ward, E. R. (1955). «1,4-Dinitronaphthalene». Org. Synth.; Coll. Vol., 3 (diazodization followed by treatment with nitrite)
- ↑ Sandin, R. B.; Cairns, T. L. (1943). «1,2,3-Triiodo-5-nitrobenzene». Org. Synth.; Coll. Vol., 2 (diazodization followed by treatment with iodide)
- ↑ Coleman, George H.; Lillis, Gerald A.; Goheen, Gilbert E.; Herrmann, C. V.; Booth, H. S. (1939). «Nitrosyl Chloride». John Wiley & Sons, Ltd (em inglês): 55–59. ISBN 978-0-470-13232-6. doi:10.1002/9780470132326.ch20. Consultado em 31 de maio de 2021