Neurônio olfatório
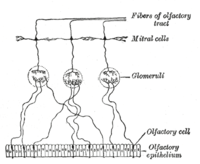
Um neurônio receptor olfatório (do inglês ORN ou OSN), é uma célula de transdução de sinal do sistema olfativo presente no epitélio olfatório.[1] Esses neurônios podem se dividir em neurônios olfatórios maduros ou imaturos e são originados das células horizontais ou basais.
Vertebrados[editar | editar código-fonte]
Os seres humanos têm cerca de 6 milhões de neurônios olfatórios.[2] Em vertebrados, OSNs são neurônios bipolares com um dendrito voltados para a luz da cavidade nasal e um axônio que atravessa a placa cribriforme e segue ao longo do nervo olfatório para o bulbo olfatório onde convergem para estruturas denominadas glomérulos. Os OSNs estão localizados na cavidade nasal do epitélio olfatório . Os corpos celulares dos OSNs são distribuídos entre as três camadas estratificadas do epitélio olfatório.[3]
Estrutura[editar | editar código-fonte]
Pequenas estruturas denominadas cílios se projetam a partir do dendrito da célula olfatória para fora do epitélio olfatório onde ficam recobertos do muco presente nessa cavidade. A superfície desses cílios é coberto com receptores olfatórios, um tipo de Receptor acoplado à proteína G que ativa os neurônios mediante reconhecimento de um odorante. Cada OSN expressa apenas um tipo de receptor olfatório (OR) dentre cerca de 800 possibilidades (em humanos) e 1400 em camundongos. Os axônios das células receptoras que expressam um mesmo OR convergem para os mesmos glomérulos no bulbo olfatório[4][5][6].
Função[editar | editar código-fonte]
A principal função dos neurônios olfatórios é reconhecer moléculas, que tenham se dissolvido no muco, e sinalizar esse reconhecimento para neurônios de níveis hierárquicos superiores, como as células mitrais do bulbo olfatório. O reconhecimento dessas moléculas acontece através dos receptores olfatórios, localizados nas membranas dos cílios, que desencadeiam uma complexa cascata que leva a ativação de receptores ionotrópicos capazes de despolarizar o neurônio.[7] Os neurônios ativos realizam sinapses, nos glomérulos, com as células mitrais indicando a presença dos odorantes pelos quais aqueles neurônios são responsáveis.
Mecanismo[editar | editar código-fonte]
Um odorante (molécula que ativa os receptores olfatórios) dissolve-se no muco do epitélio olfatório e, em seguida, liga-se a receptores olfatórios (ORs) específicos para aquela molécula. Essa interação ativa o OR que muda de conformação e ativa a proteína G. Quando ativa, a subunidade alfa da proteína G (que nesses neurônios é a G alfa olf) se desliga do restante do complexo e fosforila a proteína adenilato ciclase III.
A proteína adenilato ciclase III fosforilada é capaz de converter ATP e cAMP. O aumento na concentração de cAMP causa a ativação de canais iônicos, na membrana celular, que mudam de conformação e permitem um fluxo de íons sódio e cálcio para dentro da célula, e um efluxo de íons cloreto de dentro para fora da célula. Essa passagem de íons faz com que o neurônio depolarize, gerando um potencial de ação. Se esse potencial é suficientemente positivo, o neurônio libera vesículas contendo neurotransmissores, para os glomérulos, que podem ser reconhecidos por outros neurônios.[8][9]

Dessensibilização de Neurônio Olfatório[editar | editar código-fonte]
O feedback negativo de resposta após a despolarização neurônio olfatório tem um funcionamento rápido. Quando o neurônio é despolarizado, o canal de íons CNG é aberto, permitindo que a entrada de Sódio e Cálcio. O cálcio, agora em alta concentração na célula, inicia uma cascata de eventos que geram a dessensibilização do neurônio. Primeiro, o cálcio se liga à calmodulina para formar o complexo CaM. CaM vai, em seguida, se ligar ao canal (CNG) e fechá-lo, interrompendo a entrada de sódio e de cálcio.[10] A Proteína quinase dependente de calmodulina (CaMKII) será ativada pela presença de CaM, que vai fosforilar a adenilato ciclase II e reduzir a produção cAMP.[11] CaMKII irá também ativar a fosfodiesterase, que, em seguida, irá hidrolisar o cAMP presente na célula.[12] O efeito da resposta de feedback negativo diminui a sensibilidade do neurônio, necessitando uma maior quantidade de odorantes para sua ativação.
Ciclo de Maturação[editar | editar código-fonte]
Células Basais[editar | editar código-fonte]
São pequenas, redondasas ou cónicas e formam uma camada única basal na região do epitélio, entre as células olfativas e as de sustentação.
Células Globosas[editar | editar código-fonte]
Neurônios Olfatórios Imaturos[editar | editar código-fonte]
As células globosas se diferenciam em neurônios olfatórios que ficam em porções mais basais do epitélio. É nesse período que o neurônio passa a expressar genes característicos de neurônios olfatórios, como por exemplo os fatores de transcrição necessários para a expressão dos genes ORs.
Nessa fase, é iniciada a transcrição de receptores olfatórios num padrão de expressão diferente dos neurônios maduros. A quantidade de transcritos ainda é bem reduzida e mais de um gene pode ser expresso desde que seja pertencente àquela zona[13]. Essa transcrição desencadeia um sinal de feedback negativo [14][15] que causa uma uma marcação epigenética responsável pelo silenciamento desses outros genes. Depois disso, o neurônio escolhe apenas um dos receptores olfatórios para ser expresso e intensifica sua transcrição reprimindo também os demais. Os mecanismos envolvidos nessa escolha e na repressão dos genes ainda são desconhecidos, embora já se saiba que dependem da expressão das proteínas de receptores olfatórios funcionais, da adenilyl ciclase III e da proteína de deposição de marcas de histona LSD I
Neurônios Olfatórios Maduros[editar | editar código-fonte]
Insetos[editar | editar código-fonte]
Veja também[editar | editar código-fonte]
- Quimiorreceptores
- Receptores sensoriais
Referências
- ↑ Vermeulen, A; Rospars, J. P. (1998). «Dendritic integration in olfactory sensory neurons: A steady-state analysis of how the neuron structure and neuron environment influence the coding of odor intensity». Journal of computational neuroscience. 5 (3): 243–66. PMID 9663551
- ↑ Moran, David T.; Rowley III, J. Carter; Jafek, Bruce W.; Lovell, Mark A. (1982). «The fine structure of the olfactory mucosa in man». Journal of Neurocytology. 11 (5): 721–46. PMID 7143026. doi:10.1007/BF01153516
- ↑ Cunningham, A.M.; Manis, P.B.; Reed, R.R.; Ronnett, G.V. (1999). «Olfactory receptor neurons exist as distinct subclasses of immature and mature cells in primary culture». Neuroscience. 93 (4): 1301–12. PMID 10501454. doi:10.1016/s0306-4522(99)00193-1
- ↑ Ressler, K. J.; S. L. (30 de dezembro de 1994). «Information coding in the olfactory system: evidence for a stereotyped and highly organized epitope map in the olfactory bulb». Cell. 79 (7): 1245–1255. ISSN 0092-8674. PMID 7528109
- ↑ Wang, F.; A. (3 de abril de 1998). «Odorant receptors govern the formation of a precise topographic map». Cell. 93 (1): 47–60. ISSN 0092-8674. PMID 9546391
- ↑ Mombaerts, P.; F. (15 de novembro de 1996). «Visualizing an olfactory sensory map». Cell. 87 (4): 675–686. ISSN 0092-8674. PMID 8929536
- ↑ Touhara, Kazushige (2009). «Insect Olfactory Receptor Complex Functions as a Ligand-gated Ionotropic Channel». Annals of the New York Academy of Sciences. 1170: 177–80. Bibcode:2009NYASA1170..177T. PMID 19686133. doi:10.1111/j.1749-6632.2009.03935.x
- ↑ Lin, David M.; Yang, Yee Hwa; Scolnick, Jonathan A.; Brunet, Lisa J.; Marsh, Heather; Peng, Vivian; Okazaki, Yasushi; Hayashizaki, Yoshihide; Speed, Terence P. (24 de agosto de 2004). «Spatial patterns of gene expression in the olfactory bulb». Proceedings of the National Academy of Sciences of the United States of America (em inglês). 101 (34): 12718–12723. ISSN 0027-8424. PMID 15304640. doi:10.1073/pnas.0404872101
- ↑ Firestein, Stuart. «www.nature.com/doifinder/10.1038/35093026». Nature. 413 (6852): 211–218. doi:10.1038/35093026
- ↑ Bradley, J; Reuter, D; Frings, S (2001). «Facilitation of calmodulinmediated odor adaptation by cAMP-gated channel subunits». Science. 294: 2176–2178. doi:10.1126/science.1063415
- ↑ Wei, J; Zhao, AZ; Chan, GC; Baker, LP; Impey, S; Beavo, JA; Storm, DR (1998). «Phosphorylation and inhibition of olfactory adenylyl cyclase by CaM kinase II in Neurons: a mechanism for attenuation of olfactory signals». Neuron. 21: 495–504. doi:10.1016/s0896-6273(00)80561-9
- ↑ Yan, C; Zhao, AZ; Bentley, JK; Loughney, K; Ferguson, K; Beavo, JA (1995). «Molecular cloning and characterization of a calmodulin-dependent phosphodiesterase enriched in olfactory sensory neurons». Proc Natl Acad Sci USA. 92: 9677–9681. doi:10.1073/pnas.92.21.9677
- ↑ Hanchate, Naresh K.; Kunio (4 de dezembro de 2015). «Single-cell transcriptomics reveals receptor transformations during olfactory neurogenesis». Science (em inglês). 350 (6265): 1251–1255. ISSN 0036-8075. PMID 26541607. doi:10.1126/science.aad2456
- ↑ Serizawa, Shou; Kazunari (19 de dezembro de 2003). «Negative feedback regulation ensures the one receptor-one olfactory neuron rule in mouse». Science (New York, N.Y.). 302 (5653): 2088–2094. ISSN 1095-9203. PMID 14593185. doi:10.1126/science.1089122
- ↑ Lewcock, Joseph W.; Randall R. (27 de janeiro de 2004). «A feedback mechanism regulates monoallelic odorant receptor expression». Proceedings of the National Academy of Sciences of the United States of America. 101 (4): 1069–1074. ISSN 0027-8424. PMID 14732684. doi:10.1073/pnas.0307986100
Ligações externas[editar | editar código-fonte]
- NIF de Busca Olfativa receptor do neurônio através da Neurociência Estrutura de Informações
- Inseto olfato
