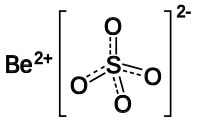
Sulfato de berílio
Aspeto
| Sulfato de berílio Alerta sobre risco à saúde | |
|---|---|
| |

| |
| Identificadores | |
| Número CAS | |
| PubChem | |
| Número EINECS | |
| ChemSpider | |
| ChEBI | |
| Número RTECS | DS4800000 |
| SMILES |
|
| InChI | 1/Be.H2O4S/c;1-5(2,3)4/h;(H2,1,2,3,4)/q+2;/p-2
|
| Propriedades | |
| Fórmula molecular | BeSO4 |
| Massa molar | 105.075 g/mol (anidro) 177.136 g/mol (tetrahidratado) |
| Aparência | Sólido branco |
| Odor | Sem odor |
| Densidade | 2.50 g/cm3 (anidro) 1.71 g/cm3 (tetrahidratado) |
| Ponto de fusão |
110 °C (tetrahidratado, −2H2O) |
| Ponto de ebulição |
2500 °C (anidro) |
| Solubilidade em água | 30.5 g/100 mL (30 °C) |
| Solubilidade | Insolúvel em álcool |
| Índice de refracção (nD) | 1.4374 (tetrahidratado) |
| Riscos associados | |
| MSDS | ICSC 1351 |
| Classificação UE | Carc. Cat. 2 Very toxic (T+) Dangerous for the environment (N) |
| Índice UE | 004-002-00-2 |
| Frases R | R49, R25, R26, R36/37/38, R43, R48/23, R51/53 |
| Frases S | S53, S45 |
| Ponto de fulgor | Não inflamável |
| LD50 | 82 mg/kg |
| Compostos relacionados | |
| Outros catiões/cátions | Sulfato de magnésio Sulfato de cálcio Sulfato de estrôncio Sulfato de bário |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Sulfato de berílio (BeSO4) é um sólido branco cristalino. Foi isolado pela primeira vez em 1815 por Jons Jakob Berzelius.[1]
O composto pode ser preparado pelo tratamento de uma solução aquosa de qualquer sal de berílio com ácido sulfúrico e posterior evaporação e cristalização. O sal hidratado se converte na forma anidra pelo aquecimento a 400 °C.[2]
Uma mistura de sulfato de berílio e rádio foi utilizada como fonte de nêutrons na descoberta da fissão nuclear.
Referências
- ↑ Lathrop Parsons, Charles (1909). The Chemistry and Literature of Beryllium (em inglês). Londres: [s.n.] pp. 29–33
- ↑ Patnaik, Pradyot (2002). Handbook of Inorganic Chemicals. [S.l.]: McGraw-Hill. ISBN 0-07-049439-8
