Ponto crítico (termodinâmica)
Em física, termodinâmica, química, físico-química e física da matéria condensada, um ponto crítico, também chamado de estado crítico, ocorre sob condições (tais como valores específicos de temperatura, pressão ou composição) no qual não existem limites de fase. Existem vários tipos de pontos críticos, incluindo pontos críticos líquido-vapor e líquido-líquido.[1][2]
Substâncias puras: ponto crítico líquido-vapor[editar | editar código-fonte]
O "ponto crítico" é por vezes usado para denotar o ponto especificamente vapor-líquido crítico de um material, a partir do qual a distinção entre fase a líquida e gasosa não existe.
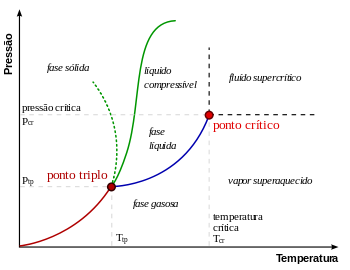
O ponto crítico de vapor-líquido em um diagrama de fases pressão-temperatura está no extremo de alta temperatura do limite de fase líquido-gás. A linha pontilhada verde mostra o comportamento anômalo da água.[3]
Como se mostra no diagrama de fases para a direita, isto é o ponto em que a fronteira entre a fase líquida e gasosa termina. Em água, o ponto crítico ocorre em cerca de 647 K. (374 ° C; 705 ° F) e 22,064 MPa (218 atm)
À medida que a substância se aproxima da temperatura crítica, as propriedades da sua fases gasosa e líquida convergem, resultando em apenas uma fase no ponto crítico: um fluido supercrítico homogêneo. O calor de vaporização é zero no ponto crítico e para além dele, por isso não existe distinção entre as duas fases. No diagrama de Pressão-temperatura, o ponto em que a temperatura crítica e pressão crítica satisfazer é chamado de ponto crítico da substância. Acima da temperatura crítica, um líquido não pode ser formada por um aumento da pressão, apesar de um sólido poder ser formado sob uma pressão suficiente. A pressão crítica é a pressão de vapor, à temperatura crítica. O volume crítico é o volume molar de uma mole do material a uma temperatura e pressão críticas.
Propriedades críticas variam de material para material, e para muitas substâncias puras estão prontamente disponíveis na literatura. No entanto, a obtenção de propriedades críticas para misturas é mais desafiador.
Definição matemática[editar | editar código-fonte]
No caso das substâncias puras, há um ponto de inflexão na curva isotérmica crítica (linha de temperatura constante) com um diagrama de Pressão-Volume. Isto significa que, no ponto crítico: [4][5][6]
Isto é, as primeira e segunda derivadas parciais da pressão p no que diz respeito ao volume V são ambos zero, com as derivadas parciais avaliados em temperatura constante T. Esta relação pode ser usada para avaliar dois parâmetros de uma equação de estado em termos das propriedades críticas, tais como os parâmetros a e b na equação de van der Waals.[4]
Às vezes um conjunto de propriedades reduzidas é definida em termos das propriedades importantes, isto é:[7]
onde é a temperatura reduzida, é a pressão reduzida, é a redução do volume, e é a constante universal dos gases.
História[editar | editar código-fonte]
A existência de um ponto crítico foi descoberto pela primeira vez por Charles Cagniard de la Tour em 1822[8] [9] e nomeado por Thomas Andrews, em 1869.[10] Ele mostrou que o CO2 poderia ser liquefeito a 31 ° C a uma pressão de 73 atm, mas não a uma temperatura ligeiramente mais elevada, mesmo sob uma pressão muito mais elevada (até 3,000 atm).
Misturas: ponto crítico líquido-líquido[editar | editar código-fonte]
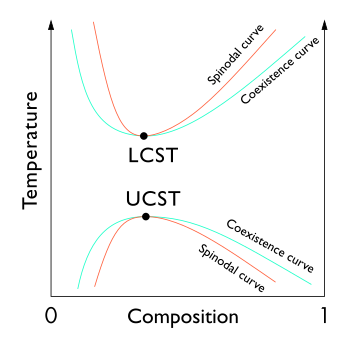
O ponto crítico líquido-líquido de uma solução, o que ocorre a uma temperatura crítica da solução, ocorre no limite da região de duas fases no diagrama de fases. Em outras palavras, é o ponto no qual uma mudança infinitesimal em alguma variável termodinâmica (tais como a temperatura ou a pressão), conduzirá a separação da mistura em duas fases líquidas distintas, como se mostra no diagrama de fases do polímero-solvente à direita. Existem dois tipos de pontos críticos líquido-líquido, que são a temperatura de solução crítica superior , em inglês (UCST), representa o ponto mais quente na qual o arrefecimento irá induzir a separação de fases, e a temperatura de solução crítica inferior, em inglês (TCIS), que é o ponto mais frio no qual o aquecimento irá induzir a separação de fases.
Definição matemática[editar | editar código-fonte]
Do ponto de vista teórico, o ponto crítico líquido-líquido representa o extremo da temperatura da concentração da curva spinodal (como pode ser visto na figura, à direita). Assim, o ponto crítico líquido-líquido em um sistema de dois componentes deve satisfazer duas condições: condição da curva spinodal (a segunda derivada da energia livre em relação a concentração deve ser igual a zero), e da condição extrema (a terceira derivada da energia livre no que diz respeito à concentração também deve ser igual a zero ou a derivada da temperatura spinodal com respeito à concentração deve ser igual a zero).
Ver também[editar | editar código-fonte]
Referências[editar | editar código-fonte]
- ↑ http://fge.if.usp.br/~oliveira/term082ed.pdf
- ↑ O. Gomes, Gabriel; Stanley, H. Eugene; Souza, Mariano de (19 de agosto de 2019). «Enhanced Grüneisen Parameter in Supercooled Water». Scientific Reports (em inglês). 9 (1): 1–8. ISSN 2045-2322. doi:10.1038/s41598-019-48353-4
- ↑ Anomalia da água. Por Domiciano Correa Marques da Silva. Mundo Educação.
- ↑ a b P. Atkins and J. de Paula, Physical Chemistry, 8th ed. (W.H. Freeman 2006), p.21
- ↑ K.J. Laidler and J.H. Meiser, Physical Chemistry (Benjamin/Cummings 1982), p.27
- ↑ P.A. Rock, Chemical Thermodynamics (MacMillan 1969), p.123
- ↑ Cengel, Yunus A.; Boles, Michael A. (2002). Thermodynamics: an engineering approach. Boston: McGraw-Hill. pp. 91–93. ISBN 0-07-121688-X
- ↑ Charles Cagniard de la Tour (1822) #v=onepage&q&f=false "Exposé de quelques résultats obtenu par l'action combinée de la chaleur et de la compression sur certains liquides, tels que l'eau, l'alcool, l'éther sulfurique et l'essence de pétrole rectifiée" (Presentation of some results obtained by the combined action of heat and compression on certain liquids, such as water, alcohol, sulfuric ether [i.e., diethyl ether], and distilled petroleum spirit), Annales de chimie et de physique, 21 : 127-132.
- ↑ Berche, B., Henkel, M., Kenna, R (2009) Critical phenomena: 150 years since Cagniard de la Tour. Journal of Physical Studies 13 (3) , pp. 3001-1-3001-4.
- ↑ Andrews, Thomas (1869) "The Bakerian lecture: On the continuity of the gaseous and liquid states of matter," Philosophical Transactions of the Royal Society (London), 159 : 575-590; the term "critical point" appears on page 588.











