Secagem supercrítica

Secagem supercrítica é um processo para remover o líquido em uma maneira controlada com precisão. É útil na produção de sistemas microeletromecânicos (MEMS), secagem de especiarias, produção de aerogel e na preparação de amostras biológicas para microscopia eletrônica de varredura.
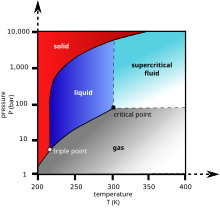
Como a substância em um corpo líquido atravessa a fronteira do estado líquido para gás (veja a seta verde no diagrama de fases), o liquido vira gás em uma taxa finita, enquanto o volume de líquido do corpo diminui. Quando isso acontece dentro de um ambiente heterogêneo, a tensão superficial de líquidos no corpo puxa contra quaisquer estruturas sólidas do líquido que possa entrar em contato. Estruturas delicadas, como as paredes celulares, os dendritos em gel de sílica e dispositivos microeletromecânicos, tendem a ser quebrados por esta tensão de superfície como os movimentos por interface líquido-sólido.
Para evitar isso, a amostra pode ser trazida por meio de dois possíveis caminhos alternativos a partir da fase líquida para a fase gasosa sem cruzar a fronteira líquido-gás no diagrama de fase. Na liofilização, isso significa ir ao redor à esquerda (baixa temperatura, baixa pressão; seta azul). No entanto, algumas estruturas são interrompidas até mesmo pela fronteira sólido-gás. Na secagem supercrítica, por outro lado, vai em torno da linha para a direita, sobre a alta temperatura e alta pressão (seta vermelha). Esta rota de líquido para gás não atravessa qualquer fronteira fase, em vez de passar pela região supercrítica, onde a distinção entre gás e líquido deixa de ser aplicável. Densidades da fase líquida e fase vapor torna-se igual em ponto crítico de secagem.
Os fluidos mais adequados para esse processo são o dióxido de carbono (ponto critico em 304.25 K a 7.39 MPa ou 31.1 °C a 1072 psi) e o freon (≈300 K a 3.5–4 MPa ou 25–0 °C em 500–600 psi).[1]
Na maioria dos processos dessa natureza, a acetona é usada primeiramente para lavar toda a água, explorando a completa miscibilidade desses dois fluidos. A acetona é então lavada com alta pressão de dióxido de carbono líquido, o padrão da indústria, agora que o Diclorodifluorometano não está disponível. O dióxido de carbono líquido é então aquecido até que sua temperatura vai além do ponto crítico, momento em que a pressão pode ser gradualmente liberada, permitindo que o gás escape, deixando um produto seco.
Notas[editar | editar código-fonte]
- Este artigo foi inicialmente traduzido, total ou parcialmente, do artigo da Wikipédia em inglês cujo título é «supercritical drying».
Referencias[editar | editar código-fonte]
- ↑ «ProSciTech: Page K3: Critical point dryers, freeze dryers». Consultado em 18 de novembro de 2010. Arquivado do original em 9 de setembro de 2012
