Gluconato
| Ácido glucónico Alerta sobre risco à saúde | |
|---|---|
| |
| |
| Nome IUPAC | ácido (2R,3S,4R,5R)-2,3,4,5,6-pentahidroxihexanóico |
| Outros nomes | Nenhum |
| Identificadores | |
| Número CAS | |
| Propriedades | |
| Fórmula molecular | C6H12O7 |
| Massa molar | 196 g/mol |
| Aparência | Cristais incolores |
| Densidade | ? |
| Solubilidade em água | boa |
| Solubilidade em outros solventes | ? |
| Acidez (pKa) | 3.86 |
| Riscos associados | |
| Principais riscos associados |
Corrosivo (C) |
| Ponto de fulgor | ? |
| Compostos relacionados | |
| Compostos relacionados | Glucose (carboxila reduzida a carbonila) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
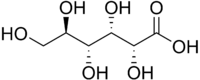
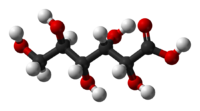
O ácido glucónico é um composto orgânico com fórmula molecular C6H12O7 e fórmula estrutural condensada HOCH2(CHOH)4COOH.
Em soluções aquosas a pH neutro, o ácido glucónico forma o ião gluconato. Os sais de ácido glucónico são conhecidos como "gluconatos". O ácido glucónico e os sais de gluconato ocorrem muito na natureza porque tais espécies derivam da oxidação da glucose. Ésteres de gluconato também podem ser formados, tal como gluconato de quinina que é usado em injecções intramusculares para o tratamento da malária.
Estrutura Química
[editar | editar código-fonte]A estrutura química do ácido glucónico consiste numa cadeia de seis carbonos com 5 grupos hidroxila terminando num ácido carboxílico. Em solução aquosa o ácido glucónico existe em equilíbrio com o éster cíclico glucono delta-lactona
Ocorrência e usos
[editar | editar código-fonte]O ácido glucónico ocorre naturalmente na fruta, mel e vinho Como aditivo alimentar (E574[1]), é um regulador de acidez. É também usado em produtos de limpeza, onde dissolve depósitos minerais, especialmente um soluções alcalinas. O anião gluconato é um quelante de Ca2+, Fe2+, Al3+, e de outros metais pesados. O gluconato de cálcio, na forma de gel, é usado para tratar queimaduras de ácido fluorídrico.[2][3]
Referências
[editar | editar código-fonte]- ↑ Food Standards Agency - Current EU approved additives and their E Numbers
- ↑ el Saadi MS, Hall AH, Hall PK, Riggs BS, Augenstein WL, Rumack BH (1989). «Hydrofluoric acid dermal exposure». Vet Hum Toxicol. 31 (3): 243–7. PMID 2741315
- ↑ Roblin I, Urban M, Flicoteau D, Martin C, Pradeau D (2006). «Topical treatment of experimental hydrofluoric acid skin burns by 2.5% calcium gluconate». J Burn Care Res. 27 (6): 889–94. PMID 17091088. doi:10.1097/01.BCR.0000245767.54278.09
