Éter coroa

Éter coroa é um composto químico cíclico constituído por um anel e vários grupos éter. Os éteres coroa mais comuns são os oligômeros do óxido de etileno, sendo etilenoxi a unidade repetida -CH2CH2O-. Importantes membros dessa série são os tetrâmeros (n=4), pentâmeros (n=5) e o hexâmeros (n=6). O termo coroa se refere à semelhança entre o anel do éter coroa se ligando a um cátion e a uma coroa sobre uma cabeça.
O primeiro número do nome de um éter coroa se refere ao número de átomos no heterociclo, e o segundo se refere ao número de átomos de oxigênio.
Éteres coroa se ligam fortemente a certos cátions, formando complexos. Os átomos de oxigênio estão bem situados para se coordenarem com o cátion no meio do anel, enquanto que o exterior do anel é hidrofóbico. Os cátions resultantes frequentemente formam sais que são solúveis em solventes não polares, por isso éteres coroa são úteis em catálise de transferência de fase. A seletividade do éter-coroa para um determinado cátion deriva da complementaridade de tamanho da cavidade com o diâmetro do cátion. Por exemplo, 18-coroa-6 tem alta afinidade para cátions K+, 15-coroa-5 tem afinidade com cátions Na+, 12-coroa-4 tem afinidade para cátions Li+. A alta afinidade por K+ do 18-coroa-6 contribui para sua toxidade.
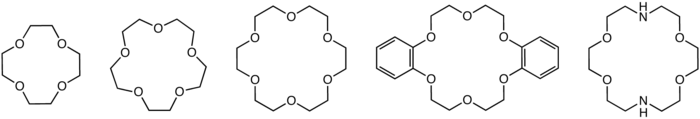
Estrutura de éteres coroa comuns: 12-Coroa-4, 15-Coroa-5, 18-Coroa-6, Dibenzo-18-coroa-6, and Diaza-18-coroa-6
Éteres coroa na natureza[editar | editar código-fonte]
Éteres coroa não são os únicos ligantes macrocíclicos que tem afinidade por íons potássio. Ionóforos como valinomicina também mostram uma afinidade maior ao cátion potássio do que a outros cátions.
História dos éteres coroa sintéticos[editar | editar código-fonte]
Em 1967, Charles J. Pedersen, um químico que trabalhava para a DuPont, descobriu um método simples de sintetizar éteres coroa quando estava tentando sintetizar um agente complexante para cátions divalentes.[1][2] Sua estratégia consistiu em ligar dois grupos catecolato através de uma hidroxila de cada molécula. Essa vinculação define um ligante polidentado que poderia envolver parcialmente o cátion, e por ionização das hidroxilas fenólicas, neutralizar o dicátion preso. Pedersen ficou surpreso em isolar um subproduto que ficou fortemente complexado a cátions de potássio. Citando um trabalho mais recente sobre a dissolução de potássio em 16-coroa-4,[3][4] ele percebeu que poliéteres cíclicos representavam uma nova classe de agentes complexantes que podiam se ligar a cátions de metais alcalinos. Pedersen então começou a reportar uma serie de estudos sistemáticos sobre a síntese, e propriedades de complexação de éteres coroa. Pedersen popularizou os éteres de coroa dibenzo.[5]
Pedersen dividiu o prêmio Nobel de química de 1987 com Donald J. Cram e Jean Marie Lehn pela descoberta e uso de moléculas de estrutura especifica de alta seletividade.
Afinidade por cátions[editar | editar código-fonte]
Além de sua alta afinidade por cátions K+, 18-coroa-6 pode também se complexar com aminas protonadas, esses complexos são estáveis tanto em solução quanto em fase de gás. Alguns aminoácidos como a lisina possuem amina primária em sua cadeia lateral. Esses grupos aminos protonados podem se ligar na cavidade do 18-coroa-6 e formar complexos estáveis na fase de gás. São formadas ligações de hidrogênio entre os três átomos de hidrogênio da amina terciária e três átomos de oxigênio da 18-coroa-6. As ligações de hidrogênio fazem deste composto um aduto estável.
Coroas-aza[editar | editar código-fonte]
Derivados de éteres Coroas diaza de 18 e 21 membros exibem excelente seletividade para com cálcio e magnésio e são amplamente usados em eletrodos íons-seletivos.[6] Uma parte ou todos os oxigênios do éter coroa podem ser substituídos para formar criptandos.[7]
Referências
- ↑ Pedersen, Charles J. (1 de dezembro de 1967). «Cyclic polyethers and their complexes with metal salts». Journal of the American Chemical Society. 89 (26): 7017-7036. ISSN 0002-7863. doi:10.1021/ja01002a035
- ↑ Pedersen, Charles J. (1 de maio de 1967). «Cyclic polyethers and their complexes with metal salts». Journal of the American Chemical Society. 89 (10): 2495-2496. ISSN 0002-7863. doi:10.1021/ja00986a052
- ↑ D. G. Stewart. D. Y. Waddan and E. T. Borrows, GB 785229 Oct. 23, 1957.
- ↑ J. L. Down, J. Lewis, B. Moore and G. W. Wilkinson, Proc. Chem. Soc., 1959, 209; J. Chem. Soc., 1959, 3767.
- ↑ Charles J. Pedersen (1988). «Macrocyclic Polyethers: Dibenzo-18-Crown-6 Polyether and Dicyclohexyl-18-Crown-6 Polyether». Org. Synth.; Coll. Vol., 6
- ↑ K. Suzuki, K. Watanabe, Y. Matsumoto, M. Kobayashi, S. Sato, D. Siswanta, H. Hisamoto (1995). «Design and Synthesis of Calcium and Magnesium Ionophores Based on Double-Armed Diazacrown Ether Compounds and Their Application to an Ion Sensing Component for an Ion-Selective Electrode». Anal. Chem. 67 (2): 324–334. doi:10.1021/ac00098a016
- ↑ Vincent J. Gatto, Steven R. Miller, and George W. Gokel (1988). «4,13-Diaza-18-Crown-6». Org. Synth.; Coll. Vol., 8

