Tetróxido de nitrogênio: diferenças entre revisões
m Bot: Modificando: bg:Диазотен тетраоксид |
|||
| Linha 41: | Linha 41: | ||
[[Categoria:Compostos de azoto|Oxido de nitrogenio, tetra]] |
[[Categoria:Compostos de azoto|Oxido de nitrogenio, tetra]] |
||
[[bg:Диазотен тетраоксид]] |
|||
[[bg:Двуазотен четириокис]] |
|||
[[da:Dinitrogentetroxid]] |
[[da:Dinitrogentetroxid]] |
||
[[de:Distickstofftetroxid]] |
[[de:Distickstofftetroxid]] |
||
Revisão das 08h26min de 25 de abril de 2009
| Dinitrogen tetroxide Alerta sobre risco à saúde | |
|---|---|
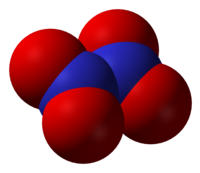
| |
| Nome IUPAC | Dinitrogen Tetroxide |
| Identificadores | |
| Número CAS | |
| Propriedades | |
| Fórmula molecular | N2O4 |
| Massa molar | 92.011 u |
| Aparência | Gás transparente |
| Densidade | 1443 kg/m³ (líquido a 1.013 bar, ponto de ebulição) |
| Ponto de fusão | |
| Ponto de ebulição |
294.3 K (21.1 °C) |
| Solubilidade em outros solventes | reage com a água |
| Pressão de vapor | 96 kPa (20 °C) [1] |
| Termoquímica | |
| Entalpia padrão de formação ΔfH |
-35.05 kJ/mol |
| Entropia molar padrão S |
150.38 J/(mol•K) |
| Riscos associados | |
| Principais riscos associados |
Ingestão: ? Inalação: Corrosivo & tóxico a pele: Corrosivo olhos: Corrosivo |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Tetróxido de nitrogênio ou tetróxido de dinitrogênio é um composto com fórmula N2O4. Apresenta-se como líquido abaixo de 21ºC e que solidifica a -11ºC. Decompõe-se facilmente e reversivelmente a um gás avermelhado que possui elétrons desemparelhados, agindo em muitos casos como radical livre, o NO2.
Em contato com a água, forma ácido nítrico, sendo por isso usado na produção deste. A redução do ácido nítrico pode formar este óxido novamente e o óxido é formado pela reação espontânea entre o monóxido de nitrogênio (NO) e o oxigênio, sendo no passado esta reação usada no processo de câmara de chumbo para produção de ácido sulfúrico, pela reação do NO2 com o SO2 para produzir SO3 e ácido sulfúrico pela adição deste com água. O NO é produzido pela queima catalítica da amônia (processo Ostwald) ou pelo forte aquecimento (acima de 1000ºC) de uma mistura de nitrogênio e oxigênio.
É usado como propelente de foguetes, formando misturas hipergólicas (de auto-ignição), com hidrazina e seus compostos.
