Isofluorofato
| Isofluorofato Alerta sobre risco à saúde | |
|---|---|
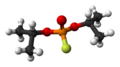
| |
| Nome IUPAC | 2-[fluoro(propan-2-ol-oxi)fosforil]oxipropano |
| Identificadores | |
| Número CAS | |
| SMILES |
|
| InChI | InChI=1S/C6H14FO3P/c1-5(2)9-11(7,8)10-6(3)4/h5-6H,1-4H3
|
| Propriedades | |
| Fórmula molecular | C6H14FO3P |
| Massa molar | 140.09 g/mol |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Isofluorofato, fluorofosfato de di-isopropil (português brasileiro) ou di-isopropilo fluorofosfato (português europeu) é um composto sintético de fósforo de formulação C6H14FO3P.[1]
Referências
- ↑ PubChem. «Diisopropyl fluorophosphate». pubchem.ncbi.nlm.nih.gov (em inglês). Consultado em 30 de janeiro de 2021
