Nitreto de alumínio
| Nitreto de alumínio Alerta sobre risco à saúde[1] | |
|---|---|

| |
| Identificadores | |
| Número CAS | |
| Propriedades | |
| Fórmula molecular | AlN |
| Massa molar | 40.988 g mol-1 |
| Aparência | sólido cristalino, branco azulado |
| Densidade | 3260 kg m-3 |
| Ponto de fusão |
2200 °C |
| Ponto de ebulição |
2517 °C |
| Condutividade térmica | 140–180 W m-1 K-1 |
| Termoquímica | |
| Capacidade calorífica molar Cp 298 |
740 J Kg-1 K-1 |
| Compostos relacionados | |
| Outros aniões/ânions | Fosfeto de alumínio Óxido de alumínio Carbeto de alumínio |
| Outros catiões/cátions | Nitreto de boro Nitreto de gálio Nitreto de magnésio Nitreto de silício |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O nitreto de alumínio é um composto químico de fórmula AlN. Possui alta condutividade térmica, resistência mecânica e estabilidade estrutural, mesmo em altas temperaturas. É utilizado como cerâmica semicondutora em dispositivos eletrônicos.
O nitreto de alumínio, AlN, é um material com excelentes propriedades mecânicas, térmicas, ópticas e eletrônicas e por isso apresentam um enorme potencial em diversas aplicações tecnológicas. Um exemplo disso é a alta velocidade de propagação de onda superficial, as excelentes propriedades piezelétricas, o excelente coeficiente de acoplamento eletromecânico, alta dureza, alto ponto de fusão e associado à estabilidade química a altas temperaturas (acima de 2000 ºC). Essas combinações excepcionais fazem do AlN um candidato atraente a ser aplicado em sensores de temperatura e pressão baseados em ondas acústicas superficiais, por exemplo. [2] [3]
O AlN pode ser usado como um substrato cerâmico para a elaboração de microcircuitos, principalmente na área aeroespacial, pois possui excelentes propriedades térmicas, como a dissipação térmica. O AlN também é aplicado nas janelas de transmissão de luz e nos dispositivos de emissão na região UV devido ao seu alto valor da largura de banda (~6,2 eV).[4]
Propriedades do Material[editar | editar código-fonte]
Estrutura Cristalina[editar | editar código-fonte]
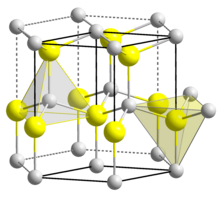
O nitreto de alumínio (AlN) é formado pela reação dos elementos de nitrogênio e alumínio. A estrutura do AlN é normalmente hexagonal fechada (hcp) do tipo wurtzita (2H) (hP4). O AlN com tal estrutura apresenta o maior coeficiente piezoelétrico (5 ∙ 10-2 CºN-1) entre os nitretos do grupo IIIA, tornando-o apropriado para aplicações como em microeletrônica. O AlN possui estrutura cristalográfica isomorfa e com alta resistividade (~1013 Ω∙cm).[5]
A figura da Wurtzite mostra a ligação atômica do AlN, onde o átomo de alumínio é ligado a quatro átomos de nitrogênio em um arranjo tetraédrico quatro vezes coordenado (sp3). O alumínio tem menor eletronegatividade do que o nitrogênio. No entanto, o elemento de nitrogênio tem o menor raio atômico. O nitreto de alumínio é excelente isolante elétrico porque seus elétrons estão fortemente ligados ao núcleo e não estão disponíveis para ligação metálica. [6]
O nitreto de alumínio pode ser encontrado em três formas: Wurtzita é a forma mais comum, porque pode ser encontrada em temperatura ambiente. Ambas as outras formas são as fases metaestáveis: a forma Zincblende é mais freqüentemente obtida quando o crescimento em Si (001) e GaAs (100) a granel, e a outra forma é a cúbica, conhecida como Rocksalt, que foram encontrados apenas em experimentos com alta pressão. A orientação de crescimento preferencial do Wurtzite está no eixo c. [7]
Ionicidade AlN[editar | editar código-fonte]
A ionicidade da ligação atômica é um parâmetro significante para obter informações sobre a estrutura cristalina do AlN. A ionicidade pode ser definida de acordo com a relação da equação abaixo, que é uma fração do iônico fiα em comparação com o covalente fih. A ionicidade do nitreto dos principais semicondutores é citada na Tabela 1.[9]
| Material | fi | fiP | fih |
| BN | 0,221 | 0,42 | 0,43 |
| AlN | 0,490 | 0,56 | 0,57 |
| GaN | 0,500 | 0,55 | 0,61 |
| InN | 0,578 | - | - |
A ionicidade Phillips é baseada na conexão entre as propriedades de ligação química da família ANB8-N de cristais e sua estrutura eletrônica de banda de energia. Analisando a energia iônica e covalente, Phillips encontrou uma correlação entre a ionicidade da ligação química e a estrutura cristalina adotada pelo composto que para valores reduzidos de (fi), consequentemente tem alta fc e então apresenta estrutura tetraédrica com coordenada zinco -blend (zb). A estrutura Wurtzita é obtida quando os valores de fi são altos. De acordo com Phillips[10] a ligação química observada presente nos semicondutores e a estabilização da estrutura do material entre a mistura de zinco e a wurtzita são o resultado do equilíbrio entre a ionicidade e a ligação química covalente.[10]
Parâmetros de Rede[editar | editar código-fonte]
O grupo de simetria do material é definido pela distância entre átomos na rede cristalina e o arranjo na estrutura e com isso é possível explicar as propriedades físicas e químicas de um material. Para definir a simetria de uma estrutura hexagonal é necessário definir os parâmetros de rede do AlN, a = 0,3112 nm e c = 0,4982 nm. A constante de rede e a simetria estão expostas na tabela abaixo.
| Material | Estrutura | Simetria | a (Å) | c (Å) |
| c-BN | zb | F_43m(Td) | 3,6155 | - |
| h-BN | h | P63/mmc(D6h) | 2,5040 | 6,6612 |
| w-AlN | w | P63mm(C6v) | 3,112 | 4,982 |
| c-AlN | zb | F_43m(Td) | 4,38 | - |
| α-GaN | w | P63mc(C6v) | 3,1896 | 5,1855 |
| β-GaN | zb | F_43m(Td) | 4,52 | - |
| InN | W | P63mc(C6v) | 3,5848 | 5,760 |
Plano de Clivagem[editar | editar código-fonte]
Outro parâmetro que depende dos átomos dispostos na estrutura é o plano de clivagem, esta propriedade é mostrada na Tabela abaixo.
| Diamante | (111) |
| Blende | (110) |
| Wurtzita | (110), (110) |
| Cúbica | (100) |
Propriedades Mecânicas[editar | editar código-fonte]
Embora o AlN possua propriedades mecânicas significativas acima mencionadas, sua dureza (Dureza Vickers) é de 12 GPa, o módulo de elasticidade é de 315 GPa e a resistência à flexão está entre 590 - 970 MPa. Além disso, o nitreto de alumínio é capaz de se deformar plasticamente em alguns graus acima do dúctil a frágil. Além dessas propriedades mecânicas, o AlN possui alta temperatura e resistência à corrosão.
Propriedades Térmicas[editar | editar código-fonte]
As propriedades térmicas dos nitretos monocristais são baseadas no alto ponto de fusão (> 2000 ºC), porém o nitreto de alumínio é um material de difícil reprodução de crescimento dos monocristais. Assim, o ponto de fusão do AlN pode ser obtido com base nos parâmetros de rede usando a Equação 2. As propriedades térmicas básicas, como a temperatura de fusão, o calor específico e a temperatura de Debye de alguns nitretos semicondutores são mostradas na Tabela 4.[11]
sendo
a = parâmetro de rede para estruturas blend e cúbicas
a = aeef, aeef = para haxagonal
O AlN possui estabilidade térmica de até 2200 ºC, condutividade térmica de cerca de 320 W / mK e boa capacidade de metalização. [5] Apenas para comparação, a condutividade térmica do SiO2 é de 1,38 W / mK. Esta característica permite uma melhor dissipação de calor no dispositivo em que é aplicada, aumentando a eficiência e, consequentemente, a vida útil do dispositivo.[11]
| Material | Tm (K) | Cp (J/gk) | ΘD (K) |
| c-BN | 3,246 | 0,643 | 1,613 |
| h-BN | - | 0,805 | 323 |
| w-AlN | 3,487 | 0,28 | 988 |
| α-GaN | 2,791 | 0,42 | 821 |
| InN | 2,146 | 2,274 | 674 |
Propriedades Elétricas e Ópticas[editar | editar código-fonte]
Devido a estas propriedades térmicas, o nitreto de alumínio é o material mais apropriado para ser aplicado em dispositivos eletrônicos que exigem demanda de alta potência. A condutividade térmica de alguns nitretos é apresentada na Tabela de Condutividade.
| Material | Tm (K) |
| Si | 148 |
| GaAs | 54 |
| InP | 68 |
| c-BN | 749 |
| GaN | 130 |
| w-AlN | 285 |
| w-InN | 38,5; 45; 80; 176 |
| 6H-SiC | 390; 490 |
| 4H-SiC | 330 |
| Safira | 42 |
| Diamond | 2000; 2500 |
A metodologia para preparar amostras precisa de atenção porque pode interferir nas propriedades do material, como propriedades ópticas e elétricas, normalmente as impurezas encontradas são: O, Al2O3, Al2OC. As impurezas fazem com que propriedades elétricas como a resistividade variar em uma faixa muito grande de 1011 a 1013 Ω.cm. O AlN também possui uma das mais altas velocidades de ondas acústicas de superfície (SAW) (aproximadamente 5500 m/s), tornando-se um material atraente para a aplicação de circuitos integrados Si e na fabricação de dispositivos SAW.[11]
O efeito de impurezas no material também produz uma forte mudança na resistência dielétrica que varia de 1 a 6 MV / cm.[13][14]Normalmente, o valor típico do bandgap correspondente aos títulos Al-N é em torno de 670 cm-1 e pode ser diminuído com o recozimento pós-processamento, devido ao estreitamento da largura da banda vibracional que contribui para uma melhoria na cristalinidade do filme.[15] Os valores típicos de bandgap (~6,2 eV) também são afetados pela presença das impurezas no filme depositado. [16]
Referências
- ↑ «Aluminum Nitride». Accuratus
- ↑ Clement, M; Vergara, L; Sangrador, J; Iborra, E; Sanz-Hervás, A (abril de 2004). «SAW characteristics of AlN films sputtered on silicon substrates». Ultrasonics (em inglês). 42 (1-9): 403–407. doi:10.1016/j.ultras.2004.01.034
- ↑ Elmazria, O.; Bénédic, F.; El Hakiki, M.; Moubchir, H.; Assouar, M.B.; Silva, F. (fevereiro de 2006). «Nanocrystalline diamond films for surface acoustic wave devices». Diamond and Related Materials (em inglês). 15 (2-3): 193–198. doi:10.1016/j.diamond.2005.07.031
- ↑ Strite, S. (julho de 1992). «GaN, AlN, and InN: A review». Journal of Vacuum Science & Technology B: Microelectronics and Nanometer Structures. 10 (4). 1237 páginas. doi:10.1116/1.585897
- ↑ a b Firek, Piotr; Wáskiewicz, Michał; Stonio, Bartłomiej; Szmidt, Jan (1 de dezembro de 2015). «Properties of AlN thin films deposited by means of magnetron sputtering for ISFET applications». Materials Science-Poland. 33 (4): 669–676. ISSN 2083-134X. doi:10.1515/msp-2015-0095
- ↑ Pierson, Hugh O. (1996). Handbook of refractory carbides and nitrides : properties, characteristics, processing, and applications. Park Ridge, N.J.: Noyes Publications. ISBN 1591240921. OCLC 49708267
- ↑ Rodríguez-Clemente, R.; Aspar, B.; Azema, N.; Armas, B.; Combescure, C.; Durand, J.; Figueras, A. (outubro de 1993). «Morphological properties of chemical vapour deposited AlN films». Journal of Crystal Growth (em inglês). 133 (1-2): 59–70. doi:10.1016/0022-0248(93)90103-4
- ↑ Fu, Y.Q.; Luo, J.K.; Nguyen, N.T.; Walton, A.J.; Flewitt, A.J.; Zu, X.T; Li, Y.; McHale, G.; Matthews, A. (agosto de 2017). «Advances in piezoelectric thin films for acoustic biosensors, acoustofluidics and lab-on-chip applications». Progress in Materials Science (em inglês). 89: 31–91. doi:10.1016/j.pmatsci.2017.04.006
- ↑ a b c d e Adachi, Sadao (20 de março de 2009). Properties of Semiconductor Alloys (em inglês). Chichester, UK: John Wiley & Sons, Ltd. ISBN 9780470744383. doi:10.1002/9780470744383
- ↑ a b Phillips, J. C. (1 de julho de 1970). «Ionicity of the Chemical Bond in Crystals». Reviews of Modern Physics (em inglês). 42 (3): 317–356. ISSN 0034-6861. doi:10.1103/RevModPhys.42.317
- ↑ a b c Pelegrini, Marcus V.; Pereyra, Inés (2010). «Characterization of AlN films deposited by r.f. reactive sputtering aiming MEMS applications». physica status solidi c (em inglês). 7 (3-4): 840–843. ISSN 1610-1642. doi:10.1002/pssc.200982861
- ↑ Quay, Rüdiger. (2007). GaN electronics. Berlin: Springer. ISBN 9783540718925. OCLC 233973232
- ↑ Gerova, E.V.; Ivanov, N.A.; Kirov, K.I. (julho de 1981). «Deposition of A1N thin films by magnetron reactive sputtering». Thin Solid Films (em inglês). 81 (3): 201–206. doi:10.1016/0040-6090(81)90482-X
- ↑ Tsubouchi, K.; Mikoshiba, N. (setembro de 1985). «Zero-Temperature-Coefficient SAW Devices on AlN Epitaxial Films». IEEE Transactions on Sonics and Ultrasonics. 32 (5): 634–644. ISSN 0018-9537. doi:10.1109/T-SU.1985.31647
- ↑ Interrante, Leonard V. (1989). «Preparation and Properties of Aluminum Nitride Films Using an Organometallic Precursor». Journal of The Electrochemical Society (em inglês). 136 (2). 472 páginas. doi:10.1149/1.2096657
- ↑ Pastrňák, J.; Roskovcová, L. (1968). «Optical Absorption Edge of AIN Single Crystals». Physica Status Solidi (b) (em alemão). 26 (2): 591–597. doi:10.1002/pssb.19680260223



