Nitreto de boro
O nitreto de boro é um composto químico binário do boro, que apresenta fórmula molecular BN. É um composto que apresenta somente ligações covalentes.
O nitreto de boro é obtido junto com o óxido de boro reagindo-se o boro com oxigênio e nitrogênio do ar atmosférico, em temperaturas elevadas.
É um isolante elétrico, porém, conduz o calor tão bem quanto os metais. É empregado na obtenção de materiais tão duros quanto o diamante.
Nitreto de boro cúbico
[editar | editar código-fonte]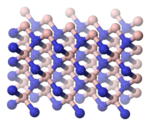
O nitreto de boro cúbico (c-BN) é um material artificial extremamente duro, mas com uma dureza inferior ao do diamante à temperatura ambiente, apesar de mais estável quimicamente. Atinge 2000 °C sem grandes perdas de dureza, enquanto o diamante já grafitiza em torno de 900 °C. Tal qual o diamante, o c-BN é um isolante elétrico e um excelente condutor de calor. É amplamente utilizado como um abrasivo para ferramentas industriais, em especial para a usinagem de peças de aços e materiais de grande dureza.
Fabricação
[editar | editar código-fonte]O c-BN é produzido a partir do tratamento do nitreto de boro hexagonal a altas pressões e temperaturas, da mesma forma que é produzido o diamante artificial a partir da grafite. A conversão direta de nitreto de boro hexagonal em nitreto de boro cúbico ocorre a pressões superiores a 18 GPa e temperaturas entre 1730 °C e 3230 °C. A adição de pequenas quantidades de óxido de boro pode reduzir a pressão requerida entre 4 GPa a 76 GPa, e a temperatura em torno de uns 1500 °C. Industrialmente, são utilizados diferentes tipos de catalisadores para provocar a reação, os quais variam segundo o método de produção. Exemplo: lítio, potássio ou magnésio, seus nitretos, água com compostos de amoníaco, etc.
Nitreto de boro hexagonal
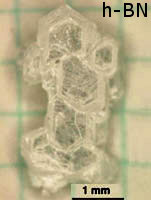
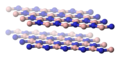
[editar | editar código-fonte]A forma cristalina mais estável é a hexagonal, também chamada de h-BN, α-BN, g-BN e nitreto de boro grafítico. O nitreto de boro hexagonal (grupo pontual = D3h; grupo espacial = P63/mmc) tem uma estrutura em camadas semelhante à do grafite. Dentro de cada camada, os átomos de boro e nitrogênio são ligados por fortes ligações covalentes, enquanto as camadas são mantidas juntas por forças fracas de van der Waals.
-
Forma hexagonal (h-BN)
No entanto, o “registro” entre as camadas dessas folhas é diferente do padrão observado no grafite, pois os átomos estão eclipsados, com os átomos de boro sobrepostos e acima dos átomos de nitrogênio. Esse registro reflete a polaridade local das ligações B-N, bem como as características N-doador/B-aceitador entre camadas. Da mesma forma, existem muitas formas metaestáveis que consistem em poliptipos empilhados de forma diferente. Portanto, o h-BN e o grafite são vizinhos muito próximos, e o material pode acomodar o carbono como um elemento substituinte para formar BNCs. Foram sintetizados híbridos BC6N, nos quais o carbono substitui alguns átomos de B e N.[4] A monocamada de nitreto de boro hexagonal é análoga ao grafeno, tendo uma estrutura de treliça em forma de favo de mel com quase as mesmas dimensões. Ao contrário do grafeno, que é preto e condutor elétrico, a monocamada de h-BN é branca e isolante. Ela foi proposta para ser usada como substrato isolante atômico plano ou como barreira dielétrica de tunelamento em eletrônica 2D.[5]
Nitreto de boro wurtzite
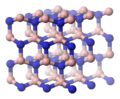
[editar | editar código-fonte]A forma wurtzita do nitreto de boro (w-BN; grupo pontual = C6v; grupo espacial = P63mc) tem a mesma estrutura da lonsdaleita, um raro polimorfo hexagonal de carbono. Como na forma cúbica, os átomos de boro e nitrogênio são agrupados em tetraedros.[6] Na forma wurtzita, os átomos de boro e nitrogênio são agrupados em anéis de 6 membros. Na forma cúbica, todos os anéis estão na configuração de cadeira, enquanto no w-BN os anéis entre as “camadas” estão na configuração de barco. Relatórios otimistas anteriores previam que a forma wurtzita era muito forte e foi estimada por uma simulação como tendo uma força 18% maior do que a do diamante. Como existem apenas pequenas quantidades do mineral na natureza, isso ainda não foi verificado experimentalmente.[7] Sua dureza é de 46 GPa, um pouco mais dura do que os boretos comerciais, mas mais suave do que a forma cúbica do nitreto de boro.[8]
-
Forma de wurtzita (w-BN)
Estabilidade térmica
[editar | editar código-fonte]O BN hexagonal e cúbico (e provavelmente o BN wurtzita) apresentam estabilidade química e térmica notáveis. Por exemplo, o h-BN é estável à decomposição em temperaturas de até 1.000 °C no ar, 1.400 °C no vácuo e 2.800 °C em uma atmosfera inerte. A reatividade do h-BN e do c-BN é relativamente semelhante, e os dados do c-BN estão resumidos na tabela abaixo.
| Sólido | Ambiente | Ação | Temperatura limite (°C) |
|---|---|---|---|
| Mo | vácuo de 10−2 Pa | Reação | 1360 |
| Ni | vácuo de 10−2 Pa | Umidificação | 1360 |
| Fe, Ni, Co | Argônio | Reação | 1400-1500 |
| Al | vácuo de 10−2 Pa | Umidificação e reação | 1050 |
| Si | vácuo de 10−3 Pa | Umificação | 1500 |
| Cu, Ag, Au, Ga, In, Ge, Sn | vácuo de 10−3 Pa | Sem umidificação | 1100 |
| B | - | Sem umidificação | 2200 |
| Al2O3 + B2O3 | vácuo de 10−2 Pa | Sem reação | 1360 |
A estabilidade térmica do c-BN pode ser resumida da seguinte forma:
- No ar ou no oxigênio: A camada protetora de B2O3 impede a oxidação adicional a ~1300 °C; não há conversão para a forma hexagonal a 1400 °C.
- Em nitrogênio: alguma conversão para h-BN a 1525 °C após 12 h.
- No vácuo (10-5 Pa): conversão em h-BN a 1550-1600 °C.
Ver também
[editar | editar código-fonte]Referências
- ↑ a b Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie, 102. Auflage, Berlin 2007, ISBN 978-3-11-017770-1.
- ↑ David R. Lide (2009). CRC Handbook of Chemistry and Physics 90. ed. [S.l.]: Taylor & Francis. ISBN 978-1-4200-9084-0
- ↑ Base de dados Nitreto de boro por AlfaAesar, consultado em 2. Februar 2010 ..
- ↑ Kawaguchi, Masayuki; Kuroda, Shinya; Muramatsu, Yasuji (maio de 2008). «Electronic structure and intercalation chemistry of graphite-like layered material with a composition of BC6N». Journal of Physics and Chemistry of Solids (em inglês) (5-6): 1171–1178. doi:10.1016/j.jpcs.2007.10.076. Consultado em 20 de julho de 2024
- ↑ Ba, Kun; Jiang, Wei; Cheng, Jingxin; Bao, Jingxian; Xuan, Ningning; Sun, Yangye; Liu, Bing; Xie, Aozhen; Wu, Shiwei (3 de abril de 2017). «Chemical and Bandgap Engineering in Monolayer Hexagonal Boron Nitride». Scientific Reports (em inglês) (1). ISSN 2045-2322. doi:10.1038/srep45584. Consultado em 20 de julho de 2024
- ↑ Silberberg, Martin S.; Weberg, Elizabeth Bent (2009). Chemistry: the molecular nature of matter and change 5th ed ed. Boston: McGraw-Hill
- ↑ Griggs, Jessica (maio de 2014). «Scotland: How to build a start-up nation». New Scientist (2971): 13–14. ISSN 0262-4079. doi:10.1016/s0262-4079(14)61041-1. Consultado em 20 de julho de 2024
- ↑ Brazhkin, Vadim V.; Solozhenko, Vladimir L. (7 de abril de 2019). «Myths about new ultrahard phases: Why materials that are significantly superior to diamond in elastic moduli and hardness are impossible». Journal of Applied Physics (em inglês) (13). ISSN 0021-8979. doi:10.1063/1.5082739. Consultado em 20 de julho de 2024
- ↑ Beiss, P.; Ruthardt, R.; Warlimont, H., eds. (2002). Powder Metallurgy Data. Refractory, Hard and Intermetallic Materials. Col: Landolt-Börnstein - Group VIII Advanced Materials and Technologies (em inglês). 2A2. Berlin/Heidelberg: Springer-Verlag