Ácido salicílico: diferenças entre revisões
| Linha 37: | Linha 37: | ||
:[[Imagem:Kolbe-Schmitt.png|left|400px]]<br clear=left/> |
:[[Imagem:Kolbe-Schmitt.png|left|400px]]<br clear=left/> |
||
Pode ser também preparado pela [[hidrólise]] da [[Aspirina]] (ácido acetilsalicílico)<ref>{{cite web | title=Hydrolysis of ASA to SA | url=http://www.crscientific.com/article-aspirin.html | accessdate= 31 julho | accessyear=2007 }} {{en}}</ref> ou [[salicilato de metila]] (óleo de Wintergreen) com um forte ácido ou base. |
Pode ser também preparado pela [[hidrólise]] da [[Aspirina]] (ácido acetilsalicílico)<ref>{{cite web | title=Hydrolysis of ASA to SA | url=http://www.crscientific.com/article-aspirin.html | accessdate= 31 julho | accessyear=2007 }} {{en}}</ref> ou [[salicilato de metila]] (óleo de Wintergreen) com um forte ácido ou base. |
||
== Análise == |
== Análise == |
||
Revisão das 18h48min de 16 de abril de 2009
| Ácido salicílico Alerta sobre risco à saúde | |
|---|---|

| |

| |
| Nome IUPAC | 2-Hydroxybenzoic acid |
| Identificadores | |
| Número CAS | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C7H6O3 |
| Massa molar | 138.123 g/mol |
| Densidade | 1.44 g/cm³ (at 20 °C) |
| Ponto de fusão |
159 °C |
| Ponto de ebulição |
211 °C (2666 Pa) |
| Compostos relacionados | |
| Compostos relacionados | Salicilato de metila, ácido benzóico, fenol, Aspirina, ácido 4-hidroxibenzóico, salicilato de magnésio, subsalicilato de bismuto (Pepto Bismol), ácido sulfossalicílico |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O ácido salicílico é um Beta-Hidroxiácido (ß-Hidroxiácido) com propriedades queratolíticas (esfoliantes) e antimicrobianas, o que significa que afina a camada espessada da pele e age evitando a contaminação por bactérias e fungos oportunistas. É um ácido utilizado no tratamento de pele hiperqueratótica, isto é, super espessada, em condições de descamação como: caspa, dermatite seborréica, ictiose, psoríase e acne, problemas que atingem facilmente a ala masculina. É caracterizado ainda por ser um regularizador da oleosidade e também um antiinflamatório potencial. A grande vantagem deste ácido é que apresenta um bom poder esfoliativo e também uma acção hidratante, cuja característica principal é a capacidade de penetração nos poros ajudando na remoção da camada queratinizada com uma acção irritante muito menor que os outros ingredientes. Diversos trabalhos têm referido a ação favorável do ácido salicílico em acne, especialmente em suas formas iniciais, não-inflamatórias, por seu efeito comedolítico e esfoliante, com resultados superiores aos do peróxido de benzoíla. É solúvel no álcool e parcialmente na água fria. Contra acne, tem sido utilizado em sabões, detergentes, loções tônicas, compressas, géis e emulsões fluidas, em concentrações que variam de 0,5 a 2,%. É considerado um hidroxiácido de fundamental importância para o melhoramento da aparência da pele envelhecida. Num recente congresso de Dermatologia da American Academy of Dermatology realizado em São Francisco, ficou confirmado que o Beta-Hidroxiácido - Ácido Salicílico - representa a próxima geração de produtos para o tratamento do envelhecimento cutâneo, pois melhora a aparência da pele foto-envelhecida, com baixa irritação, quando comparado com o ácido glicólico.
O ácido salicílico foi originalmente descoberto devido às suas acções antipirética e analgésica. Desde 400 a.C, que se sabe que a casca do salgueiro possuía estas propriedades. Em 1827, o seu princípio ativo, a salicilina, foi isolado. Dele se extrai o álcool salicílico, que pode ser oxidado para o ácido salicílico.
Porém, descobriu-se depois que este ácido pode ter uma acção corrosiva nas paredes do estômago. Para contornar isto foi adicionado um radical acetil à hidroxila ligada directamente ao anel aromático, dando origem a um éster de acetato, chamado de ácido acetil-salicílico (AAS), menos corrosivo mas também menos potente.
Produção
O ácido salicílico é biosintetizado do amino ácido fenilalanina.
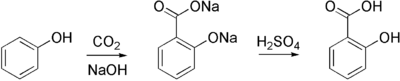
O salicilato de sódio é comercialmente preparado por tratar fenóxido de sódio com uma alta pressão de dióxido de carbono a alta temperatura via a reação de Kolbe-Schmitt. A acidificação da solução do produto dá o ácido salicílico:
Pode ser também preparado pela hidrólise da Aspirina (ácido acetilsalicílico)[1] ou salicilato de metila (óleo de Wintergreen) com um forte ácido ou base.
Análise
Com ferro (III) em solução aquosa dá uma cor vermelha característica.
Isso se dá porque o ácido salicílico é um enol de um β-ácido quetocarbônico e portanto forma complexos de cor avermelhada à púrpura com sais de ferro (III):
Este tri(quelado) complexo forma-se mais rapidamente em solução básica.
Aplicações
- Fabricação de aspirina na indústria medicinal.
- Produção de salicilatos na indústria química (ver abaixo).
- Iniciador e agente solubilizante na manufatura de colorantes e pastas de impressão na indústria têxtil.
- Preservante na indústria alimentar (depende da legislação).
- Ingrediente em numerosas preparações medicinais e cosméticas.
Especialmente por ser b-hidroxi-ácido com propriedades queratolíticas (dissolve a queratina) e antimicrobianas. Como queratolítico ele diminui a espessura da pele e atua contra a contaminação de bactérias e fungos oportunistas.
É utilizado com este fim, para o tratamento de pele hiperqueratótica, que significa com exagerada produção e acúmulo de queratina, em diversas condições de descamação como: caspa, dermatite seborréica, ictiose, psoríase e acne.
Caracteriza-se ainda por ser um regularizador da oleosidade e também um agente potencialmente antiinflamatório.
Ésteres do ácido salicílico
Reagindo ácido salicílico com álcoois e fenóis, obtem-se ésteres deste ácido, que são chamados salicilatos.
Entre estes, os principais e mais úteis são:
- Éster metílico do do ácido salicílico, ou salicilato de metila.
- Éster benzílico do ácido salicílico, ou salicilato de benzila.
- Fórmula: C14H12O3
- Massa molar: 228,25 g/mol
- Número CAS: 118-58-1
- Ponto de fusão: 24 °C
- Ponto de Ebulição: 211 °C
- Éster isobutílico do ácido salicílico, ou salicilato de isobutila.
- Fórmula: C11H14O3
- Massa molar: 194,22 g/mol
- Número CAS: 23408-05-1
- Ponto de fusão: 6 °C
- Ponto de Ebulição: 262 °C
- Éster isopentílico do ácido salicílico, ou salicilato de isopentila.
- Fórmula: C12H16O3
- Massa molar: 208,25 g/mol
- Número CAS: 87-20-7
- Ponto de fusão: ?
- Ponto de Ebulição: 274-278 °C
- Éster fenílico do ácido salicílico, ou salicilato de fenila.
- Fórmula: C13H10O3
- Massa molar: 214,21 g/mol
- Número CAS: 118-55-8
- Ponto de fusão: 41-43 °C
- Ponto de Ebulição: 173 °C
Referências
- ↑ «Hydrolysis of ASA to SA». Consultado em 31 julho Parâmetro desconhecido
|accessyear=ignorado (|acessodata=) sugerido (ajuda); Verifique data em:|acessodata=(ajuda) (em inglês)