Clorossilano
Este artigo não cita fontes confiáveis. (Novembro de 2011) |
| Clorossilano Alerta sobre risco à saúde | |
|---|---|

| |
|
|
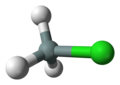
| Nome IUPAC | chlorosilane |
| Outros nomes | cloreto de silila |
| Identificadores | |
| Número CAS | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | H3ClSi |
| Massa molar | 66.56 g mol−1 |
| Compostos relacionados | |
| Outros aniões/ânions | Fluorossilano Bromossilano Iodossilano Mercaptossilano |
| Outros catiões/cátions | Clorometano |
| Cloro-silanos relacionados | Diclorossilano Triclorossilano Tetracloreto de silício (tetraclorossilano) |
| Compostos relacionados | Clorometilsilano |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Clorossilanos são um grupo de compostos químicos reativos contendo cloro, relacionados ao silano e usados em muitos processos químicos. Cada uma destas substâncias tem ao menos uma ligação silício-cloro.
Eles são preparados pelo processo Rochow, o qual envolve tratar silício com cloreto de hidrogênio a elevadas temperaturas na presença de um catalisador de cobre. A equação idealizada é:
- 2 Si +6 HCl → 2HSiCl3 + 2 H2,
Triclorossilano (HSiCl3) é o principal produto; diclorossilano (H2SiCl2) e tetracloreto de silício (SiCl4) são obtidos como produtos intermediários.
Todos os clorossilanos reagem com água produzindo cloreto de hidrogênio. O grupo hidroxila restante liga-se ao silício, inicialmente formando um grupo silol (análogo ao álcool). Em geral, este irá eventualmente ligar-se a uma superfície de um óxido sólido ou reagir com outra molécula de clorossilano ou silol. Nos últimos casos, o oxigênio forma uma ligação entre dois átomos de silício, análogo à ligação dos éteres em química orgânica, e idêntica à ligação no dióxido de silício.
Tetracloreto de silício (SiCl4) e triclorossilano (HSiCl3) são intermediários na produção de silício ultrapuro na indústria de semicondutores. Clorossilanos obtidos do silício bruto são purificados por técnicas de destilação fracionada e então reduzidos com hidrogênio para dar silício de 99.999999999 % (11 noves) de pureza.
Clorossilanos orgânicos são frequentemente usados como revestimentos para superfícies de sílica e vidros, e na produção de polímeros de silicone (polisiloxano). Quando fenil clorossilanos e muitos outros podem ser usados, metilsiloxanos são produzidos em maiores quantidades.
Metil clorossilanos têm de um a três grupos metil. No caso de diclorodimetilsilano, dois átomos de cloro são disponíveis, tanto que uma reação com excesso de água produz uma cadeia linear de ligações como as de éteres entre os átomos de silício. Como em poliéteres, estas ligações flexíveis produzem um polímero elástico, polidimetilsiloxano (PDMS). Triclorometilsilanos podem ser usados para induzir ramificações e reticulação em moléculas de PDMS, enquanto clorotrimetilsilanos servem para finalizar as cadeias, limitando os peso moleculares.
Outras espécies formadoras de ácido, especialmente acetato, podem substituir o cloro em síntese de silicones com pequenas diferenças na química de finalização de polímeros. Estes análogos de clorossilanos são bastante comuns nos selantes e adesivos comercializados, e como precursores de silicone de grau médico, devido à sua reduzida toxicidade.
