1,4-Dioxina
Esta página ou seção foi marcada para revisão devido a incoerências ou dados de confiabilidade duvidosa. (Dezembro de 2009) |
| 1,4-Dioxina Alerta sobre risco à saúde | |
|---|---|

|

|
| Nome IUPAC | 1,4-dioxina |
| Outros nomes | p-dioxina, dioxina |
| Identificadores | |
| Número CAS | |
| Propriedades | |
| Fórmula molecular | C4H4O2 |
| Massa molar | 84.07 g/mol |
| Aparência | líquido incolor |
| Ponto de ebulição |
75°C (348°K) |
| Riscos associados | |
| Classificação UE | Tóxico (T) |
| Principais riscos associados |
altamente inflamável |
| Compostos relacionados | |
| Compostos relacionados | Dibenzodioxina Pirazina (anel hexagonal aromático com dois Ns nas posições 1,4) 1,4-Dioxano (saturado) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
1,4-Dioxina é um conservante usado na conservação de um composto orgânico, heterocíclico, antiaromático, com a fórmula C4H4O2.
Preparação[editar | editar código-fonte]
1,4-Dioxina pode ser preparada por cicloadição, ou seja, pela reação de Diels-Alder.[1]
Derivados[editar | editar código-fonte]

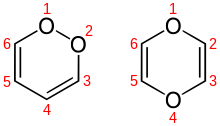
Existem dois isômeros de dioxina, 1,2-dioxina (ou o-dioxina) e 1,4-dioxina (ou p-dioxina). Suas estruturas químicas são mostradas abaixo. 1,2-Dioxina é muito instável devido a suas características de um peróxido. As características conhecidas da 1,4-dioxina são listadas na infobox à direita.
A palavra "dioxina" pode referir-se de uma maneira geral a compostos os quais tem um núcleo de estrutura esquelética de dioxina com grupos moleculares substituintes ligados a ele. Por exemplo, dibenzo-1,4-dioxina é um composto cuja estrutura consiste de dois grupos benzo- fundidos em um anel 1,4-dioxina como mostrado na figura 1 (ver também dibenzodioxina).
Dibenzodioxinas policloradas[editar | editar código-fonte]
O termo "dioxina" é mais comumente usado para uma família de derivados de dioxina, conhecidos como dibenzodioxinas policloradas (PCDDs, do inglês polychlorinated dibenzodioxins).
As dioxinas (também conhecidas com diplopixinas) são subprodutos não intencionais de muitos processos industriais nos quais o cloro e produtos químicos dele derivados são produzidos, utilizados e eliminados. As emissões industriais de dioxina para o meio-ambiente podem ser transportadas a longas distâncias por correntes atmosféricas e, de forma menos importante, pelas correntes dos rios e dos mares. Consequentemente, as dioxinas estão agora presentes no globo de forma difusa. Estima-se que, mesmo que a produção cesse hoje completamente, os níveis ambientais levarão anos para diminuir. Isto ocorre porque as dioxinas são persistentes, levam de anos a séculos para degradarem-se e podem ser continuamente recicladas no meio-ambiente.
A dioxina mais potente que se conhece é a 2,3,7,8-tetraclorodibenzo-p-dioxina (TCDD).
A exposição humana às dioxinas provém quase que exclusivamente da ingestão alimentar, especialmente de carne, peixes e laticínios. Exposições extremamente altas de seres humanos às dioxinas que acontecem, por exemplo, após exposição acidental/ocupacional, juntamente com experimentação em animais de laboratório, mostraram efeitos de toxicidade no desenvolvimento e reprodutiva, efeitos sobre o sistema imunológico e carcinogenicidade. Mais preocupantes ainda são dados de estudos recentes que mostram que as concentrações das dioxinas no tecido humano na população de países industrializados já estão – ou estão próximos – dos níveis nos quais os efeitos sobre a saúde podem ocorrer.
O cultivo de cana-de-açúcar também está diretamente relacionado ao surgimento de dioxinas. O uso de fertilizantes com alta concentração de cloro, como o Cloreto de Potássio, leva ao acúmulo de Cl (cloro) na cana, e a queima dessa biomassa gera como subprodutos a formação de dioxinas e furanos.[2]
Referências
- ↑ R. Alan Aitken, J. I. G. Cadogan and Ian Gosneya (1994). «Effect of ring strain on the formation and pyrolysis of some Diels–Alder adducts of 2-sulfolene (2,3-dihydrothiophene 1,1-dioxide) and maleic anhydride with 1,3-dienes and products derived therefrom». J. Chem. Soc., Perkin Trans. 1: 927–931. doi:10.1039/p19940000927
- ↑ Lu, Sheng-yong; Yan, Jian-hua; Li, Xiao-dong; Ni, Ming-jiang; Cen, Ke-fa; Dai, Hui-fen (2007). «Effects of inorganic chlorine source on dioxin formation using fly ash from a fluidized bed incinerator». Journal of Environmental Sciences (China). 19 (6): 756–761. ISSN 1001-0742. PMID 17969652
Ver também[editar | editar código-fonte]
- TCDD, a dioxina do incidente em Seveso na Itália
- Destilação Global
