Difenilamina
| Difenilamina Alerta sobre risco à saúde | |
|---|---|
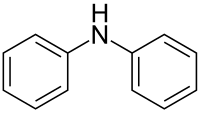
| |
| Nome IUPAC | Diphenylamine |
| Outros nomes | N-Fenilbenzenamina; N-Fenil Anilina; DPA; Anilinobenzeno; (fenilamino)benzeno; N,N-difenilamina; big dipper; C.I. 10355; fenilbenzenamina; Difenilamina; |
| Identificadores | |
| Número CAS | |
| Número RTECS | 9 |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C12H11N |
| Massa molar | 169.23 g/mol |
| Aparência | cristais brancos |
| Densidade | 1.2 g/cm³ |
| Ponto de fusão |
53 °C (326 K) |
| Ponto de ebulição |
302 °C (575 K) |
| Solubilidade em água | Levemente |
| Riscos associados | |
| Principais riscos associados |
Tóxico. Possível mutagênico. Possível teratogênico. Nocivo em contato com pele, e se ingerido ou inalado. Irritante. |
| NFPA 704 | |
| Frases R | R23 R24 R25 R33 R50 R53 |
| Frases S | S36 S37 S45 S60 S61 |
| Ponto de fulgor | 152°C |
| Compostos relacionados | |
| Outros aniões/ânions | Fenoxibenzeno (éter fenílico) |
| Amina relacionados | Anilina Trifenilamina 4-Aminobifenil (isômero) 4-Aminodifenilamina Ácido fenâmico (ácido 2-(fenilamino)benzoico) |
| Compostos relacionados | Difenilmetano Azobenzeno (Ph-N=N-Ph) Difenilfosfina |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Difenilamina é o composto orgânico com a fórmula (C6H5)2NH. É um sólido incolor, mas amostras são frequentemente amarelas devido a impurezas oxidadas.[1]
Preparação e reatividade[editar | editar código-fonte]
Difenilamina é produzida pela deaminação térmica de anilina sobre óxido catalisador:
- 2 C6H5NH2 → (C6H5)2NH + NH3
É uma base fraca, com uma KB de 10−14. Com ácidos fortes, forma sais solúveis em água.
Referências[editar | editar código-fonte]
- ↑ P. F. Vogt, J. J. Gerulis, “Amines, Aromatic” in Ullmann’s Encyclopedia of Industrial Chemistry 2005, Wiley-VCH, Weinheim.

