Metil-lítio
| Metil-lítio Alerta sobre risco à saúde | |
|---|---|

| |
| Nome IUPAC | Metil-lítio |
| Outros nomes | metaneto de lítio |
| Identificadores | |
| Número CAS | |
| PubChem | |
| Número EINECS | |
| ChemSpider | |
| ChEBI | |
| SMILES |
|
| Referência Beilstein | 3587162 |
| Referência Gmelin | 288 |
| Propriedades | |
| Fórmula química | CH3Li |
| Massa molar | 21.98 g mol-1 |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Metil-lítio é um reagente de organolítio de fórmula empírica CH3Li. Este composto organometálico do bloco s adota uma estrutura oligomérica em solução e em estado sólido. É um composto altamente reativo, invariavelmente usado como solução em éter, é um reagente em síntese orgânica, bem como em química organometálica. Operações envolvendo metil-lítio requerem condições anidras, porque o composto é reage fortemente com a água. Oxigênio e dióxido de carbono também são incompatíveis com MeLi. Geralmente, o metil-lítio não é preparado, mas comprado como solução em vários éteres.
Síntese[editar | editar código-fonte]
Na síntese direta, brometo de metila é tratado com uma suspensão de lítio em éter dietílico.
- 2 Li + MeBr → LiMe + LiBr
O brometo de lítio forma um complexo com o LiMe. A forma mais disponível comercialmente de LiMe consiste desse complexo. Metil-lítio livre de haleto é preparado a partir do cloreto de metila.[1] O cloreto de lítio se precipita do éter dietílico por não formar um complexo forte com o metil-lítio. O filtrado consiste de metil-lítio relativamente puro.
Reatividade[editar | editar código-fonte]
LiMe é ao mesmo tempo fortemente básico e altamente nucleofílico devido à carga parcial negativa no carbono e, portanto, particularmente reativo para doadores de elétrons e prótons. Ao contrário do n-BuLi, MeLi reage muito lentemente com THF a temperatura ambiente, e soluções em éter são indefinidamente estáveis. Água e álcoois reagem violentamente. Muitas reações envolvendo metil-lítio são conduzidas abaixo da temperatura ambiente. Embora MeLi possa ser usado para deprotonações, n-butil-lítio é mais empregado por ser menos caro e mais reativo.
Metil-lítio é muito usado como o equivalente sintético (sínton) do ânion metil. Por exemplo, cetonas reagem formando álcoois terciários em um processo de duas etapas:
- Ph2CO + MeLi → Ph2C(Me)OLi
- Ph2C(Me)OLi + H+ → Ph2C(Me)OH + Li+
Haletos não-metálicos são convertidos a compostos de metila pelo metil-lítio:
- PCl3 + 3 MeLi → PMe3 + 3 LiCl
Tais reações empregam mais comumente os haletos de metilmagnésio (reagentes de Grignard), que são quase sempre igualmente efetivos, e mais econômicos ou mais facilmente preparados in situ.
Também reage com dióxido de carbono para formar acetato de lítio:
- CH3Li + CO2 → CH3CO2-Li+
Metilcompostos de metais de transição podem ser preparados pela reação de MeLi com haletos desses metais. Especialmente importante é a formação de compostos de organocobre (reagentes de Gilman), dos quais o mais útil é o dimetilcuprato de lítio. Este reagente é largamente usado em substituições nucleofílicas de epóxidos, haletos de alquila e sulfonatos de alquila, bem como para conjugar adições a carbonilcompostos α,β-insaturados pelo ânion metil.[2] Vários outros metilcompostos de metais de transição têm sido preparados.[3]
- ZrCl4 + 6 MeLi → Li2ZrMe6 + 4 LiCl
Estrutura[editar | editar código-fonte]
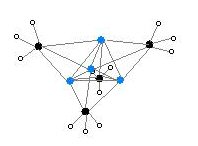
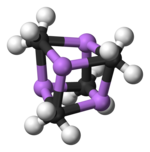
Duas estruturas foram verificadas por cristalografia de raios X e espectroscopia NMR de 6Li, 7Li, e 13C. O cluster tetramérico consiste de um cubano distorcido, com os átomos de lítio e carbono em arestas alternadas. A distância Li---Li é de 2.68 Å, quase idêntica à da ligação Li-Li no gasoso dilítio. A distância C-Li é de 2.31 Å. O carbono está ligado a três átomos de hidrogênio e três de Li. A não-volatilidade do (MeLi)4 e sua insolubilidade em alcanos resulta do fato de que os clusteres interagem via inter-cluster interação agóstica. Diferentemente do cluster mais volumoso (terc-butil-Li)4, no qual interações intercluster são impedidas por efeitos estéricos, é volátil e solúvel em alcanos.[4]
Código de cores: Li- azul C- preto H- branco
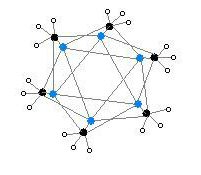
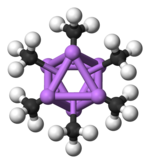
A forma hexamérica aparece como prismas hexagonais com átomos de Li e C se alternando nas arestas.
Código de cores: Li- azul C- preto H- branco
O grau de agregação, "n" para (MeLi)n, depende do solvente e da presença de aditivos (como brometo de lítio). Solventes hidrocarbônicos como o benzeno[5] favorecem a formação do hexâmero, e solventes etéreos favorecem o tetrâmero.
Ligação[editar | editar código-fonte]
Esses clusters são considerados "elétron-deficientes," isto é, eles não seguem a regra do octeto, ao contrário da maioria dos compostos orgânicos. O hexâmero é um compsto de 30 elétrons (30 elétrons de valência). Se 18 elétrons são alocados para as ligações fortes C-H, restam 12 elétrons para as ligações Li-C e Li-Li. São seis elétrons para seis ligações metal-metal e um elétron por interação metil-η3 lítio.
A força da ligação C-Li foi estimada em cerca de 57 kcal/mol por meio de medidas espectroscópicas de IR.[5]
Referências
- ↑ Lusch, M. J.; Phillips, M. V.; Sieloff, W. V.; Nomura, G. S.; House, H. O. (1990). «Preparation of Low-Halide Methyllithium». Org. Synth.; Coll. Vol., 7
- ↑ Organocopper Reagents: Substitution, Carbo/Metallocupration, and Other Reactions. Lipshutz, B. H.; Sengupta, S. Organic Reactions 1992, 41, 135-631.
- ↑ Morse, P. M.; Girolami, G. S. "Are d0 ML6 Complexes Always Octahedral? The X-ray Structure of Trigonal-Prismatic [Li(tmed)]2[ZrMe6]" Journal of the American Chemical Society 1989, 111, 4114-6. doi:10.1021/ja00193a061
- ↑ Elschenbroich, C. ”Organometallics” (2006) Wiley-VCH: Weinheim. ISBN 978-3-29390-6
- ↑ a b Brown, Theodore L.; Rogers, Max T. (1957). «The Preparation and Properties of Crystalline Lithium Alkyls». Journal of the American Chemical Society. 79 (8): 1859–1861. doi:10.1021/ja01565a024 DOI: 10.1021/ja01565a024
| Parte ou a integralidade do conteúdo desta página resulta da tradução de uma página originalmente presente numa Wikipédia noutra língua. A página correspondente pode ser conferida aqui. As fontes não foram verificadas. |