2,4-Dinitrofenol
| 2,4-Dinitrofenol Alerta sobre risco à saúde | |
|---|---|

| |

| |
| Nome IUPAC | 2,4-dinitrofenol |
| Outros nomes | Solfo Black |
| Identificadores | |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C6H4N2O5 |
| Massa molar | 184.106 |
| Densidade | 1.683 g/cm³ |
| Ponto de fusão |
108 °C |
| Ponto de ebulição |
113 °C |
| Riscos associados | |
| NFPA 704 | |
| Frases R/S | R: 10, 23, 24, 25, 33 S: 1, 2, 28, 37, 45 |
| Compostos relacionados | |
| Compostos aromáticos relacionados | 4-Nitrofenol Ácido pícrico (2,4,6-Trinitrofenol) Ácido 3,5-dinitrosalicílico |
| Compostos relacionados | Diazodinitrofenol |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O 2,4-dinitrofenol (DNP'), é um composto orgânico, nitroderivado, de fórmula C6H4N2O5.
Trata-se de um sólido inodoro e de cor amarela. É utilizado no fabrico de tintas, conservantes de madeira, herbicidas, pesticidas e explosivos[1][2].
Os dinitrofenóis são uma classe de compostos, dos quais existem seis membros, isômeros de posição, que não ocorrem naturalmente e são todos sintéticos.
Não deve ser confundido com o radical 2,4-dinitrofenil da farmacologia e bioquímica, utilizado para a produção de vacinas e análises bioquímicas, também abreviado como DNP.
Durante os anos 30, o 2,4-DNP foi amplamente prescrito nos EUA como um fármaco para tratamento da obesidade. No entanto, no documento Federal Food, Drug and Cosmetic Act (EUA) de 1938, o 2,4-DNP foi descrito como uma substância "extremamente perigosa e imprópria para consumo humano" e o seu uso como fármaco foi proibido. Esta proibição surge no seguimento de relatos de efeitos adversos graves, como o aparecimento de cataratas e hipertermia, que pode levar à morte [1].
O 2,4-DNP é, atualmente, vendido através da Internet sob diferentes designações. Os produtos que se encontram disponíveis online estão maioritariamente direcionados para praticantes de culturismo, já que o 2,4-DNP favorece a perda de gordura mas mantém a massa muscular. É possível, através da Internet, adquirir grandes quantidades da substância, quer sob a forma de pó, comprimidos ou cápsulas[1].
É de salientar que, apesar de o 2,4-DNP ser publicitado como uma substância segura, os riscos da sua administração ultrapassam largamente os benefícios. O 2,4-DNP possui uma janela terapêutica muito estreita; isto é, o intervalo entre a dose “segura” e a dose tóxica é muito pequeno, sendo assim extremamente fácil entrar num estado de overdose [1].
Risco para a saúde[editar | editar código-fonte]
Como ficamos expostos?[editar | editar código-fonte]
A exposição ao 2,4-dinitrofenol pode ser acidental ou ocupacional, no caso de trabalhadores de empresas que usam ou produzem o composto, que incineram lixo/resíduos ou limpem locais onde este composto está presente. A exposição pode igualmente ocorrer através da contaminação ambiental[3].
Atualmente tem sido muito procurado com o objetivo de reduzir o peso/ massa gorda, sendo a venda feita online de forma ilícita.
Efeitos na saúde[editar | editar código-fonte]
A intoxicação por 2,4-Dinitrofenol, independentemente da duração do período de exposição, pode levar ao aumento das taxas metabólicas basais o que se traduz em aumento da temperatura corporal, fraqueza, mal-estar, dor de cabeça, aumento da transpiração, sede e dispneia, que pode evoluir para situações de hipertermia, perda de peso acentuada, com insuficiência respiratória e por fim morte [2] [4]
Mecanismo de Ação[editar | editar código-fonte]
É um veneno metabólico celular. Desacopla a fosforilação oxidativa através do transporte de prótons através da membrana mitocondrial, levando a um rápido consumo de energia sem a geração de ATP. O 2, 4 -dinitrofenol não interage diretamente com uma molécula alvo, mas exerce a sua ação influenciando negativamente o micro-ambiente biológico [5]. Como este composto não exerce a sua ação sobre um alvo específico, os seus efeitos não se restringem ao tecido adiposo, onde a sua ação seria pretendida [5].
Este xenobiótico é um desacoplador protonofórico, que se dissocia nos seus protões fenólicos na matriz mitocondrial, levando à dissipação do gradiente de protões dirigido para o exterior através da membrana mitocondrial interna. Desta forma, a síntese de ATP é inibida por ocorrer alteração do fluxo de protões, que é a força motriz para a atividade da ATP-sintetase. Além disso, também previne o uptake de fosfato inorgânico para a mitocôndria, que é necessário para a síntese de ATP, verificando-se acumulação dos iões fosfato no citosol das células [1][5][6]
O seu uso para a perda de peso prende-se com o facto de o 2,4-DNP conduzir à incapacidade das células restabelecerem as reservas de energia e, consequentemente, aumentar o metabolismo [7].
Comporta-se como um indicador de pH, apresentando ponto de virada a pH 2,8 a 4,0, quando vira de incolor a amarelado, sendo usado em solução saturada em água.[8][9]
Perfil ADME[editar | editar código-fonte]
Absorção[editar | editar código-fonte]
O 2,4-dinitrofenol é rapidamente adsorvido através do trato gastrointestinal, bem com pela pele e pulmões. O 2,4-dinitrofenol apresenta alguma lipofilidade com um pKa de 4,09 e é absorvido rapidamente por difusão passiva na forma não ionizada em zonas com pH ácido, como o estomago. O facto de apresentar baixo peso molecular (184,1 Da) favorece a sua absorção, nomeadamente através de canais transportadores de água localizados nas membranas celulares. Por via cutânea, verifica-se maior taxa de absorção quando este é vinculado num óleo do que quando está presente numa solução aquosa. A absorção via inalatória pode ocorrer quer por exposição ao composto na forma de pó ou na forma de vapor. Muitas vezes, quando um individuo é exposto via inalatória o composto também contacta com a pele, ocorrendo assim absorção por ambas as vias [2].
Metabolização[editar | editar código-fonte]
O 2, 4-dinitrofenol é metabolizado por redução dos grupos amino, formando compostos com menor toxicidade[2].
As enzimas nitrorredutases podem ser encontradas maioritariamente no citosol das células e nos microssomas, verificando-se maior atividade destas enzimas no citosol. Este processo de metabolização requer a presença de NADPH. O o-nitrofenol inibe competitivamente a metabolização do 2, 4-DNP, sugerindo que competem pelo mesmo local ativo da enzima nitrorredutase. Alguns estudos indicam que o 2,4-DNP também pode ser conjugado com ácido glucurônico ou sulfato no fígado e, em seguida, ser excretado na urina [2]. Após exposição ao 2,4-dinitrofenol, são encontrados na urina diferentes compostos resultantes do seu metabolismo, bem como o próprio composto, eliminado sem sofrer metabolização. Entre esses compostos, encontram-se o 2-amino-4-nitrofenol, 4-amino-2-nitrofenol, 2,4-diaminofenol e outros compostos de nitrogênio, que podem ser produtos de conjugação por glucoronidação. O 2-amino-4-nitrofenol é o metabolito encontrado geralmente em maior quantidade [2].
Verifica-se significativa variação metabólica individual, observando-se o aumento da taxa metabólica média de 11% para cada 100 mg de DNP, quando tomado regularmente [1]. Estudos indicam que, quando exposição via oral, o tempo de semi-vida estimado é de 10,3 horas para o 2,4-DNP, para o 2-amino-4-nitrofenol de 46,2 horas e para o 4-amino-2-nitrofenol de 25,7
Distribuição[editar | editar código-fonte]
Estudos em animais mostraram que uma porção do 2,4-DNP circula ligado a proteínas plasmáticas, sendo que a fração livre pode chegar a todos os órgãos e tecidos, como o fígado, os rins e olhos, onde aí poderá exercer os seus efeitos. Não ocorre armazenamento significativo deste xenobiótico nos tecidos após a absorção. O 2, 4-dinitrofenol apresenta capacidade de passar a barreira hematoaquosa entrando no humor aquoso, sendo responsável por efeitos cataratogênicos [2]
Excreção[editar | editar código-fonte]
O 2, 4-DNP é eliminado preferencialmente através da urina. Estudos indicam que a excreção do composto ocorre por difusão passiva, havendo também evidências de eliminação ativa por transportadores de ácidos orgânicos ao nível renal. O 2,4-dinitrofenol mostrou em estudos feitos em animais menor taxa de eliminação quando comparando com outros isómeros do dinitrofenol [10]. Em pessoas expostas via inalatória, que apresentavam transpiração abundante, verificou-se coloração amarela na pele, indicando que o 2,4-DNP sofre eliminação através do suor [2].
Síntese Orgânica do DNP[editar | editar código-fonte]
O DNP pode ser sintetizado partindo do fenol, de acordo com o mecanismo abaixo descrito:
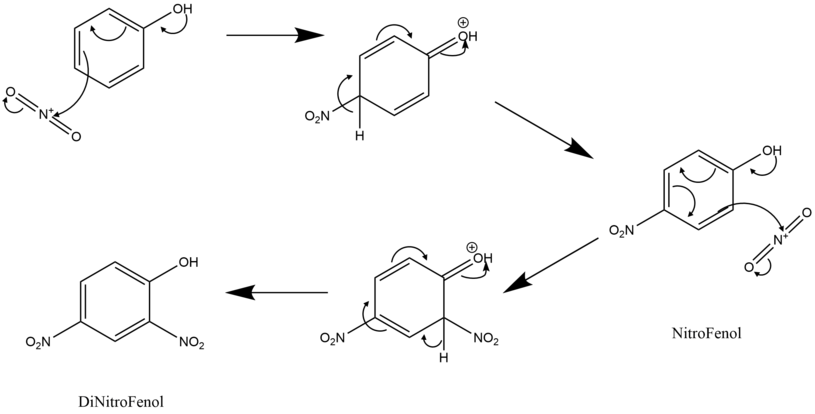
Referências
- ↑ a b c d e f Grundlingh J, Dargan PI, El-Zanfaly M, Wood DM (2011) 2,4-Dinitrophenol (DNP): A Weight Loss Agent with Significant Acute Toxicity and Risk of Death. Journal of Medical Toxicology 7(3):205-212
- ↑ a b c d e f g h ATSDR (1995) Toxicological Profile for Dinitrophenols.Disponível em: http://www.atsdr.cdc.gov/toxprofiles/tp64.pdf. Acedido a 26/05/2015
- ↑ ATSDR (1995) Public Health Statement for Dinitrophenols. Disponível em. http://www.atsdr.cdc.gov/PHS/PHS.asp?id=727&tid=132 Acedido a 22/05/15
- ↑ Wallace KB, Starkov AA (2000) Mitochondrial Targets of Drug Toxicity. Annual Review of Pharmacology and Toxicology Vol. 40:353-388
- ↑ a b c Sammons MF, Price DA (2014) Modulation of adipose tissue thermogenesis as a method for increasing energy expenditure. Bioorganic & Medicinal Chemistry Letters 24(2):425-429
- ↑ Klaassen C (2008) Mechanisms of Toxicity Casarett & Doull's Toxicology: The Basic Science of Poisons. 7th edn. McGraw-Hill
- ↑ Karl G. Hofbauer JRN, and Olivier Boss (2007) The Obesity Epidemic: Current and Future Pharmacological Treatments. Annual Review of Pharmacology and Toxicology Vol. 47:565-592
- ↑ Acid Base Indicators Arquivado em 16 de julho de 2011, no Wayback Machine. - ifs.massey.ac.nz (em inglês)
- ↑ Preparation of Acid-Base Indicators - www.csudh.edu
- ↑ U.S. National Library of Medicine (2012) HSDB: Dinitrophenol. Disponivel em http://toxnet.nlm.nih.gov/cgi-bin/sis/search2/f?./temp/~1ZWbsE:3 Acedido a 24/05/2015
Ligações externas[editar | editar código-fonte]
- «ToxFAQ about Dinitrophenols». Agency for Toxic Substances and Disease Registry. Setembro 1996. Consultado em 25 de abril de 2013
- General 2,4-dinitrophenol information.
Ver também[editar | editar código-fonte]
- Mais informações sobre 2,4-Dinitrofenol em: http://dnptoxicologia.wix.com/dinitrofenol
- 2,5-Dinitrofenol - um isômero de posição que é usado como indicador de pH.

