Decaborano
Este artigo não cita fontes confiáveis. (Junho de 2021) |
| Decaborano Alerta sobre risco à saúde | |
|---|---|
| |
| Outros nomes | decaborano tetradecahidreto de decaboro |
| Identificadores | |
| Número CAS | |
| Número EINECS | |
| ChemSpider | |
| SMILES |
|
| InChI | 1/B10H14/c11-5-1-2-3(1,5)7(2,9(3,5,11)13-7)
8(2)4(1,2)6(1,5)10(4,8,12-6)14-8/h1-10H |
| Propriedades | |
| Massa molar | 122.22 g/mol |
| Aparência | Cristais brancos |
| Ponto de fusão |
99.6 °C |
| Ponto de ebulição |
213 °C |
| Solubilidade em outros solventes | levemente em água fria. [1] |
| Riscos associados | |
| Temperatura de auto-ignição |
149 °C |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Decaborano, também chamado decaborano(14), é o borano de fórmula química B10H14. Este composto cristalino branco é um dos principais clusteres de hidreto de boro, como estrutura de referência e como precorsor para outros hidretos de boro.
Manuseio e propriedades[editar | editar código-fonte]
O decaborano 14 possui um forte odor característico, algumas vezes descrito como mofo ou intensamente amargo, parecido com chocolate que é exclusivo para boranos. As características físicas do decaborano-14 se assemelham às dos compostos orgânicos, tais como naftaleno e antraceno, na medida em que pode ser sublimado sob vácuo a temperaturas moderadas. A sublimação é o método comum de purificação. Como os compostos orgânicos, decaborano é altamente inflamável, mas, como outros hidretos de boro, ele queima com uma chama verde brilhante. Não é sensível ao ar úmido, embora hidrolisa em água fervente, liberando hidrogênio e dando uma solução de ácido bórico. É solúvel em água fria, bem como uma variedade de solventes não-polares e moderadamente polares.
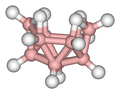
O esqueleto da estrutura do decaborano se assemelha a um octadecaedro incompleto. Cada um hidreto de boro tem hidrogênios ligados radialmente e quatro átomos de boro, perto da parte aberta do cluster possuem hidrogênios extra. Na linguagem da química cluster, a estrutura é classificada como "nido".
Sínteses e reações[editar | editar código-fonte]
é comumente sintetizado através da pirólise de clusters menores de hidreto de boro. Por exemplo, o aquecimento do diborano ou do pentaborano B5H9 dá decaborano, com perda de H2 [1].
O decaborano reage com bases de Lewis (L), tais como CH3CN e (CH3)2S, para formar derivados com a fórmula B10H12·2L. .
B10H14· + 2L → B10H12L2· H2 .
Essas espécies, que são classificados como clusters do tipo "aracno", por sua vez, reagem com o acetileno para dar um "closo" orto-carborano: .
B10H12L2 + C2H2 → C2B10H12 + 2L + H2 .
Ele é um ácido de Brønsted fraco. A eliminação de um próton gera o ânion [B10H13]-, com uma nova estrutura do tipo nido.
Aplicações[editar | editar código-fonte]
O decaborano não tem aplicações importantes, embora tenha sido frequentemente investigadas. Uma vez que a molécula se decompõe em um plasma, produzindo íons de boro monoatómico, o decaborano é potencialmente útil como um combustível para fusão aneutrônica, [2] e para a implantação de íons de boro de baixa energia na fabricação de semicondutores. Também foi considerado para a deposição assistida de plasma de vapor químico para a fabricação de filmes finos contendo boro. No estudo sobre a fusão, a habilidade do boro de absorver nêutrons tem levado ao uso desses filmes finos de boro para "boronizar" as paredes da câmara de vácuo do tokamak para reduzir a reciclagem de partículas e impurezas no plasma e melhorar o desempenho global. [ 3]
Decaborano também foi estudado como um aditivo para combustíveis especiais de alto desempenho de foguetes. Seus derivados foram investigados, como por exemplo o decaborano etílico. Um combustível de composição patenteada inclui o copolímero de decaborano com poliéster vinílico. Vinil-decaborano ("dekene") é preparado reagindo-se o decaborano com o acetileno [4].
Segurança[editar | editar código-fonte]
O decaborano, assim como o pentaborano, é uma toxina poderosa que afeta o sistema nervoso central, embora o decaborano seja menos tóxico que o pentaborano. Ele pode ser absorvido pela pele. Pode formar uma mistura explosiva com o tetracloreto de carbono, o que causou uma explosão, muitas vezes citada em uma fábrica de Malta, NY em 1948, quando CCl4 foi usado para limpar o equipamento [5].
Referências
Leitura posterior[editar | editar código-fonte]
- NIST Chemistry Webbook, decaborano, acessado em 23 de outubro de 2006. (em inglês)
- National Pollutant Inventory, Boro e compostos, acessado em 23 de outubro de 2006. (em inglês)
- Decaborano em síntese orgânica (em inglês)
- Webelements, Compostos de boro, acessado 23 de outubro de 2006. (em inglês)
