Hemo: diferenças entre revisões
m r2.7.3) (Robô: A adicionar: gl:Hemo |
|||
| Linha 4: | Linha 4: | ||
O grupo hemo possui um [[átomo]] de [[ferro]] ferroso "Fe++" para exercer a função de ligação com o [[oxigênio]] em [[Célula sanguínea|células sanguíneas]], parte se liga a um resíduo de histidina da globina e outra a uma molécula de oxigênio, a mioglobina possui um grupo heme na sua cadeia polipeptídica a hemoglobina possui quatro grupos heme. |
O grupo hemo possui um [[átomo]] de [[ferro]] ferroso "Fe++" para exercer a função de ligação com o [[oxigênio]] em [[Célula sanguínea|células sanguíneas]], parte se liga a um resíduo de histidina da globina e outra a uma molécula de oxigênio, a mioglobina possui um grupo heme na sua cadeia polipeptídica a hemoglobina possui quatro grupos heme. |
||
A sua ligação com oxigênio depende de uma pressão parcial de oxigênio determinada como P que corresponde a 50% dos seus sítios de ligações, a hemoglobina precisa de um P igual a 26mmHg para ocupar 50% dos seus sítios; a mioglobina como possui apenas um grupo heme, requer 1mmHg para ocupar P. Por isso sua importância, durante uma atividade física a concentração de oxigênio diminui e essas moléculas deixam a hemoglobina por essa diminuição de P, a mioglobina capta essas moléculas e transporta para os tecidos. |
A sua ligação com oxigênio depende de uma pressão parcial de oxigênio determinada como P que corresponde a 50% dos seus sítios de ligações, a hemoglobina precisa de um P igual a 26mmHg para ocupar 50% dos seus sítios; a mioglobina como possui apenas um grupo heme, requer 1mmHg para ocupar P. Por isso sua importância, durante uma atividade física a concentração de oxigênio diminui e essas moléculas deixam a hemoglobina por essa diminuição de P, a mioglobina capta essas moléculas e transporta para os tecidos. |
||
O succinato proveniente da descarboxilação do alfa cetoglutarato em conjunto com a glicina são as moléculas chave para a formação do grupo heme |
|||
{{esboço-bioquímica}} |
{{esboço-bioquímica}} |
||
{{Cofactores enzimáticos}} |
{{Cofactores enzimáticos}} |
||
Revisão das 17h38min de 8 de janeiro de 2013
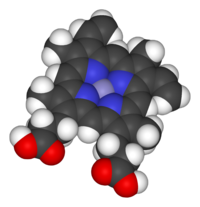
Hemo ou heme, é um grupo prostético que consiste de um átomo de ferro contido no centro de um largo anel orgânico heterocíclico chamado porfirina.
O grupo hemo possui um átomo de ferro ferroso "Fe++" para exercer a função de ligação com o oxigênio em células sanguíneas, parte se liga a um resíduo de histidina da globina e outra a uma molécula de oxigênio, a mioglobina possui um grupo heme na sua cadeia polipeptídica a hemoglobina possui quatro grupos heme. A sua ligação com oxigênio depende de uma pressão parcial de oxigênio determinada como P que corresponde a 50% dos seus sítios de ligações, a hemoglobina precisa de um P igual a 26mmHg para ocupar 50% dos seus sítios; a mioglobina como possui apenas um grupo heme, requer 1mmHg para ocupar P. Por isso sua importância, durante uma atividade física a concentração de oxigênio diminui e essas moléculas deixam a hemoglobina por essa diminuição de P, a mioglobina capta essas moléculas e transporta para os tecidos. O succinato proveniente da descarboxilação do alfa cetoglutarato em conjunto com a glicina são as moléculas chave para a formação do grupo heme
