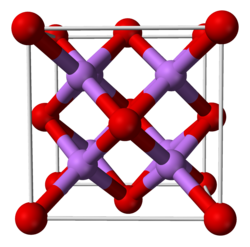
Óxido de lítio
Óxido de lítio (Li2O) ou lítia é um composto químico inorgânico.
Produção[editar | editar código-fonte]
Óxido de lítio é formado quando o lítio é queimado ao ar e combina-se com o oxigênio, ou pela decomposição térmica do peróxido de lítio ou do hidróxido de lítio:
Usos[editar | editar código-fonte]
Óxido de lítio é usado como um fundente em esmaltes cerâmicos; e cria colorações azuis com cobre e rosas com cobalto. Óxido de lítio reage com água e vapor e deve ser isolado deles.
Seu uso está também sendo investigado para valorações em espectroscopia de monitoramento de degradação de emissão não-destrutiva com sistemas de revestimento de barreira térmica. Ele pode ser adicionado como um co-dopante com ítria na cerâmica de zircônia para alto revestimento, sem um grande decréscimo na expectativa de vida em serviço do revestimento. A alta temperatura, o óxido de lítio emite um padrão espectral muito detectável, o qual aumenta em intensidade ao longo da degradação do revestimento. Implementação permitiria monitoramento in situ de tais sistemas, possibilitando um eficiente meio para predizer tempo de vida até a falha ou necessária manutenção.
Ver também[editar | editar código-fonte]
Referências
- ↑ a b c Base de dados Óxido de lítio por AlfaAesar, consultado em 15 de dezembro de 2010.
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg, Lehrbuch der Anorganischen Chemie.101. Auflage, de Gruyter, 1995, ISBN 3-11-012641-9, S. 1152.
- ↑ Georg Brauer (1978). Handbuch der Präparativen Anorganischen Chemie. II. [S.l.: s.n.] p. 951. ISBN 3-432-87813-3
Ligações externas[editar | editar código-fonte]
- «CeramicMaterials.Info entry» (em inglês)