Selenocisteína
Este artigo não cita fontes confiáveis. (Agosto de 2021) |
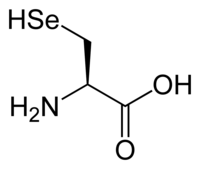
| Selenocisteína Alerta sobre risco à saúde | |
|---|---|
| |

| |
| Nome IUPAC | L-Selenocysteine |
| Identificadores | |
| Número CAS | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C3H7NO2Se |
| Massa molar | 168.053 g/mol |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
A selenocisteína é um aminoácido incomum. Sua estrutura química é semelhante à cisteína, com um átomo de selênio no lugar do enxofre. Ela faz parte de certas proteínas, especialmente enzimas que usam o selênio como grupo prostético em reações de redução. A selenocisteína está presente em várias enzimas, como por exemplo as enzimas glutationa peroxidase, tetraiodotironina 5' desiodase, tiorredoxina redutase, formiato desidrogenase , glicina redutase e algumas hidrogenases.
Nomenclatura[editar | editar código-fonte]
O comitê conjunto das nomenclaturas da IUPAC / IUBMB tem recomendado oficialmente o símbolo de três letras Sec e o símbolo de uma letra U para selenocisteína [2].
Estrutura[editar | editar código-fonte]
A selenocisteína tem uma estrutura semelhante à da cisteína, mas com um átomo de selênio no lugar do átomo de enxofre usual, formando um grupo selenol. Proteínas que contêm um ou mais resíduos de selenocisteína são chamados selenoproteínas.
Biologia[editar | editar código-fonte]
A selenocisteína tem um pKa tanto menor e um maior potencial de redução que a cisteína. Estas propriedades a tornam muito adequada em proteínas que estão envolvidas na atividade anti-oxidante. Ao contrário de outros aminoácidos presentes nas proteínas biológicas, a selenocisteína não é codificada diretamente no código genético. Em vez disso, ela é codificada de uma maneira especial por um códon UGA, que normalmente é um códon de parada. Quando as células são cultivadas na ausência de selênio, a tradução de selenoproteínas termina no códon UGA, resultando em uma enzima truncada, não-funcional. O códon UGA é feito para codificar selenocisteína pela presença de um elemento SECIS (Sequência de Inclusão de selenocisteína) no mRNA. O elemento é definido pelas sequências características de nucleotídeos no SECIS e estrutura secundária de emparelhamento de base padrões. Em bactérias, o elemento SECIS está localizado logo após o códon UGA dentro do quadro de leitura para a selenoproteína. Em archaea e eucariotas, o elemento SECIS está na <<região não traduzida>> (3' os 3 UTR) do mRNA, e pode direcionar vários códons UGA para codificar os resíduos de selenocisteína. Ao contrário dos outros aminoácidos, a selenocisteína livre não existe na célula. Sua alta reatividade incorreria danos às células. Em vez disso, as células armazenam selênio na forma de seleneto menos reativo (H2Se). A síntese de selenocisteína ocorre em um tRNA especializado, que também funciona para incorporá-lo em polipeptídeos nascentes. A estrutura primária e secundária do tRNA selenocisteína, tRNA (Sec), difere dos tRNAs padrão em vários aspectos, principalmente em ter um 8-base (bactérias) ou 10-base (eucariontes) tronco para receptor, uma região muito variável no braço, e substituições em várias posições de bases bem conservadas . Os tRNAs selenocisteína são inicialmente ligados a serina por seril-tRNA ligase, mas a resultante Ser-tRNA (Sec) não é usada para a tradução, porque não é reconhecida pelo fator de conversão normal (EF-Tu em bactérias, eEF1A em eucariotos). Em vez disso, o resíduo tRNA- seril é convertido para um resíduo de selenocisteína pela enzima selenocisteína sintase contendo o cofator fosfato de piridoxal. Finalmente, o Sec-tRNA(Sec) resultante é especificamente ligado a um fator de elongação alternativa translacional (Selb ou mSelB (aka eEFSec)), que o entrega em uma forma orientada para os ribossomos traduzindo mRNAs para selenoproteínas. A especificidade deste mecanismo de entrega é provocada pela presença de um domínio de proteína extra (em Selb bacteriana) ou uma subunidade extra (SBP2 para mSelB eucarióticas / eEFSec) que se ligam a estruturas secundárias correspondentes no RNA formado pelos elementos SECIS em mRNAs que codificam selenoproteínas.
