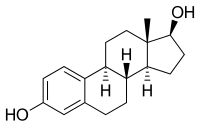
Estradiol
| |

| |
| Nome IUPAC (sistemática) | |
| (8R,9S,13S,14S,17S)-13-methyl- 6,7,8,9,11,12,14,15,16,17-decahydro cyclopenta[a]phenanthrene-3,17-diol | |
| Identificadores | |
| CAS | 50-28-2 |
| ATC | G03CA03 |
| PubChem | 5757 |
| ChemSpider | |
| Informação química | |
| Fórmula molecular | C18H24O2 |
| Massa molar | 272.39 |
| SMILES | Oc1ccc2c(CC[C@@H]3[C@@H]2CC[C@]2(C)[C@@H](O)CC[C@@H]32)c1 |
| Farmacocinética | |
| Biodisponibilidade | 97-99% |
| Metabolismo | Fígado |
| Meia-vida | ~ 13 horas |
| Excreção | Urina |
| Considerações terapêuticas | |
| Administração | Oral, transdérmico |
| DL50 | ? |
Estradiol ou 17β-estradiol é um hormônio sexual e esteroide, o principal hormônio sexual feminino. É importante na regulação do ciclo estral e do ciclo menstrual. O estradiol é essencial para o desenvolvimento e manutenção dos tecidos reprodutivos femininos[1] mas também tem efeitos importantes em muitos outros tecidos, incluindo o ósseo. Enquanto os níveis de estrogênio nos homens são mais baixos em comparação com as mulheres, estrógenos têm funções essenciais em homens também. O estradiol é encontrado na maioria dos vertebrados, bem como muitos crustáceos, insetos, peixes e outras espécies animais.[2][3] O estradiol também apresenta importantes efeitos comportamentais.[4]
Efeitos[editar | editar código-fonte]
Estradiol e Gravidez[editar | editar código-fonte]
No momento que a mulher engravida, seu corpo passa por inúmeras alterações hormonais.
Hormônios que antes não eram produzidos passam a ser pelo organismo com o objetivo de oferecer as condições favoráveis para desenvolvimento do bebê no útero.
Algumas outras substâncias que já eram produzidas antes da gestação, passam a existir em maior quantidade no corpo. Dentre os hormônios que são importantes para conseguir engravidar, o estradiol é um dos principais.[5]
Reprodução masculina[editar | editar código-fonte]
O efeito do estradiol (e estrógenos) sobre a reprodução masculina é complexo. O estradiol é produzido por ação da aromatase, principalmente nas células de Leydig dos testículos dos mamíferos, mas também por algumas células germinativas e células de Sertoli de mamíferos imaturos.[4] Sua função (in vitro) mostrou ser impedir a apoptose das células do sêmen.[6]
Vários estudos têm observado que a contagem de espermatozoides têm diminuído em muitas partes do mundo e a exposição ao estrogênio no meio ambiente tem sido postulada como sendo a causa.[7] A supressão da produção de estradiol em uma subpopulação de homens subférteis mostrou melhorar a análise do sêmen.[8]
Homens com condições genéticas de cromossomos sexuais, como a síndrome de Klinefelter, têm um maior nível de estradiol.[9]
Ossos[editar | editar código-fonte]
O estradiol tem um efeito profundo sobre os ossos. Indivíduos sem ele (ou outros estrogênios) se tornam altos e eunucoides, já que o fechamento epifisário está atrasado ou inexiste. A estrutura óssea é também afetada, o que resulta em osteoporose e osteopenia precoce.[10] Além disso, mulheres que passaram da menopausa têm uma perda acelerada da massa óssea devido a relativa deficiência de estrogénio.[11]
O papel do estradiol no cancro[editar | editar código-fonte]
Em termos gerais a relação entre o estradiol e o desenvolvimento de cancro ainda não é um dado adquirido, pois embora muitos estudos venham a ser desenvolvidos ao longo dos anos as conclusões a que chegam não são de forma alguma uniformes, com exceção de alguns tipos de cancro.
Existem estudos que mostram que poderá ter efeitos benéficos[12][13][14] e outros deduzem exatamente o contrário.[15][16][17][18]
Uma explicação para este facto poderá ser os efeitos muito variados que o estradiol poderá provocar, que em uns casos pode ser benéfico e noutros nem tanto. Num estudo acerca do efeito do estradiol em carcinomas da pele foi concluído que que o efeito era positivo devido à prevenção da proliferação e migração obtida nas linhas celulares GLL19 e A375, que são linhas celulares de melanomas, e também foi observado uma redução do nível de MDM2, um conhecido regulador negativo da p53 (proteína supressora de tumores).[19]
O estradiol é um fator importante a ter em conta em cancro do endométrio e ovário, onde 5% das mulheres com menos de 40 anos que desenvolvem este tipo de cancro apresentam tumores dependentes de estrogénio bem diferenciados.[20]
Já quanto aos cancros testiculares e da próstata, mais uma vez os estudos não são conclusivos, com alguns a mostrarem uma associação entre os dois[21][22] e outros sem associação.[23][24]
Embora ainda não completamente comprovado a exposição a estrogénios parece aumentar a predisposição para o desenvolvimento de cancro da próstata. Os elevados níveis de estrogénios em casos de cancro da próstata, alterações nos recetores de estrogénio nas fases mais avançadas deste tipo de neoplasias e estudos que mostram a indução de cancro da próstata em células humanas tratadas com estrogénios e testosterona, são evidências que apoiam a possibilidade dos estrogénios estarem envolvidos no desenvolvimento de cancro.[25]
No que concerne ao cancro da mama as evidências são mais consistentes e apontam o estradiol como um carcinogéneo, no entanto os mecanismos que explicam isso são complexos.
Os metabolitos genotóxicos do estradiol e a sinalização genómica e não genómica mediada pelos recetores de estrogénio afetam a proliferação celular e a apoptose. A extensão pela qual estes dois processos afetam o processo carcinogénico, bem como de que forma os polimorfismos genéticos e fatores ambientais afetam ambos processos ainda necessita de uma maior investigação.[26]
Paradoxalmente o estradiol pode ser usado para tratamento em certos casos, como por exemplo nos casos de cancro da mama metastáticos positivos para o recetor de estrogénio, onde devido a invariavelmente surgirem resistências ao tratamento de bloqueio da ação dos recetores de estrogénio (seja por redução do substrato ou inibição direta) o estradiol é usado em elevadas doses para induzir apoptose pela via extrínseca por aumento do ligando Fas e seu recetor.[27]
O metabolismo oxidativo do estradiol poderá ter uma influência muito marcada no desenvolvimento de cancros devido à possível formação de quinonas que irão interagir com o DNA, formando aductos que por sua vez podem levar à depurinação do DNA.[28] A atividade da enzima catecol-O-metiltransferase (COMT) será muito importante na prevenção destes danos, uma vez que metila os catecóis que são formados através da reação de metabolismo de fase I do estradiol, formando metoxi-catecóis que não são nocivos para o DNA. Sendo assim, indivíduos que expressem variantes da COMT com baixas atividades terão um risco superior de desenvolvimento de cancro, cujas probabilidades podem variar entre 1,7 e 3,0 vezes.[29]
Um fator potencialmente fulcral para explicar o papel do estradiol no desenvolvimento de cancro da mama poderá ser a elevada presença de catecolaminas como epinefrina ou dopamina que também são metiladas pela COMT, podendo levar um excesso de substratos para esta enzima. Devido a este aumento de substratos, pode ocorrer em maior quantidade a formação de quinonas, sendo assim nocivo para o DNA.[30] A relação do estradiol no cancro da mama já está devidamente estabelecida, fruto de todas as evidências já referidas. O mesmo não acontece com os outros tipos de cancro, uma vez que há informações discordantes e menos estudos sobre os mesmos.
Referências
- ↑ Ryan KJ (agosto de 1982). «Biochemistry of aromatase: significance to female reproductive physiology». Cancer Res. 42 (8 Suppl). pp. 3342s–3344s. PMID 7083198
- ↑ Mechoulam R, Brueggemeier RW, Denlinger DL. «Estrogens in insects» (PDF). Cellular and Molecular Life Sciences. 40 (9). pp. 942–944. doi:10.1007/BF01946450
- ↑ David R. Idler (1972). Steroids In Nonmammalian Vertebrates. Elsevier. p. 393. ISBN 978-0-323-14098-0.
- ↑ a b Carreau S, Lambard S, Delalande C, Denis-Galeraud I, Bilinska B, Bourguiba S (2003). «Aromatase expression and role of estrogens in male gonad : a review». Reproductive Biology and Endocrinology. 1. 35 páginas. PMC 155680
 . PMID 12747806. doi:10.1186/1477-7827-1-35
. PMID 12747806. doi:10.1186/1477-7827-1-35
- ↑ Estradiol - Universo do Bebê
- ↑ Pentikäinen V, Erkkilä K, Suomalainen L, Parvinen M, Dunkel L (2000). «Estradiol acts as a germ cell survival factor in the human testis in vitro». The Journal of Clinical Endocrinology and Metabolism. 85 (5). pp. 2057–67. PMID 10843196. doi:10.1210/jc.85.5.2057
- ↑ Sharpe RM, Skakkebaek NE (1993). «Are oestrogens involved in falling sperm counts and disorders of the male reproductive tract?». Lancet. 341 (8857). pp. 1392–5. PMID 8098802. doi:10.1016/0140-6736(93)90953-E
- ↑ Raman JD, Schlegel PN (2002). «Aromatase inhibitors for male infertility». The Journal of Urology. 167 (2 Pt 1). pp. 624–9. PMID 11792932. doi:10.1016/S0022-5347(01)69099-2
- ↑ Visootsak J, Graham JM (2006). «Klinefelter syndrome and other sex chromosomal anueploidies». Orphanet Journal of Rare Diseases. 1 (42). p. 42. PMC 1634840
 . PMID 17062147. doi:10.1186/1750-1172-1-42. Consultado em 18 de outubro de 2014
. PMID 17062147. doi:10.1186/1750-1172-1-42. Consultado em 18 de outubro de 2014
- ↑ Carani C, Qin K, Simoni M, Faustini-Fustini M, Serpente S, Boyd J, Korach KS, Simpson ER (1997). «Effect of testosterone and estradiol in a man with aromatase deficiency». The New England Journal of Medicine. 337 (2). pp. 91–5. PMID 9211678. doi:10.1056/NEJM199707103370204
- ↑ Albright, Fuller; Smith Patricia H., Richardson Anna M. (31 de maio de 1941). «Postmenopausal Osteoporosis: Its Clinical Features». JAMA. 116 (22). pp. 2465–2474. doi:10.1001/jama.1941.02820220007002
- ↑ Huang, Fung-Yu; Wong, Danny Ka-Ho; Seto, Wai-Kay; Lai, Ching-Lung; Yuen, Man-Fung (30 de setembro de 2015). «Estradiol induces apoptosis via activation of miRNA-23a and p53: implication for gender difference in liver cancer development». Oncotarget. 6 (33). ISSN 1949-2553. doi:10.18632/oncotarget.5472
- ↑ Roy, Sayantani; Reddy, Bathula Surendar; Sudhakar, Godeshala; Kumar, Jerald Mahesh; Banerjee, Rajkumar (18 de fevereiro de 2011). «17β-Estradiol-Linked Nitro-l-arginine as Simultaneous Inducer of Apoptosis in Melanoma and Tumor-Angiogenic Vascular Endothelial Cells». Molecular Pharmaceutics. 8 (2): 350–359. ISSN 1543-8384. doi:10.1021/mp2000346
- ↑ Sudhakar, Godeshala; Bathula, Surendar Reddy; Banerjee, Rajkumar (outubro de 2014). «Development of new estradiol-cationic lipid hybrids: Ten-carbon twin chain cationic lipid is a more suitable partner for estradiol to elicit better anticancer activity». European Journal of Medicinal Chemistry. 86: 653–663. ISSN 0223-5234. doi:10.1016/j.ejmech.2014.09.030
- ↑ Bandyopadhyay, Debasish; Rivera, Gildardo; Sanchez, Jorge L.; Rivera, Jesse; Granados, Jose C.; Guerrero, Adrian M.; Chang, Fang-Mei; Dearth, Robert K.; Short, John D. (julho de 2014). «Bismuth nitrate-induced novel nitration of estradiol: An entry to new anticancer agents». European Journal of Medicinal Chemistry. 82: 574–583. ISSN 0223-5234. doi:10.1016/j.ejmech.2014.06.010
- ↑ Hackenberg, Reinhard; Turgetto, Inga; Filmer, Angelika; Schulz, Klaus-Dieter (novembro de 1993). «Estrogen and androgen receptor mediated stimulation and inhibition of proliferation by androst-5-ene-3β,17β-diol in human mammary cancer cells». The Journal of Steroid Biochemistry and Molecular Biology. 46 (5): 597–603. ISSN 0960-0760. doi:10.1016/0960-0760(93)90187-2
- ↑ Hornsby, Peter (1 de setembro de 1999). «Human Adrenal Androgens: Regulation of Biosynthesis and Role in Estrogen-Responsive Breast Cancer in a Mouse Model». Fort Belvoir, VA
- ↑ Pequeux, C.; Raymond-Letron, I.; Blacher, S.; Boudou, F.; Adlanmerini, M.; Fouque, M.-J.; Rochaix, P.; Noel, A.; Foidart, J.-M. (20 de abril de 2012). «Stromal Estrogen Receptor- Promotes Tumor Growth by Normalizing an Increased Angiogenesis». Cancer Research. 72 (12): 3010–3019. ISSN 0008-5472. doi:10.1158/0008-5472.can-11-3768
- ↑ Li, Li; Feng, Jianguo; Chen, Ying; Li, Shun; Ou, Mengting; Sun, Weichao; Tang, Liling (27 de dezembro de 2016). «Estradiol shows anti-skin cancer activities through decreasing MDM2 expression». Oncotarget. 8 (5). ISSN 1949-2553. doi:10.18632/oncotarget.14275
- ↑ Kumar, Anita; Banerjee, Antara; Singh, Dipty; Thakur, Gargi; Kasarpalkar, Nandini; Gavali, Shubhangi; Gadkar, Sushama; Madan, Taruna; Mahale, Smita (22 de março de 2018). «Estradiol: A Steroid with Multiple Facets». Hormone and Metabolic Research. 50 (05): 359–374. ISSN 0018-5043. doi:10.1055/s-0044-100920
- ↑ Barba, Maddalena; Yang, Li; Schünemann, Holger J; Sperati, Francesca; Grioni, Sara; Stranges, Saverio; Westerlind, Kim C; Blandino, Giovanni; Gallucci, Michele (2009). «Urinary estrogen metabolites and prostate cancer: a case-control study and meta-analysis». Journal of Experimental & Clinical Cancer Research. 28 (1). 135 páginas. ISSN 1756-9966. doi:10.1186/1756-9966-28-135
- ↑ King, I. B. (1 de abril de 2005). «Serum Trans-Fatty Acids Are Associated with Risk of Prostate Cancer in -Carotene and Retinol Efficacy Trial». Cancer Epidemiology Biomarkers & Prevention. 14 (4): 988–992. ISSN 1055-9965. doi:10.1158/1055-9965.epi-04-0517
- ↑ Levin, Ellis R. (14 de janeiro de 2015). «Extranuclear Steroid Receptors Are Essential for Steroid Hormone Actions». Annual Review of Medicine. 66 (1): 271–280. ISSN 0066-4219. doi:10.1146/annurev-med-050913-021703
- ↑ Platz, E. A. (1 de maio de 2005). «Sex Steroid Hormones and the Androgen Receptor Gene CAG Repeat and Subsequent Risk of Prostate Cancer in the Prostate-Specific Antigen Era». Cancer Epidemiology Biomarkers & Prevention. 14 (5): 1262–1269. ISSN 1055-9965. doi:10.1158/1055-9965.epi-04-0371
- ↑ Nelles, Jason L; Hu, Wen-Yang; Prins, Gail S (maio de 2011). «Estrogen action and prostate cancer». Expert Review of Endocrinology & Metabolism. 6 (3): 437–451. ISSN 1744-6651. doi:10.1586/eem.11.20
- ↑ Yager, James D.; Davidson, Nancy E. (19 de janeiro de 2006). «Estrogen Carcinogenesis in Breast Cancer». New England Journal of Medicine. 354 (3): 270–282. ISSN 0028-4793. doi:10.1056/nejmra050776
- ↑ Kota, Karthik; Brufsky, Adam; Oesterreich, Steffi; Lee, Adrian (6 de julho de 2017). «Estradiol as a Targeted, Late-Line Therapy in Metastatic Breast Cancer with Estrogen Receptor Amplification». Cureus. ISSN 2168-8184. doi:10.7759/cureus.1434
- ↑ Weinshilboum, Richard M. (29 de junho de 2006). «Pharmacogenomics: Catechol O-Methyltransferase to Thiopurine S-Methyltransferase». Cellular and Molecular Neurobiology. 26 (4-6): 537–559. ISSN 0272-4340. doi:10.1007/s10571-006-9095-z
- ↑ Goulding, R. (1 de dezembro de 1987). «Casarett & Doull's Toxicology: the Basic Science of Poisons». Postgraduate Medical Journal. 63 (746): 1112–1112. ISSN 0032-5473. doi:10.1136/pgmj.63.746.1112-b
- ↑ Cavalieri, Ercole (1 de maio de 2017). «Etiology and prevention of prevalent types of cancer». Journal of Rare Diseases Research & Treatment. 2 (3): 22–29. PMC 6404759
 . PMID 30854528. doi:10.29245/2572-9411/2017/3.1093
. PMID 30854528. doi:10.29245/2572-9411/2017/3.1093
