Éter difenílico
| Éter difenílico Alerta sobre risco à saúde | |
|---|---|
| |

| |
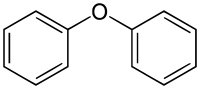
| Nome IUPAC | Diphenyl ether |
| Outros nomes | Diphenyl oxide; 1,1'-Oxybisbenzene; Phenoxybenzene |
| Identificadores | |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| ChEBI | |
| SMILES |
|
| InChI | 1/C12H10O/c1-3-7-11(8-4-1)13-12-9-5-2-6-10-12/h1-10H
|
| Propriedades | |
| Fórmula química | C12H10O |
| Massa molar | 170.2 g mol-1 |
| Aparência | Colorless solid or liquid with a geranium-like odor |
| Densidade | 1,07 g·cm-3[1] |
| Ponto de fusão |
26,9 °C[1] |
| Ponto de ebulição |
258 °C[1] |
| Solubilidade em água | insolúvel (21 mg·l-1 a 20 °C)[1] |
| Pressão de vapor | 8 Pa (20 °C)[1] |
| Índice de refracção (nD) | 1,579 a 20 °C[2] |
| Riscos associados | |
| MSDS | Aldrich MSDS |
| NFPA 704 | |
| Frases R | R36/37, R51/53 |
| Frases S | S60, S61 |
| Ponto de fulgor | 115 °C (388.15 K) |
| LD50 | 2450 mg·kg-1 (rato, oral)[2] |
| Compostos relacionados | |
| Éteres relacionados | Anisol (metoxibenzeno) 4,4'-Oxidianilina (+2 aminas, posições 4 e 4') Tironina (aminoácido, com um difeniléter no meio) |
| Compostos relacionados | Difenilamina Sulfeto de difenila |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Éter difenílico ou difenil éter é um composto orgânico de fórmula O(C6H5)2. essa molécula esta sujeita aos mesmos tipos de reações que outros anéis fenílicos, tais como: halogenação, nitração, sulfonação, hidroxilação e reação de Friedel-Crafts.[3]
Síntese[editar | editar código-fonte]
Éter difenílico e muitas de suas propriedades foram descobertas pela primeira vez no inicio de 1901.[4] É sintetizado pela reação entre fenol e bromobenzeno na presença de uma base e cobre como catalisador. Envolvendo reações similares, éter difenílico é produzido de forma colateral na hidrólise de alta pressão do clorobenzeno para produção de fenol.[5]
Usos[editar | editar código-fonte]
O éter difenílico é usado principalmente na produção de uma mistura eutética juntamente com o bifenil para troca de calor. Essa mistura é apropriada para tal aplicação pois sua fase líquida possui uma ampla gama de temperaturas. O éter difenílico é o material de partida para a produção de fenoxatiina via reação de Ferrario. A fenoxatiina é usada na produção de poliamidas e poliimidas.
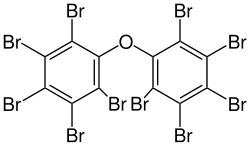
Por causa de seu odor parecido com gerânios, seu baixo preço e por sua estabilidade, o éter difenílico é amplamente usado em perfumes e sabões. Muitos éteres difenílicos polibrominados são úteis como retardante de chamas. Os éteres penta, octa e deca brominados são os três mais comuns, porém somente o decasubstituido ainda é amplamente usado desde que foram banidos na União Europeia, em 2003.[6] Também conhecido pelo nome de óxido decabromodifenila.[7] O decabromo difenil éter é produzido em massa nos Estados Unidos (450.000 kg anualmente), sendo usado, como retardante de chamas, na fabricação de plásticos reforçados e tintas. Seu nome comercial é Saytex 102.
Referências
- ↑ a b c d e Registo de CAS RN 101-84-8 na Base de Dados de Substâncias GESTIS do IFA
- ↑ a b Catálogo da Sigma-Aldrich, Éter difenílico, consultado em 28 de março de 2011
- ↑ Fiege, H.; Voges, H.-M.; Hamamoto, T; Umemura, S.; Iwata, T.; Miki, H.; Fujita, Y.; Buysch, H.-J.; Garbe, D.; Paulus, W. (2000). «Phenol Derivatives». Weinheim: Wiley-VCH. Ullmann's Encyclopedia of Industrial Chemistry. ISBN 3527306730. doi:10.1002/14356007.a19_313
- ↑ Cook, A. N. (1901). «Derivatives of Phenylether». Journal of the American Chemical Society. 23 (11): 806-813. doi:10.1021/ja02037a005
- ↑ Fahlbusch, K.-G.; Hammerschmidt, F.-J.; Panten, J.; Pickenhagen, W.; Schatkowski, D.; Bauer, K.; Garbe, D.; Surburg, H. (2003). «Flavor and Fragrances». Weinheim: Wiley-VCH. Ullmann's Encyclopedia of Industrial Chemistry. ISBN 3527306730. doi:10.1002/14356007.a11_141
- ↑ DIRECTIVE 2003/11/EC of the European Parliament and of the Council
- ↑ Sutker, B. J. (2005). «Flame Retardants». Weinheim: Wiley-VCH. Ullmann's Encyclopedia of Industrial Chemistry. ISBN 3527306730. doi:10.1002/14356007.a11_123
- Este artigo foi inicialmente traduzido, total ou parcialmente, do artigo da Wikipédia em inglês cujo título é «Diphenyl ether», especificamente desta versão.

