Fulerenos endoédricos
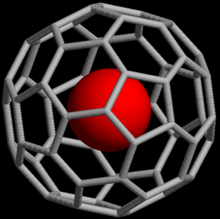

Fulerenos endoédricos, também chamados de endofulerenos, são fulerenos que contém átomos, íons ou clusters adicionais enclausurados em suas esferas interiores. O primeiro complexo de C60 com lantânio foi sintetizado em 1985 e foi denominado como La@C60.[2] O símbolo @ (arroba) no nome se refere à noção de que há uma pequena molécula aprisionada dentro da estrutura. Existem dois tipos de complexos endoédricos: metalofulerenos endoédricos e fulerenos dopados não-metálicos.
Notação[editar | editar código-fonte]
Em uma notação de fórmula química tradicional, um buckminsterfulereno (C60) com um átomo (M) era simplesmente representada como MC60 independentemente se M estava dentro ou fora do fulereno. Para permitir discussões mais detalhadas com uma perda mínima de informação, uma notação mais explícita foi proposta em 1991,[2] na qual os átomos listados à esquerda do símbolo @ estão situados dentro da cadeia composta pelos átomos listados à direita. O exemplo acima seria então denominado M@C60 se M estiver dentro da cadeia carbônica. Um exemplo mais complexo é K2(K@C59B), o qual denota "um fulereno de cadeia de 60 átomos com um átomo de boro substituindo um carbono na cadeia geodésica, um único potássio aprisionado dentro da estrutura e dois átomos de potássio aderidos na face exterior."[2]
A escolha do símbolo foi explicada pelos autores como sendo concisa, facilmente impressa e transmitida eletronicamente (o símbolo de arroba está incluído no ASCII, no qual os esquemas mais modernos de codificação de caracteres são baseados) e com aspectos visuais que lembram a estrutura de um fulereno endoédrico.
Metalofulerenos endoédricos[editar | editar código-fonte]
A dopagem de fulerenos com metais eletropositivos acontece em um reator de arco ou por evaporação a laser. Os metais podem ser de transição, como escândio e ítrio, assim como lantanídeos, como lantânio e cério. Também são possíveis complexos endoédricos com elementos dos metais alcalino-terrosos, como bário e estrôncio, metais alcalinos, como potássio, e metais tetravalentes, como urânio, zircônio e háfnio. A síntese no reator de arco é, portanto, não específica. Assim como os fulerenos não preenchidos, os metalofulerenos endoédricos podem ter diferentes tamanhos de gaiola, como La@C60 ou La@C82, e diferentes gaiolas isoméricas. Apesar da presença dominante de gaiolas monometálicas, numerosos complexos fulerenos di e trimetálicos como Sc3C2@C80 também foram isolados.
Em 1999 uma descoberta chamou grande atenção. Com a síntese de Sc3N@C80 por Harry Dorn e colaboradores, a inclusão de um fragmento molecular em uma gaiola fulerênica foi bem sucedida pela primeira vez. O composto pode ser preparado por vaporização em arco sob temperaturas acima de 1100ºC em bastões de grafite empacotados com óxido de escândio(III), nitreto de ferro e grafite em pó em um gerador K-H em atmosfera de nitrogênio a 300 Torr.[3]
Metalofulerenos endoédricos são caracterizados pelo fato de que os elétrons são transferidos do átomo metálico para a gaiola de fulereno e que aquele ocupa uma posição fora do centro da estrutura. A extensão da transferência de carga não é sempre simples de se determinar. Na maioria dos casos é por volta de duas a três unidades de carga. No caso do La2@C80 contudo podem ser por volta de seis unidades, assim como em Sc3N@C80, melhor descrito como [Sc3N]6+@[C80]6-. Essas cadeias fulerênicas aniônicas são moléculas muito estáveis e não tem reatividade associada com fulerenos vazios ordinários. Elas são estáveis no ar até altas temperaturas (de 600 a 800ºC).
A falta de reatividade em reações de Diels-Alder é utilizada como método para purificar compostos de [C80]6- de uma mistura complexa de fulerenos parcialmente ou não preenchidos e de diferentes tamanhos de gaiola.[3] Neste método uma resina de Merrifield é modificada como uma resina de ciclopentadienila e usado como fase sólida em uma cromatografia em coluna; a fase líquida consiste na mistura complexa de fulerenos. Somente fulerenos estáveis como [Sc3N]6+@[C80]6- passam através da coluna sem sofrer reações.
Em Ce2@C80 os dois átomos metálicos exibem uma interação não-ligante.[4] Desde que todos os aneis de seis membros de C80-Ih sejam iguais[4] os dois átomos de cério encapsulados exibem um movimento tridimensional aleatório.[5] Isto é evidenciado pela presença de apenas dois sinais no espectro de RMN de 13C. É possível forçar a imobilização dos átomos metálicos no equador como mostrado na cristalografia de raios X quando o fulereno é funcionalizado externamente por um grupo silil doador de elétrons em uma reaçao de Ce2@C80 com 1,1,2,2-tetrakis(2,4,6-trimetilfenil)-1,2-dissilirano.
Fulerenos dopados não-metálicos[editar | editar código-fonte]
Em 1993 Martin Saunders produziu complexos endoédricos de He@C60 e Ne@C60 por pressurização de C60 em uma atmosfera de gás nobre de cerca de 3 bar.[6] Sob tais condições, cerca de uma a cada 650000 cadeias de C60 foram dopadas com um átomo de hélio. A formação de complexos endoédricos com hélio, neônio, argônio, criptônio e xenônio, assim como numerosos adutos de He@C60, foi demonstrada sob pressão de 3 kbar e incorporação de gases nobres acima de 0,1%.[7]
Enquanto gases nobres são quimicamente muito inertes e comumente existem como átomos individuais, nitrogênio e fósforo não se comportam da mesma maneira, de modo que a formação de complexos endoédricos tais como N@C60 e P@C60 é ainda mais surpreendente. O átomo de nitrogênio está em seu estado eletrônico inicial (4S3/2) e é por tal razão altamente reativo. Ainda assim, N@C60 é estável suficientemente para que a derivatização exoédrica do mono para o hexa aduto de éster etílico de ácido malônico ocorra. Nestes compostos não ocorre transferência de carga do átomo de nitrogênio central para os carbonos da gaiola. Por consequência, acoplamentos de 13C, que são facilmente observados em metalofulerenos endoédricos, só podem ser detectados no caso de N@C60 em um espectro de alta resolução como ombros de uma linha central.
O átomo central nesses complexos endoédrivos está localizado no centro da gaiola. Enquanto outros traps atômicos requerem equipamento complexo, como arrefecimento a laser ou traps magnéticos, fulerenos endoédricos representam um trap atômico que é estável em temperatura ambiente e por um tempo longo arbitrário. Traps atômicos ou iônicos são de grande interesse desde que as partículas estejam presentes livres de interação (significante) com seu ambiente, permitindo que fenômenos mecânico-quânticos únicos sejam explorados. Por exemplo, a compressão da função de onda atômica como consequência do empacotamento na gaiola poderia ser observada em espectroscopia ENDOR. O átomo de nitrogênio pode ser usado como prova, a fim de se detectar as menores mudanças da estrutura eletrônica de seu ambiente.
Ao contrário dos compostos metaloendroédricos, estes complexos não podem ser produzidos em arco. Os átomos são implantados no material de partida fulerênico usando descarga de gás (complexos de nitrogênio e fósforo) ou por implantação iônica direta. Alternativamente, fulerenos de hidrogênio endoédricos podem ser produzidos por abertura e fechamento de um fulereno por métodos de química orgânica. Um exemplo recente de fulerenos endoédricos inclui moléculas individuais de água encapsuladas por C60.[8]
De acordo com os cálculos DFT de estado-da-arte, endofulerenos de gases nobres demonstram polarizabilidade incomum. Deste modo, valores calculados para a polarizabilidade média de Ng@C60 não se igualam à soma de polarizabilidades da gaiola de fulereno com a do átomo aprisionado, isto é, ocorre uma exaltação da polarizabilidade.[9][10] O sinal de exaltação da variação de polarizabilidade Δα depende do número de átomos na molécula fulerênica: para fulerenos pequenos (n < 30), é positivo; para os maiores (n > 30), é negativo (depressão de polarizabilidade). A fórmula a seguir, descrevendo a dependência de Δα em n, foi proposta: Δα = αNg(2e−0.06(n – 20)-1). Ela descreve as polarizabilidades médias calculadas por DFT de endofulerenos Ng@C60 com acurácia suficiente. Os dados calculados permitem usar o fulereno C60 como gaiola de Faraday,[11] o que isola o átomo encapsulado do campo elétrico externo. As relações mencionadas devem ser típicas para mais estruturas endoédricas complicadas (como C60@C240[12] e "cebolas" contendo fulerenos gigantes[13]).
Endofulerenos moleculares[editar | editar código-fonte]
Fulerenos fechados encapsulando pequenas moléculas tem sido sintetizados por longas sequências de reações orgânicas. Realizações notáveis são a síntese do endofulereno de di-hidrogênio H2@C60, o endofulereno de água H2O@C60 e o endofulereno de fluoreto de hidrogênio HF@C60 pelos grupos de Komatsu,[14] Murata[15] e Whitby[16] As moléculas encapsuladas apresentam propriedades físicas atípicas que tem sido estudadas por uma variedade de métodos físicos.[17] Conforme mostrado teoricamente,[18] a compressão de endofulerenos moleculares (como em H2@C60) podem conduzir à dissociação das moléculas encapsuladas e a reação de seus fragmentos com os interiores da cadeia de fulereno. Tal reação deve resultar em adutos fulerênicos endoédricos, os quais são desconhecidos atualmente.
Uma hipótese interessante citada no livro Duvoisin e col. [19] é a hipótese da produção de superátomos, através do controle das armadilhas de elétrons, estilo Garrafa de Leyden. Ou seja, se um reator de plasma produtor de fulerenos e endofulerenos estiver adaptado com uma espécie de Garrafa de Leyden, assim proporcionando uma verdadeira armadilha de elétrons. Desta forma, esta suposição poderá resultar em acúmulos maiores de átomos para serem encapsulados pelo fulereno, com isso resultando em uma compactação nuclear, cuja se interpretaria em um método de produzir superátomos de forma controlada.
Ver também[editar | editar código-fonte]
Referências
- ↑ Gimenez-Lopez, Maria del Carmen; Chuvilin, Andrey; Kaiser, Ute; Khlobystov, Andrei N. (2010). «Functionalised endohedral fullerenes in single-walled carbon nanotubes». Chem. Commun. 47 (7): 2116–2118. doi:10.1039/C0CC02929G
- ↑ a b c Chai, Yan; Guo, Ting; Jin, Changming; Haufler, Robert E.; Chibante, L. P. Felipe; Fure, Jan; Wang, Lihong; Alford, J. Michael; Smalley, Richard E. (1991). «Fullerenes wlth Metals Inside». Journal of Physical Chemistry. 95 (20): 7564–7568. doi:10.1021/j100173a002
- ↑ a b Ge, Z; Duchamp, Jc; Cai, T; Gibson, Hw; Dorn, Hc (2005). «Purification of endohedral trimetallic nitride fullerenes in a single, facile step». Journal of the American Chemical Society. 127 (46): 16292–8. PMID 16287323. doi:10.1021/ja055089t
- ↑ a b K.Muthukumar; J.A.Larsson (2008). «Explanation of the different preferential binding sites for Ce and La in M2@C80 (M = Ce, La)». Journal of Materials Chemistry. 18 (28): 3347–51. doi:10.1039/b804168g
- ↑ Yamada, M; Nakahodo, T; Wakahara, T; Tsuchiya, T; Maeda, Y; Akasaka, T; Kako, M; Yoza, K; Horn, E; Mizorogi, N; Kobayashi, K; Nagase, S (2005). «Positional control of encapsulated atoms inside a fullerene cage by exohedral addition». Journal of the American Chemical Society. 127 (42): 14570–1. PMID 16231899. doi:10.1021/ja054346r
- ↑ Saunders, M.; Jiménez-Vázquez, H. A.; Cross, R. J.; Poreda, R. J. (1993). «Stable compounds of helium and neon. He@C60 and Ne@C60». Science. 259 (5100): 1428–1430. Bibcode:1993Sci...259.1428S. PMID 17801275. doi:10.1126/science.259.5100.1428
- ↑ Saunders, Martin; Jimenez-Vazquez, Hugo A.; Cross, R. James; Mroczkowski, Stanley; Gross, Michael L.; Giblin, Daryl E.; Poreda, Robert J. (1994). «Incorporation of helium, neon, argon, krypton, and xenon into fullerenes using high pressure». J. Am. Chem. Soc. 116 (5): 2193–2194. doi:10.1021/ja00084a089
- ↑ Kurotobi, Kei; Murata, Yasujiro (2012). «A Single Molecule of Water Encapsulated in Fullerene C60». Science. 333 (6042): 613–6. Bibcode:2011Sci...333..613K. PMID 21798946. doi:10.1126/science.1206376
- ↑ Sabirov, D.; Bulgakov, R. (2010). «Polarizability exaltation of endofullerenes X@Cn (n = 20, 24, 28, 36, 50, and 60; X is a noble gas atom)». JETP Lett. 92 (10): 662–665. Bibcode:2010JETPL..92..662S. doi:10.1134/S0021364010220054
- ↑ Yan, Hong; Yu, Shengping; Wang, Xin; He, Yang; Huang, Wen; Yang, Mingli (2008). «Dipole polarizabilities of noble gas endohedral fullerenes». Chemical Physics Letters. 456 (4–6): 223–226. Bibcode:2008CPL...456..223Y. doi:10.1016/j.cplett.2008.03.046
- ↑ Delaney, P.; Greer, J. C. (2004). «C60 as a Faraday cage». Applied Physics Letters. 84 (3). 431 páginas. Bibcode:2004ApPhL..84..431D. doi:10.1063/1.1640783
- ↑ Zope, Rajendra R (2008). «Electronic structure and static dipole polarizability of C60@C240». Journal of Physics B: Atomic, Molecular and Optical Physics. 41 (8). 085101 páginas. Bibcode:2008JPhB...41h5101Z. doi:10.1088/0953-4075/41/8/085101
- ↑ Langlet, R.; Mayer, A.; Geuquet, N.; Amara, H.; Vandescuren, M.; Henrard, L.; Maksimenko, S.; Lambin, Ph. (2007). «Study of the polarizability of fullerenes with a monopole–dipole interaction model». Diamond Relat. Mater. 16 (12): 2145–2149. Bibcode:2007DRM....16.2145L. doi:10.1016/j.diamond.2007.10.019
- ↑ Komatsu, K.; Murata, M.; Murata, Y. (2005). «Encapsulation of Molecular Hydrogen in Fullerene C60 by Organic Synthesis». Science. 307 (5707): 238–240. Bibcode:2005Sci...307..238K. PMID 15653499. doi:10.1126/science.1106185
- ↑ Kurotobi, K.; Murata, Y. (2011). «A Single Molecule of Water Encapsulated in Fullerene C60». Science. 333 (6042): 613–616. Bibcode:2011Sci...333..613K. PMID 21798946. doi:10.1126/science.1206376
- ↑ Whitby, Richard; et al. «The dipolar endofullerene HF@C60». Nature Chemistry. doi:10.1038/nchem.2563
- ↑ Levitt, M. H. (2013). «Spectroscopy of light-molecule endofullerenes». Philosophical Transactions of the Royal Society A: Mathematical, Physical and Engineering Sciences. 371 (1998). 20120429 páginas. Bibcode:2013RSPTA.37120429L. doi:10.1098/rsta.2012.0429
- ↑ Sabirov, Denis (2013). «From Endohedral Complexes to Endohedral Fullerene Covalent Derivatives: A Density Functional Theory Prognosis of Chemical Transformation of Water Endofullerene H2O@C60 upon Its Compression». J. Phys. Chem. C. 117 (2): 1178-1182. doi:10.1021/jp310673j
- ↑ DUVOISIN, Charles Adriano (2021). Armadilhas de elétrons suas curiosidades e aplicações físicas. República de Moldova/Europa: Novas Edições Acadêmicas. p. 117. ISBN 978-620-4-19366-3
