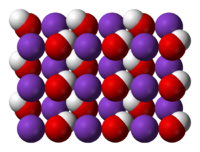
Hidróxido de potássio
O composto químico hidróxido de potássio, também conhecido como potassa cáustica é um hidróxido cáustico que tem a seguinte fórmula química: (KOH). Apresenta-se como um sólido branco, relativamente translúcido e em escamas finas praticamente incolor. Sua agregação está sempre em estado sólido. Se for ingerido, pode causar danos permanentes, inclusive a morte.
Possui muitas aplicações industriais e especiais. A maioria das aplicações explora sua reatividade com ácidos e suas características corrosivas. Em 2005, estimadas 700 mil a 800 mil toneladas foram produzidas. Aproximadamente 100 vezes mais hidróxido de sódio (NaOH - soda cáustica) é produzido anualmente que o KOH.[2][3][4] KOH é notável como o precursor da maioria de sabões líquidos e moles assim como numerosos compostos químicos contendo potássio.
Reações[editar | editar código-fonte]
Como uma base[editar | editar código-fonte]
KOH é altamente básico, formando soluções fortemente alcalinas em água e outros solventes polares. Estas soluções são capazes de deprotonar muitos ácidos, mesmo os mais fracos. Em química analítica, titrações (volumetrias) usando soluções de KOH são usadas para quantificar ácidos (mesmo em meios não aquosos, como o etanol, devido a sua solubilidade neste solvente).
Como um nucleóficlo em química orgânica[editar | editar código-fonte]
KOH, como o NaOH, serve como uma fonte de OH-, um ânion altamente nucleofílico que ataca ligações polares tanto em materiais orgânicos como inorgânicos. Em sua, talvez, mais bem entendida reação, KOH aquoso saponifica ésteres:
KOH + RCO2R’ → RCO2K + R’OH
Quando R é uma cadeia longa, o produto é chamado de um sabão de potássio. Esta reação é pelo toque "oleoso" que o KOH dá quando tocado – gorduras sobre a pele são rapidamente convertidas a sabão e glicerol.
Exemplo de saponificação envolvendo o KOH (www.fhsu.edu).
KOH fundido é usado para deslocar haletos e outros grupos removíveis de determinadas cadeias de carbono. A reação é especificamente útil para reagentes aromáticos que resultam nos fenóis correspondentes.
Reações com compostos inorgânicos[editar | editar código-fonte]
De maneira complementar a sua reatividade com ácidos, KOH ataca anidros, definidos no sentido mais amplo. Assim, SiO2 (e logo o vidro) e CO2 (mesmo o atmosférico) são atacados pelo KOH para dar os silicatos (quando no vidro, o que é chamado de "iridização") e bicarbonato, respectivamente:
KOH + CO2R → KHCO3
Esta reação é o que faz o hidróxido de potássio exposto tanto a umidade quanto ao CO2 atmosférico "carbonatar".
Produção[editar | editar código-fonte]
A maior parte do hidróxido de potássio utilizado é proveniente da eletrólise do KCl(cloreto de potássio), fundido a temperatura de 850 °C, onde a quebra da ligação ocorre pela passagem da corrente elétrica segundo reação: KCl ↔ K + Cl
K + 2Cl ↔ K + Cl₂↑
K + H₂O ↔ KOH + 1/2 H₂
Usos[editar | editar código-fonte]
Precursor de outros compostos de potássio[editar | editar código-fonte]
Os sais de potássio carbonato, cianeto, permanganato, fosfatos e vários silicatos são preparados por tratamento dos óxidos ou dos sais com KOH.[4] A alta solubilidade do fosfato de potássio é desejável em fertilizantes.
Produção de biodiesel[editar | editar código-fonte]
Embora mais custoso que usar o hidróxido de sódio, o KOH trabalha bem na produção de biodiesel por saponificação de gorduras em óleos vegetais. A glicerina do biodiesel obtido através do hidróxido de potássio é útil como um suplemento alimentar de baixo custo para pecuária (onde entra como uma fonte calórica), desde que o tóxico metanol seja removido.
Produção de sabões moles[editar | editar código-fonte]
A saponificação de gorduras com KOH é usada para preparar os correspondentes "sabões de potássio", os quais são mais macios que os mais comuns sabões derivados de hidróxido de sódio. Por causa de sua maciez e grande solubilidade, sabões de potássio requerem menos água para serem liquefeitos, e podem então conter mais agente de limpeza que sabões de sódio liquefeitos
Como um eletrólito[editar | editar código-fonte]
Hidróxido de potássio aquoso é empregado como o eletrólito em baterias alcalinas baseadas em níquel-cádmio, níquel-ferro e dióxido de manganês-zinco. Hidróxido de potássio é preferido em relação ao hidróxido de sódio porque suas soluções são mais condutivas.
Outras aplicações[editar | editar código-fonte]
Na identificação de fungos.
No processo de diafanização de vertebrados segundo o protocolo de Taylor e Van Dyke (1985), para estudo de ossos e cartilagens[5].
Referências
- ↑ a b c d Registo de CAS RN 1310-58-3 na Base de Dados de Substâncias GESTIS do IFA, accessado em 14 de Dezembro de 2007
- ↑ H. Schultz, G. Bauer, E. Schachl, F. Hagedorn, P. Schmittinger “Potassium Compounds” in Ullmann’s Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. doi:039 10.1002/14356007.a22 039
- ↑ "Caustic Potash." Oxy.com Arquivado em 25 de janeiro de 2009, no Wayback Machine.. (em inglês)
- ↑ "Potassium Hydroxide." MSDS Arquivado em 15 de outubro de 2008, no Wayback Machine. (em inglês)
- ↑ [5]Taylor, W. R. & Van Dyke, G. C. 1985. Revised procedures for staining and clearing small fishes and other vertebrates for bone and cartilage study. Cybium, 9: 107-119.