Imina
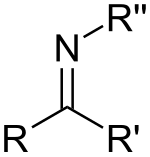
Uma imina é um grupo funcional ou composto orgânico com estrutura geral RR'C=NR'', onde R'' pode ser um H ou um grupo orgânico, sendo nesse último caso conhecida também como base de Schiff.[1][2]
As iminas são o produto da condensação do amoníaco ou uma amina primária com uma cetona ou um aldeído.
De forma análoga à dupla ligação dos alquenos, as iminas podem apresentar isomeria Z/E. Cabe se esperar que os critérios de estabilidade relativa de um isômero relacionado ao outro sejam os mesmos que com os alquenos (impedimento estérico).
Igualmente como na tautomeria ceto-enólica, também existe a tautomeria imina-enamina com predomínio da primeira (a imina).
Síntese[editar | editar código-fonte]
O mecanismo de formação da imina, de maneira simplificada, começa com a adição nucleófila da amina sobre o carbonilo eletrófilo do aldeído ou cetona, formando-se um hemiaminal como intermediário, o qual na continuação perde uma molécula de água para conduzir à imina.

A reação habitualmente requer catálise ácida. Além de ser uma reação de equilíbrio para conduzí-la até o produto há de se eliminar a água do meio de reação azeotropicamente ou mediante agentes desidratantes.
As formações de iminas está favorecida quando existe conjugação da ligação dupla carbono-nitrogênio com algum substituinte, tipicamente grupos arilo. Nestos casos a imina é relativamente estável.
Reações[editar | editar código-fonte]
- A imina pode ser reduzida a amina (aminação redutora).
- A imina pode ser hidrolisada com água aos correspondentes compostos carbonilo e amina.
- A imina reage com mais amina a um amimal.
- A imina reage com CN- na síntese de Strecker de aminoácidos.
- A sais de imínio resultantes da protonação de iminas podem ser intermediários, reagindo com nucleófilos de tipo enol, na reação de Knoevenagel e na reação de Mannich.
Ver também[editar | editar código-fonte]
- Aldeídos e Cetonas - grupo funcional C=O ligado, respectivamente, a um ou dois radicais orgânicos
- Oximas - grupo funcional C=(N-O-H) ligado a um ou dois radicais orgânicos
- Amidinas - grupo funcional C(=N)-NRR'
Referências
- ↑ IUPAC Compendium of Chemical Terminology, Electronic version, http://goldbook.iupac.org/I02957.html.
- ↑ IUPAC Compendium of Chemical Terminology, Electronic version, http://goldbook.iupac.org/S05498.html.
Bibliografia[editar | editar código-fonte]
- K. Peter C. Vollhardt (1994), Química Orgánica, Barcelona: Ediciones Omega S.A.. ISBN 84-282-0882-4.
