Succinato desidrogenase
Este artigo não cita fontes confiáveis. (Agosto de 2020) |

A succinato desidrogenase, succinato-coenzima Q redutase ou complexo II é uma flavoproteína ligada à membrana interna mitocondrial que intervém no ciclo de Krebs e na cadeia respiratória e que contém FAD (dinucleótido de flavina e adenina) unido covalentemente. Possui um peso molecular de cerca de 100 kDa, e contém uma molécula de FAD, oito átomos de ferro e oito átomos de enxofre lábeis frente aos ácidos. A enzima possui duas subunidades, cujos pesos moleculares são 30 kDa e 70 kDa respectivamente. A subunidade maior da succinato desidrogenase contém FAD, quatro átomos de ferro e quatro átomos de enxofre ácido-lábeis. A subunidade menor é uma ferro-sulfuro-proteína que contém quatro átomos de ferro e quatro de enxofre ácido-lábeis.
A molécula de FAD da enzima, é o aceitador de electrões da reacção. De maneira general a função bioquímica do FAD é oxidar os alcanos a alcenos, enquanto que o NAD+ oxida os alcóis a aldeídos ou cetonas. Isto é devido a que a oxidação de um alcano (como o succinato) a um alceno (como o fumarato) é suficiente exergónica como para reduzir o FAD a FADH2, mas não para reduzir o NAD+ a NADH. É pouco usual achar uma união covalente entre o FAD e uma proteína; na maioria dos casos, o FAD encontra-se unido à sua enzima associada de forma não covalente (união débil e transitória). Pelo que neste caso o FAD actua como grupo prostético e não como uma coenzima móvel, como o faz normalmente.
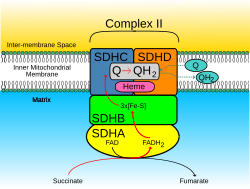
O FADH2 da succinato desidrogenasa, ao não poder desprender-se da enzima, deve oxidar-se novamente in situ. O FADH2 cede seus dois hidrogénios à ubiquinona (coenzima Q) que se reduz a ubiquinol (QH2) e abandona a enzima, difundindo na bicamada lipídica até alcançar o seguinte complexo enzimático da cadeia respiratória.
A succinato desidrogenase actua separando os átomos de hidrogénio que se acham na posição trans dos átomos de carbono metilénicos do succinato.
Esta enzima possui algumas características de uma enzima alostérica: é activada pelo succinato, o fosfato, o ATP e o coenzima Q reduzido , e é inibido pelo malonato, um análogo estrutural do succinato.
