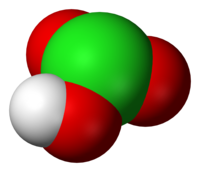
Ácido clórico
O ácido clórico (HClO3) é um oxiácido inorgânico do cloro. É um ácido forte (pKa ~ -2)[1] e um forte agente oxidante, cujo poder depende do pH do meio e é substancialmente maior em soluções ácidas[2].
Não é muito estável na forma pura; no entanto, sua estabilidade aumenta consideravelmente em solução aquosa, livre de impurezas e protegidas da luz[3] e mais ainda quando sal[4]. Na forma de solução, pode chegar a concentrações de até 30% em água fria, ou até 40% a pressão reduzida, mas que é logo acompanhada de sua decomposição em ácido perclórico (HClO4) e a evolução de gases cloro, oxigênio e dióxido de cloro[2]:
8HClO3(aq) → 4HClO4(aq) + 2H2O(l) + 2Cl2(g) + 3O2(g)
3HClO3(aq) → HClO4(aq) + H2O(l) + 2ClO2(g)
A tabela a seguir traz a densidade relativa de diferentes concentrações de ácido clórico[3].
| Concentração da solução | |
| 1% | 1,0044 |
| 6% | 1,0344 |
| 10% | 1,0594 |
| 16% | 1,0991 |
| 20% | 1,1273 |
| 24% | 1,1568 |
O ácido clórico explode caso se tente evaporá-lo à secura[5]. Ao ser aquecido, se decompõe liberando os gases oxigênio (O2) e dióxido de cloro (ClO2). Em temperaturas mais brandas, a decomposição do ácido clórico ocorre com o seu desproporcionamento, produzindo ácido perclórico (HClO4) e ácido clorídrico (HCl)[4].
4HClO3(aq) → 4ClO2(g) + 2H2O(g) + O2(g)
A decomposição dos cloratos depende de fatores termodinâmicos e cinéticos. Óxidos tendem a ser favorecidos na presença de um cátion polarizante forte (como magnésio, metais de transição e lantanídeos), enquanto a formação de cloreto é observada em cloratos de metais alcalinos, alcalinoterrosos e prata[2]. Os cloratos desproporcionam tanto em meio ácido quanto em meio básico:
4ClO3-(aq) ⇌ 3ClO4-(aq) + Cl-(aq) ∆rGº = -24kJ.mol-1 K=1,4.1025
No entanto, a reação é lenta tanto em pH alto quanto em pH baixo, e o ácido clórico é um ácido forte, de modo que os íons ClO3- podem ser facilmente manuseados em solução aquosa[6].
Obtenção[editar | editar código-fonte]
Cloratos podem ser obtidos borbulhando gás cloro (Cl2) em uma solução de hidróxido de sódio (NaOH) quente e eletrolisando o cloreto (Cl-) formado em soluções quentes sob vigorosa agitação. Nesse processo, somente ⅙ do cloreto é convertido em clorato. No entanto, o cloreto de sódio (NaCl) gerado é eletrolisado novamente, não havendo perdas[5].
6NaOH(aq) + 3Cl2(g) → NaClO3(aq) + 5NaCl(aq) + 3H2O(l)
2Cl-(aq) + 2H2O(l) → Cl2(g) + H2(g) + 2OH-(aq)
Analogamente, podem ser eletrolisadas soluções de cloreto de potássio (KCl) 25% a 70-75ºC até estar saturada de clorato de potássio. A solução é resfriada e o clorato de potássio é cristalizado[1].
Contudo, para produção em larga escala, são recomendadas outras rotas. Industrialmente, o ácido clórico é produzido pela eletrólise da salmoura em cela diafragmática, que promove uma mistura mais eficaz. O gás cloro produzido no anodo reage com os íons hidróxido produzidos no catodo, formando hipoclorito que se desproporciona ou é oxidado a clorato[2]:
Reação anódica: Cl-(aq) → ½ Cl2(g) + e-
Reação catódica: H2O(l) + e- → ½ H2(g) + OH-(aq)
Mistura: Cl2(g) + 2OH-(aq) → Cl-(aq + ClO-(aq) + H2O(l)
Desproporcionamento: 3ClO-(aq) → ClO3-(aq) + 2Cl-(aq)
Oxidação: ClO-(aq) + 2H2O(l) → ClO3-(aq) + 2H2(g)
Em células eletrolíticas modernas, usa-se anodo de dióxido de titânio (TiO2) coberto de algum metal nobre e catodo de aço, separados por 3mm de distância, com uma corrente elétrica de 2700A.m-2 em uma salmoura 80 a 100g.L-1 em temperaturas de 60 a 80ºC. Nessas condições, a eficiência do processo é de 93%, e uma tonelada de clorato de sódio (NaClO3) pode ser obtida a partir de 565kg de cloreto de sódio usando 4535kWh de eletricidade. Também é coletado gás hidrogênio (H2) no processo[2].
O ácido clórico, em laboratório, pode ser obtido pela reação do clorato de bário (Ba(ClO3)2) com ácido sulfúrico concentrado, removendo o sulfato de bário por filtração[4] ou a partir de clorato de sódio e resinas trocadoras de íons[3].
Ba(ClO3)2(aq) + H2SO4(aq) → 2HClO3(aq) + BaSO4(s)
Os cloratos também são produzidos a partir da decomposição térmica de hipocloritos[4].
Riscos[editar | editar código-fonte]
Cloratos podem explodir na moagem, durante o aquecimento ou em contato com substâncias facilmente oxidáveis, como materiais orgânicos e enxofre. É perigoso na forma sólida e é muito mais seguro na forma de solução[5].
O ácido clórico é extremamente irritante à pele e às mucosas[3].
Aplicações[editar | editar código-fonte]
O ácido clórico é utilizado como método de preparar pequenas quantidades de gás oxigênio em laboratório[2], como agente oxidante no tratamento de materiais e, junto do ácido sulfuroso, é catalisador no processo de polimerização da acrilonitrila[3].
O ácido clórico também pode ser utilizado para produzir ácido iódico (HIO3) a partir de sua reação com o iodo[4].
Os cloratos (sais derivados do ácido clórico) possuem diversas aplicações. O clorato de sódio é utilizado como herbicida e também por terroristas na confecção de bombas. No entanto, as bombas não são confiáveis e são extremamente perigosas[5]. Também são utilizados na produção de fósforos de segurança e fogos de artifício. Os cloratos de metais alcalinos desproporcionam quando fundidos[2]:
4ClO3-(aq) → Cl-(aq) + 3ClO4-(aq)
| Clorato | Ponto de fusão (ºC) | Temperatura de decomposição (ºC) |
| LiClO3 | 125 | 270 |
| NaClO3 | 248 | 265 |
| KClO3 | 368 | 400 |
Na presença de metal de transição catalisador, como MnO2, a decomposição do clorato de potássio a cloreto de potássio e gás oxigênio começa em 70ºC e é vigorosa a 100ºC:
2ClO3-(aq) → 2Cl-(aq) + 3O2(g)
Referências
- ↑ a b c Registo de Chlorsäure na Base de Dados de Substâncias GESTIS do IFA, accessado em 4 de Janeiro de 2008
- ↑ Nils Wiberg, Egon Wiberg, Arnold Fr. Holleman (2007). Lehrbuch der Anorganischen Chemie 102 ed. Berlin: de Gruyter. ISBN 978-3-11-017770-1
[1] HESLOP, R. B.; ROBINSON, P. L. Inorganic Chemistry: A Guide To Advanced Study. 3ª ed. Londres: Elsevier, 1967, pp. 531-532
[2] GREENWOOD, N. N.; EARNSHAW, A. Chemistry of the Elements. 2ª ed. Oxford: Elsevier, 1997, pp. 862-865
[3] O’NEIL, M. J. et al. The Merck Index. 14ª ed. Whitehouse Station: Merck Research Laboratories, 2006, pp. 346-347
[4] MOELLER, T. Inorganic Chemistry: An Advanced Textbook. 2ª ed. Nova York: John Wiley & Sons, Inc., 1953, pp. 438 e 441
[5] LEE, J. D. Química Inorgânica não tão concisa. 5ª ed. São Paulo: Blucher, 1999, p. 310
[6] SHRIVER, D. F.; ATKINS, P. W. Química Inorgânica. 4ª ed. Porto Alegre: Bookman, 2006, pp. 175 e 176